認知症の治療(総論)
地域の中で普段通りの生活を維持することがもっとも認知症の進展予防効果がある
もっとも進行が速いタイプは会社員でリタイアし、独居で趣味や地域との接点がなく、介護サービスも利用したがらないタイプ→都心型の生活環境に多い
もっとも進行が遅いタイプは認知症発症後も自営業を手伝いながら、普段からお茶友達とおしゃべりをし、老人会やデイサービスにも進んで参加するタイプ→郊外型の生活環境に多い
認知症の人でも生存本能は最後まで残る(危険回避、食事、睡眠、排泄・・・)
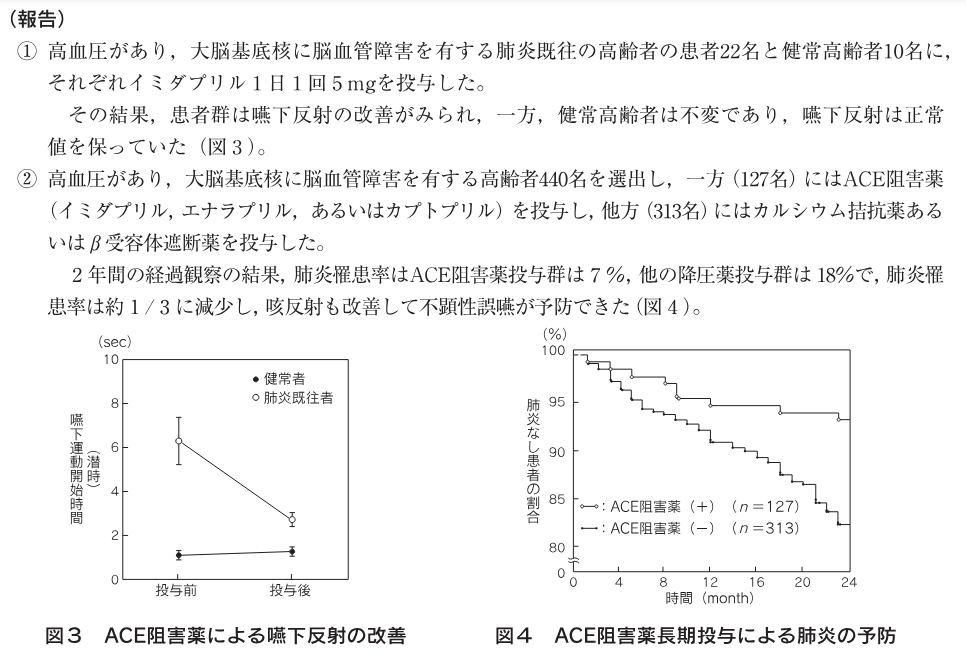
誤嚥性肺炎の予防
嚥下障害診療ガイドライン→ACE阻害薬、シロスタゾール、ニセルゴリン、半夏厚朴湯の記載あるが、エビデンスレベルは高くない
- ACE阻害薬(イミダプリル、エナラプリル、カプトプリル)
- ACE阻害薬は「脳卒中治療ガイドライン」に記載あり
- 2年間のfollowでACE阻害薬群の肺炎7%vsその他の降圧剤18%と有意に低下
- アマンタジン
- パーキンソン病の人なら処方できる?
- シロスタゾール
- 徐脈性不整脈「不整脈薬物治療に関するガイドライン」に記載されている→洞性徐脈性不整脈の方で、ペースメーカの埋め込みをしない場合などに使用されます
- 半夏厚朴湯

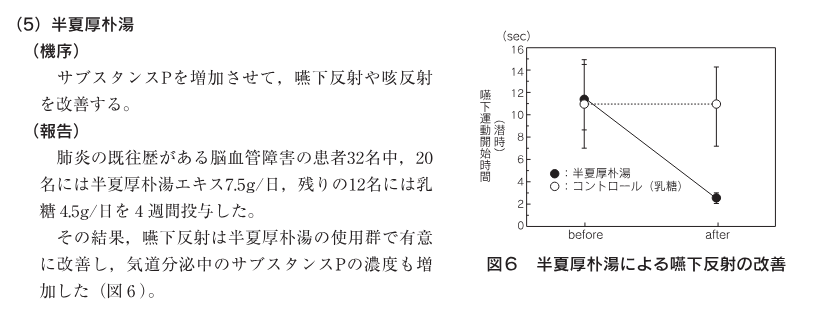
認知症の人とのコミュニケーション法
体調を聞くとき→いまのことを聞かないと覚えていない
◎いま、どのように感じているか?
×最近、どうですか?
生活状況については、ストレングスのヒアリングを重視する
生活状況を家族に質問する前には本人にも了解を得る
◎楽しみ、できていること、やりがい、役割
×できなくなったこと、失敗していること
もっと重症になって心情を伝えられなくなったとき
→認知症の人が抱きやすい心情を代弁して家族や介護者に伝える
帰宅願望や一人歩きなどのチャレンジング行動が見られたときに、当事者を中心としてその理由と対策を考える流れができる
認知症 Neurocognitive disorder(総論)
高齢者(>65歳)の5人に1人が認知症
4大認知症で認知症全体の90%を占める
スクリーニング→
認知症初期症状11質問票(SED-11Q)
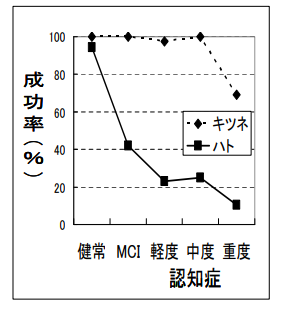
キツネ・ハト模倣テスト、(+逆キツネ)→20秒でスクリーニング可能
HDS-R(Hasegawa’s Dementia Scale-Revised:改訂長谷川式認知症スケール)→30点満点
HDS-Rは20点以下が認知症疑いで感度93%、特異度86%
MMSE(Mini-Mental State Examination:ミニメンタルステート検査)→30点満点
23点以下が認知症疑いである(感度81%、特異度89%)
27点以下は軽度認知障害(MCI)が疑われる(感度45-60%、特異度65-90%)
15点以下になってくると独居生活が困難になってくる→1年以内の施設入所をの準備を始める
この検査は実施も判定も簡便で、忙しい外来診療で無理なく、また患者さんの負担も少なく実施出来る点で非常に有用
頭頂葉~後頭葉の障害を検査する
本テストはゲーム感覚で気軽にやっていただけます。手掌・手掌パターンは、本人が誤りに気づかない場合が多く、本人の気持ちを傷つけないですみます。間違えても「良くできました」と言いましょう。また、「見え方をチェックする検査です」と伝えると、患者さんは正否をあまり気にしなくなるようです。

キツネは中等度の認知症までほぼ全員ができる(重度認知症では不能に)
キツネは左手で見本を作りますが、患者さんはどちらの手で作っても正解
ハトは両手を組み合わせますが、どちらの手が上(外側)になっても正解
評価:
ハトは軽度認知症(CDR1)で8割近くができなくなり、MCIでも約5割が間違います。
視空間認知やボディイメージの障害が、アルツハイマー病の早期からみられるようです。
認知症が疑われれば、除外診断でADと診断する
臨床における認知症の病型診断は治療を前提に考えた方が良い。
最も大事なのはレビー小体型認知症と前頭側頭型認知症(ピック病)を見逃さないことである。
レビー小体型認知症は薬剤感受性が高く、認知症治療薬(コリンエステラーゼ阻害薬)の副作用が出やすく、ピック病はコリンエステラーゼ阻害薬により興奮性の行動・心理症状(BPSD)が悪化することが多いからである。
前頭側頭型認知症(ピック病)は、簡単に言うと元気があって怒りっぽい、興奮しやすい認知症である。
純粋なピック病は若年者であるが高齢者でもピック病は少なくない。
対してレビー小体型認知症は弱々しく元気が無くて、歩行はヨチヨチ歩き(パーキンソン様)、椅子に座ると身体が傾いている患者さんである(体幹傾斜)。寝言や夜中の大声もレビー診断のヒントになる。
この両者を除外した上でアルツハイマー型認知症と脳血管性認知症を区別する。
日常診療におけるアルツハイマー診断は指模倣テストと時計描画テストが有効である。
ドネペジル(アリセプト)は前頭葉の賦活作用が最も強いが、同時に易怒、興奮、妄想、徘徊などの興奮性のBPSDを悪化させることがある。

- 認知症診療ガイドライン2017(日本神経学会)
- 定義:
認知症は後天的に生じる病的な知能低下により日常生活に支障をきたす状態(健常者でも加齢に従い軽度低下傾向となる) - 疫学:
- 令和3年10月1日現在、1億2,550万人、65歳以上人口は、3,621万人となり、高齢化率は28.9%
- 「日本における認知症の高齢者人口の将来推計に関する研究」の推計では、65歳以上の認知症患者数は2020年に約602万人、2025年には約675万人(有病率18.5%)と高齢者の5.4人に1人程度が認知症になると予測されている
- ピーク時には1000万人を超えると予想されている
- 原因疾患:
アルツハイマー病が6割、次いで脳血管性認知症(2割)、Lewy小体型認知症(4%)(3大認知症)となるが、それぞれ特徴的な症状があるため、臨床的に鑑別する(ADやDLBの確定診断には剖検が必要) - 認知症は緩徐進行性の疾患で、発症すると進行を止めることは困難(薬物療法でも無理!)
- 昔は痴呆=dementiaと呼んでいたが、差別的なネーミングのため神経認知障害=Neurocognitive disorder(DSM-5より)と変更された
- https://g.kawasaki-m.ac.jp/data/2015/125/
DSM―5 診断基準
認知機能を「複雑性注意」,「実行機能」,「学習と記憶」,「言語」,「知覚―運動」,「社会的認知」の 6 領域に分類し,認知機能を記憶のみでなく,より広範囲にとらえるようになりこれらの複数ある認知機能のうちのどこかが障害されている状態像を総称することとなった(記憶障害は必須ではなくなった)

- 「健常」でも「認知症」でもない、それらの中間に位置していて、心理検査(認知テスト)などで客観的に認知機能低下がみられる状態のことをいい認知症の前段階ともいえる状態
- 65歳以上の高齢者の15~25%に軽度認知障害がみられ、1年間に高齢者1000人当たり20~50人が新たに軽度認知障害を発症する
- 軽度認知障害の人は1年間に5~15%の割合で認知症を発症する
- この時期の過ごし方が非常に重要で、運動不足の改善、糖尿病や高血圧症等の生活習慣病の予防や治療、社会参加による社会的孤立の解消や役割の保持等を徹底的に行うことにより、認知症の発症を遅らせることができる可能性が示唆されている。
- 1年間に16~41%は健常に戻るとも報告されており、適切な時期での対応が大切→物忘れ外来に受診
認知症の危険因子と非薬物療法
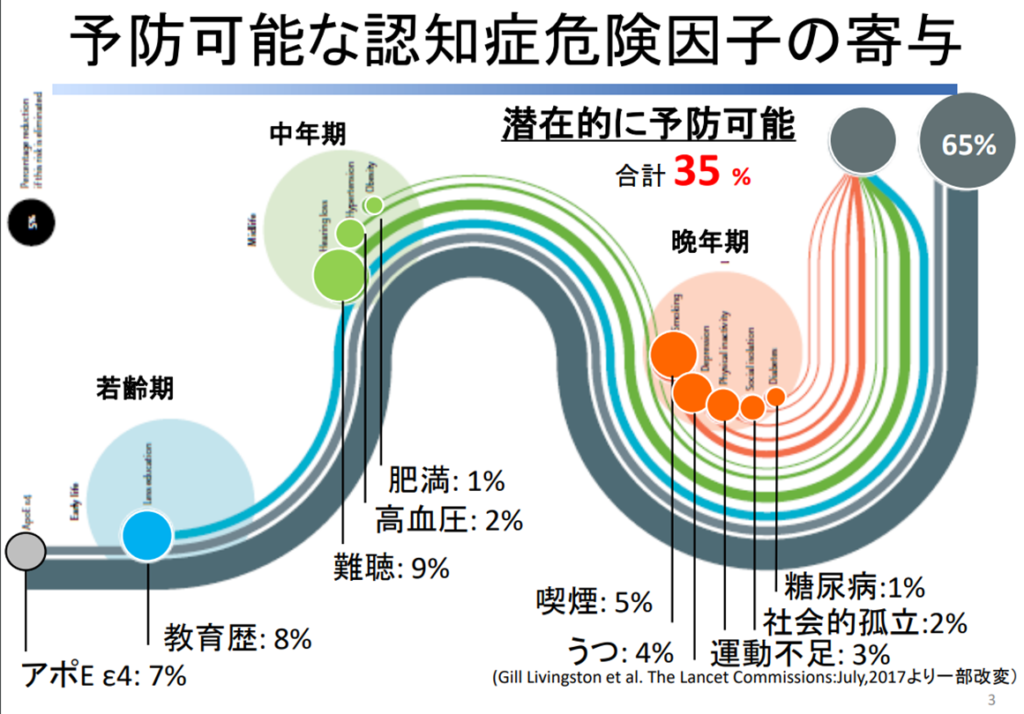
加齢、遺伝性のもの、高血圧、糖尿病、喫煙、頭部外傷、難聴、うつ病、糖尿病治療による低血糖、貧血、便秘等
もっとも割合が大きいのが中年期(40~64歳)の難聴で8%
補聴器による認知機能保持の有用性が認められたため、耳鼻科外来(補聴器相談医)での補聴器導入を勧める
運動、食事、余暇活動、社会的参加、認知訓練、活発な精神活動等
- 高血圧は血管性認知症のリスク因子
- 糖尿病はアルツハイマー型認知症のリスク因子(日本糖尿病学会による高齢者のDM管理目標は空腹時血糖<140未満、HbA1c<7.4未満、BMI=22)
認知症予防のためには
・高血圧、糖尿病、肥満の治療および予防
・運動がエビデンスレベルが高いが、脳トレは効果期待できない
・国立長寿医療センターではコグニサイズ(運動+脳トレ)を推奨している
・食事療法として地中海食(オリーブやナッツ)、大豆、緑黄色野菜、単色野菜、海藻類、牛乳・乳製品
- たとえ軽度でも貧血がある高齢者では、貧血がない高齢者に比べて認知症を発症するリスクが上昇し、アルツハイマー病のリスクは41%高くなる→Neurology(2019; 93: e917-e926)
認知症の病型診断とTreatable Dementia
認知症の原因となる疾患は70にもなる→すべてが鑑別可能ではない
Treatable Dementiaとして内服薬剤と甲状腺機能は一度はチェックが必要

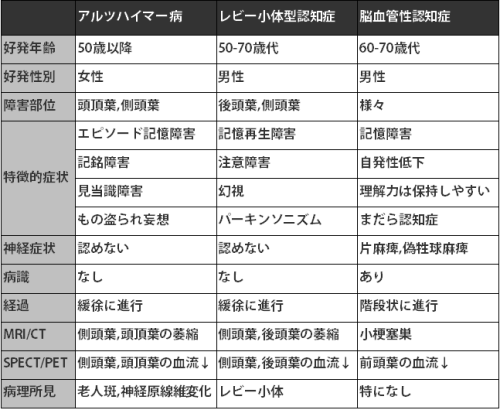
認知症の臨床像
頭を使っている人の方が認知症になってからも進行が遅い
→レーガン元米国大統領、サッチャー元英国首相
仕事(畑とか職人系)など、長年やっていることは認知症になってもできる!
思考力や計算力、理解力は初期には保持される
運転自体はできるだろうが、道がわからなくなり、混乱した結果、高速道路を逆走したり路肩走行したりする
- 初期症状:
- 記憶障害(=記憶系)により、5分前の会話は覚えていなくても理解や知能は正常(=理解系、思考系、感情系、運動系、)なので、現在進行中の会話は成立している
短期記憶→海馬
長期記憶→大脳皮質
海馬は、記憶をつかさどる脳の部位で、脳に記憶を保持するための役割を果たしている。
脳の老化に最も先行して30代より萎縮が始まる一方、脳の中で唯一、海馬だけは神経が生まれ変わり、萎縮を抑えて大きくすることもできる。
タツノオトシゴのような形をしていて、左右に一対ずつあり、それぞれ小指ほどの大きさ。
海馬が働かなくなると、私たちは新しいことが覚えられなくなる、つまり、昔のことは覚えていても、新しいことはすぐに忘れてしまう。
海馬はいわゆる「記憶の司令塔」とでもいえるとても大切な場所ですが、とても壊れやすく、酸素不足で脳がダメージを受けるとき、最初に海馬あたりから死んでいくといわれている。
PTSDなどの強いストレスでも、海馬に異常が現れる。
海馬は高性能ですが、とても繊細で壊れやすい精密機械のようなもの。
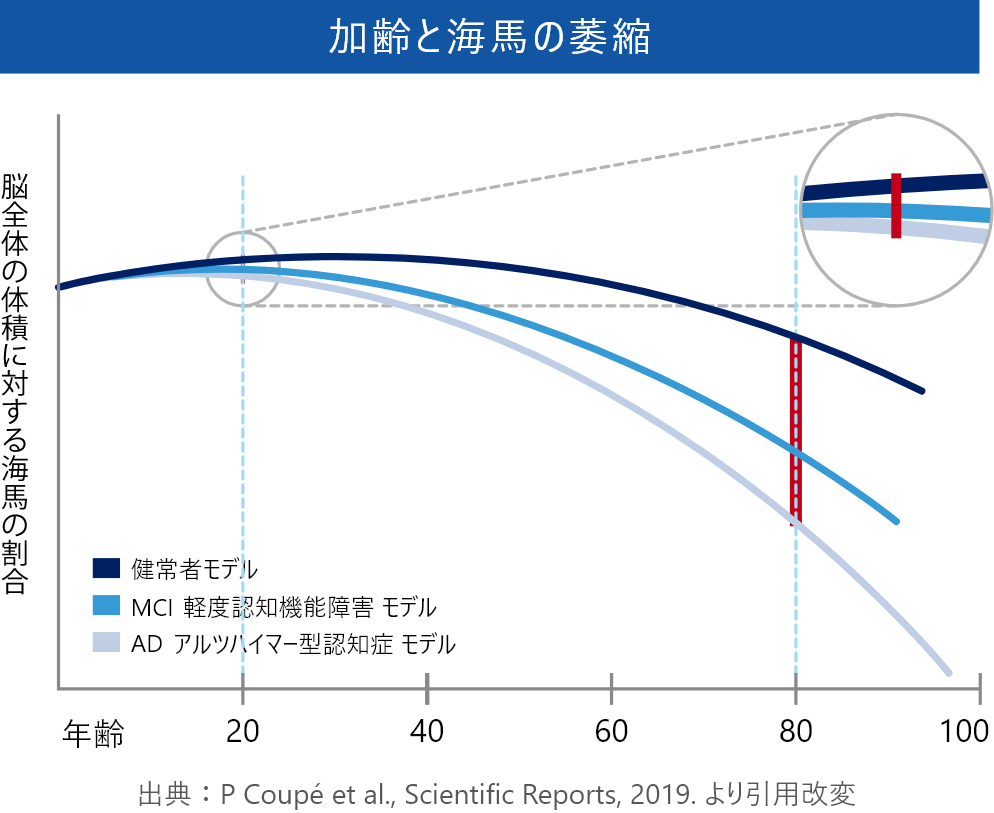
- 海馬の萎縮を加速させる因子
- ストレス
ストレスが増えると、コルチゾールというストレスホルモンの一種の分泌が過多となり、海馬の萎縮リスクが高まり、海馬の神経新生も抑制される - 睡眠不足
睡眠不足は身体への負担を増加させ、ストレス増加・免疫力の低下をもたらす - 過度のアルコール摂取
- 運動不足
- ストレス
認知症薬物治療(総論)

脳血管性認知症(VD)の薬物療法
意欲低下→サアミオン
興奮→グラマリール(抗精神病薬)、抗てんかん薬
VDには抗認知症薬使用しない(予後を悪化させたというデータもあるらしい)
MCIから認知症への進行を予防する有効性は示されなかった。
血中βアミロイドの複合体 (アルブミン-Aβ複合体) の濃度が、治療前に比べ増加する傾向が示されシロスタゾールが脳内のβアミロイドを、血液中に排出することを促進させた可能性が示唆された。
1999 年になり治療薬であるドネペジル(アリセプト)が登場したが、期待されたものの治療成績は悪く、一年後評価では過去の治療成績に劣った。またドネペジルを使うようになって以降、易怒性や妄想が悪化する症例が増え、介護者が困惑することになった。
病棟では肺炎や骨折などで入院する患者の中に、ドネペジルによる精神障害や運動障害を多く経験し、胃ろう造設目的で入院された患者が、薬を止めることで食事が取れるようになるなどの改善例が続いた。これらの副作用症例は全て会社に報告したが、情報がどのように扱われたかは判らない。
2000 年代に私が行っていた治療はドネペジル半量投与であった。長期的には半量の方が規定量よりも有効率が高く、悪化率が低かったのである。
この 10 年の啓蒙活動により、地域で治療薬を規定量で処方する医師は減り、治療効果を上げながら副作用症例は激減した。
池袋病院 平川 亘先生
→https://www.jstage.jst.go.jp/article/jsdtc/7/2/7_143/_pdf/-char/ja
抗アミロイド抗体医薬:アデュカヌマブaducanumab
米国で迅速承認されたものの、日本では、承認申請時のデータでは有効性を明確に判断することは困難であるとして、昨年12月、承認見送り(継続審議)となった
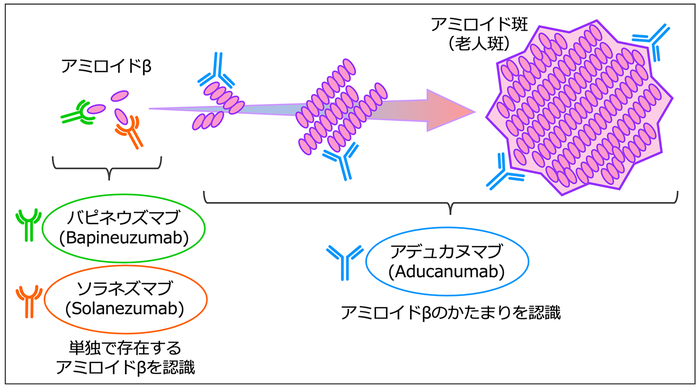
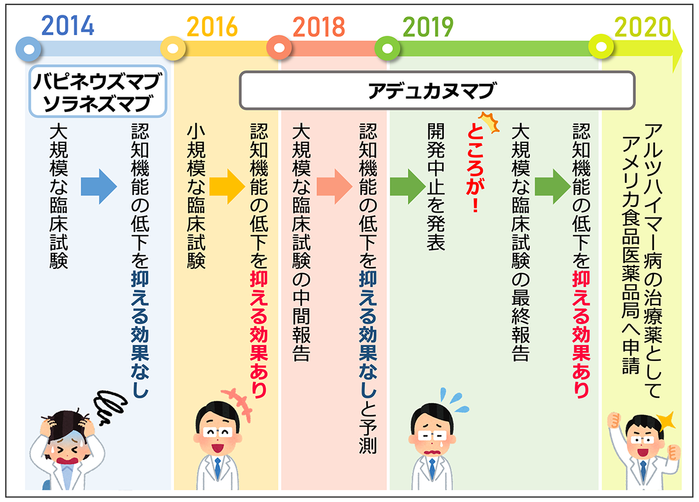

アミロイドβに対する抗体医薬の問題点
抗体医薬を高用量で投与すると、一部の被験者の方にARIAs(Amyloid-Related Imaging Abnormalities)と呼ばれる脳浮腫が見られた。
もう一つの問題は、BBBの影響で血液中に投与した抗体医薬のわずか0.1%しか脳の中に届かない。この問題に対しても、抗体医薬が脳に取り込まれやすくする工夫を施すことで、脳への取り込みを8倍程向上できることが報告されている。
アルツハイマー病を発症した後に、抗体医薬などで脳からアミロイド斑を減らしても、認知機能の低下を止めることはできない、またはその効果は限定的であることがわかった。
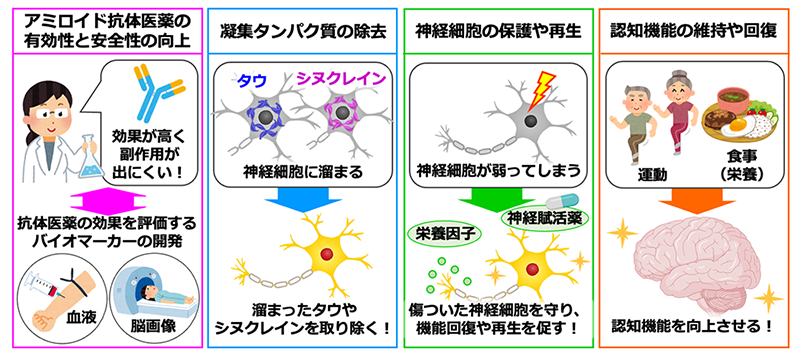
抗アミロイド抗体医薬:レカネマブ(レケンビ)
レカネマブとドナネマブの臨床試験では、脳内に溜まったアミロイドβを減らすことに加えて、認知機能や自立して生活を送る能力の低下を30%程遅らせる効果(症状の進行をおよそ7.5カ月遅らせる効果)が認められました。ただしこの効果は、患者さんに接しているご家族や、介護、医療従事者が実感するのは難しいと言われています。なぜなら、抗体医薬を投与した患者さんにおいても、認知機能は低下を続けてしまうからです。
- 2023年12月20日に発売
- 「レケンビ」はCDR-SBにおける18カ月時点の臨床症状の悪化をプラセボと比較して27%抑制しました。また、副次評価項目の一つである、衣服の着脱、食事、地域活動への参加など当事者様が自立して生活する能力を介護者が評価するAD Cooperative Study-Activities of Daily Living Scale for Mild Cognitive Impairment(ADCS MCI-ADL)においては、プラセボと比較して37%の統計学的に有意なベネフィットが認められました。なお、「レケンビ」投与群で最も多かった有害事象(10%以上)は、Infusion reaction、ARIA-H(ARIAによる脳微小出血、脳出血、脳表ヘモジデリン沈着)、ARIA-E(浮腫/浸出)、頭痛および転倒でした。
認知症と法整備
共生社会の実現を推進するための認知症基本法
基本法とは具体策のない法律全般のこと(〇〇基本法はすべて同じ性格)
『認知症のこと正しく理解しましょうね』っていう法律
→https://www.mhlw.go.jp/content/12300000/001119099.pdf
若年性認知症
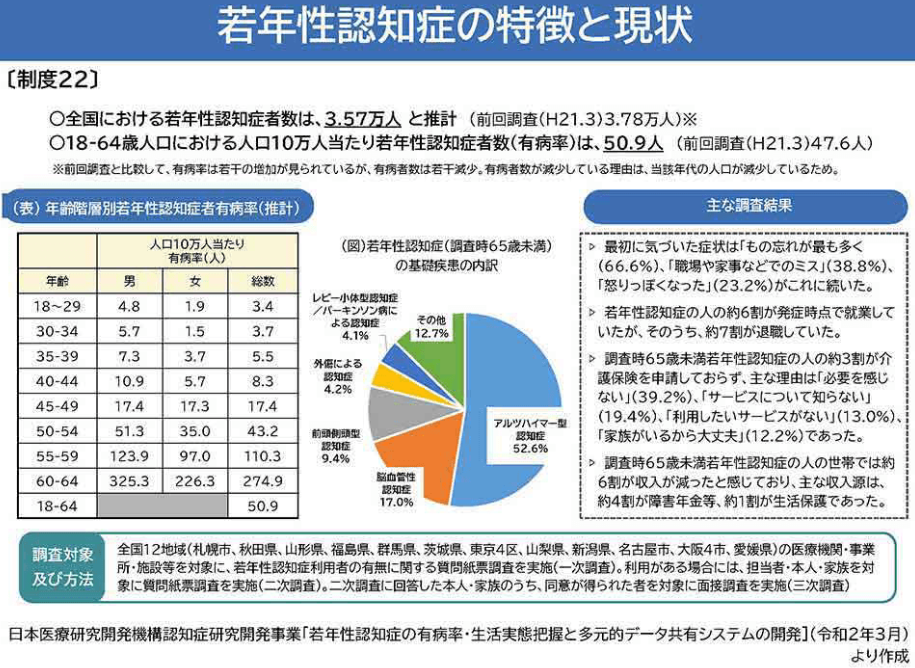

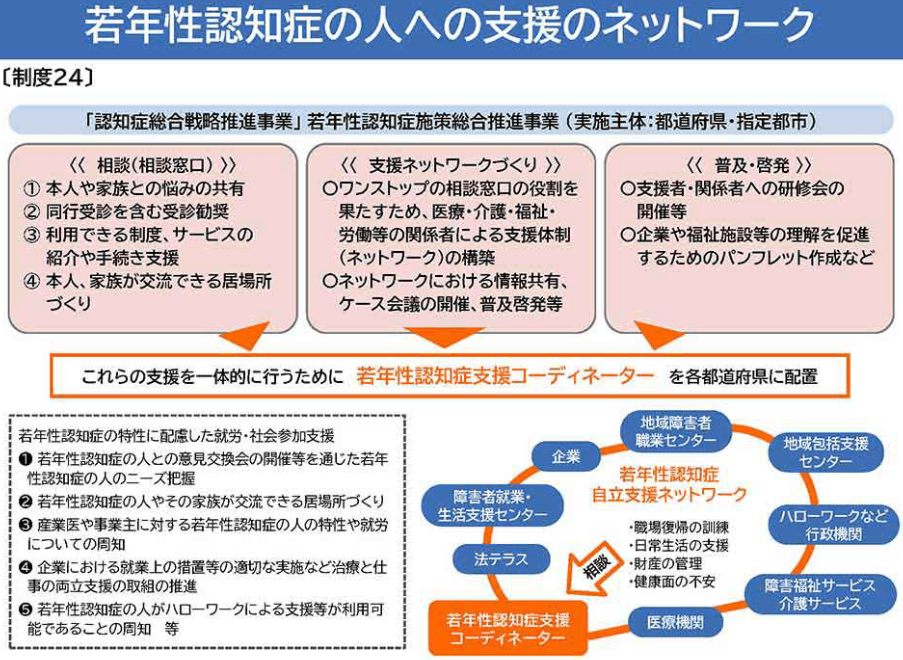

アルツハイマー型認知症
CDR(認知症の重症度評価)→レカネマブの治療適応評価(CDR0.5~1が適応、最高3点)に使用されるため、使用頻度が急増
DASC-21→日本独自の認知症アセスメント
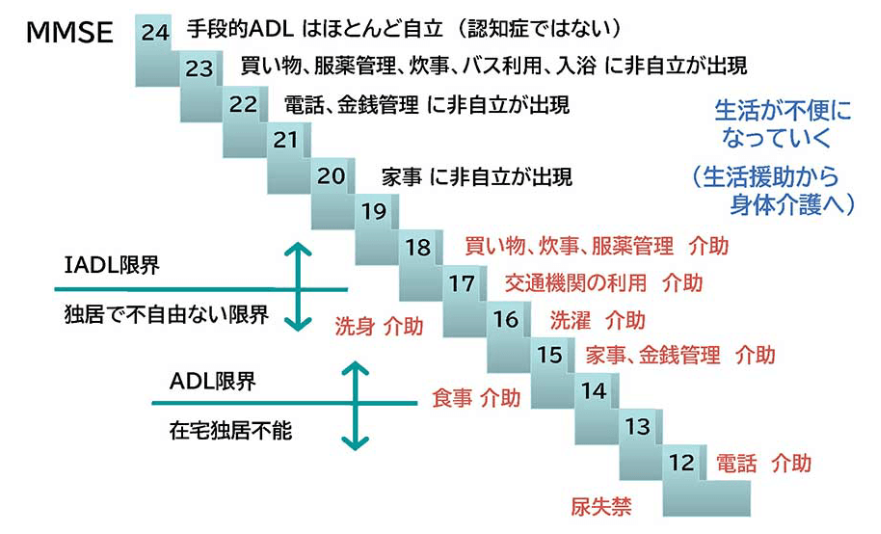
和田秀樹先生
80歳以上の脳の剖検すると、ほぼ全例、アルツハイマー型認知症の変化がある
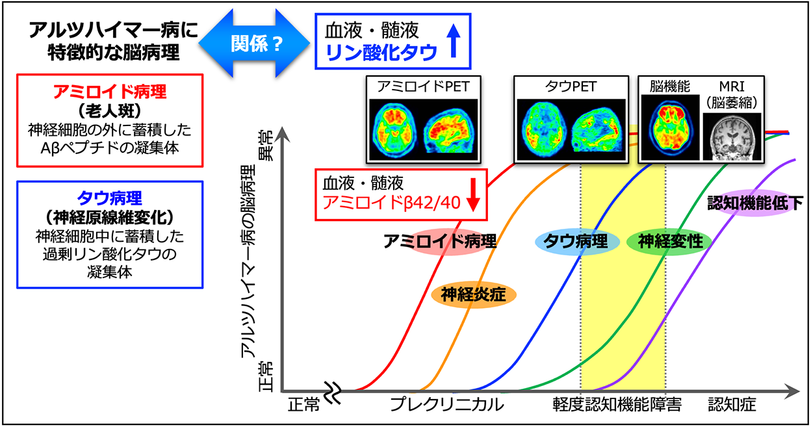
脳実質(神経細胞外)へのアミロイドβの蓄積(アミロイド病理)と,神経細胞内へのリン酸化タウタンパク質の蓄積(タウ病理),そして神経細胞死による脳萎縮を特徴とする進行性の神経変性疾患
→アルツハイマーの診断に関するリキッドバイオマーカーの開発研究が進んでいる
ADの病態解明と診断技術
認知症発症の10~20年前(50歳代ころ)からアミロイド蓄積は始まっていると考えられている
バイオマーカーの開発
→血液中のアミロイド検出技術が治験段階
MCIで診断して認知症発症を予防できる治療の開発が目標
→期待されたプレタールはnegativeだった

ADは子どもの発育と逆の流れ(→病気ではなく加齢性の自然な変化では?という人もいる)

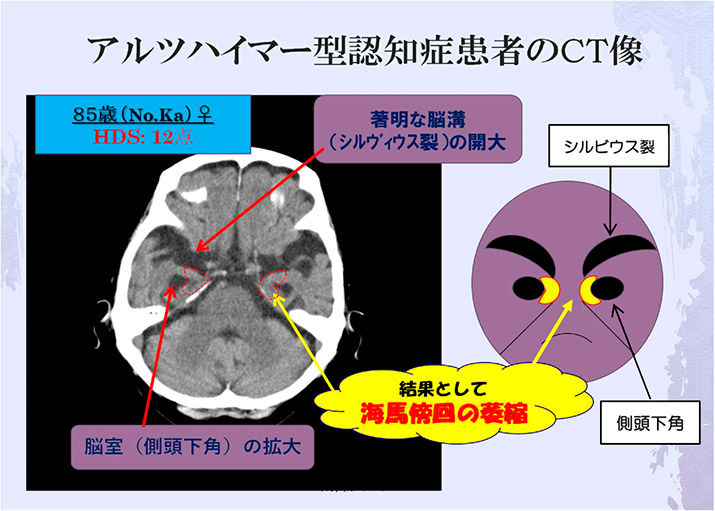
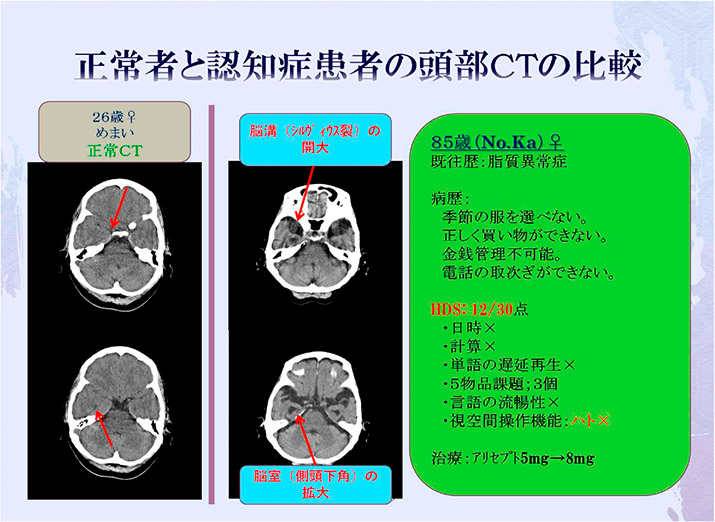
https://www.ishizawa-clinic.jp/medical/dementia03.html
ADの重症度分類と自然経過
予後良好で老衰で死亡するケースが多い
一方、脳血管性認知症は予後不良で誤嚥性肺炎などで死亡することが多い

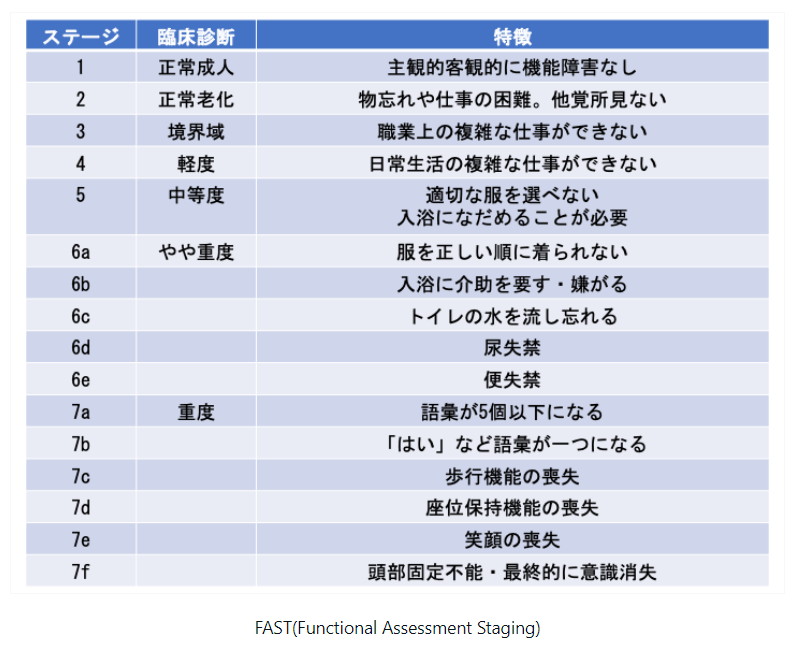
FAST6以上は便失禁、尿失禁、弄便などの症状が出るため、自宅での介護困難者が多くなる
AD薬物療法

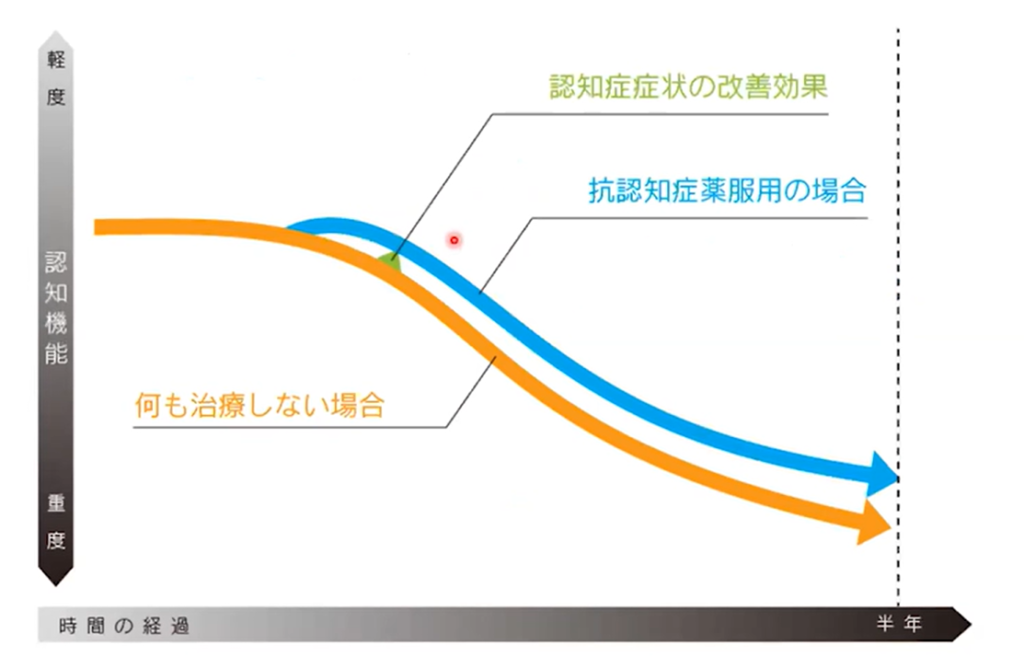
アリセプトで興奮したからメマリー足すというのはダメ!
→まずはアリセプトをやめる
常に進行性
→MMSEで3点/年程度低下していく
中核症状
→3種類のChE阻害薬±メマンチンで合計6通りの治療法から選択する
適応はいずれもADだが,血管性認知症に対しても同程度の効果を有することが複数のRCTで報告
周辺症状
→症状に応じて対応
- ChE阻害薬:
- 認知症の病態そのものの進行を抑制するという成績は得られていないと添付文書に明記されている
- 認知症症状の進行抑制はどれでも大差はない、プラセボとの比較でMMSEを1.37点改善する程度にとどまる
- 12人治療して1人に治療効果がでて、1人に副作用が出る
- 副作用:嘔気・下痢、食欲低下、徐脈・血圧低下、睡眠障害
- 興奮や怒りやすいなどの症状が出ている人は、より興奮しやすくなってしまうことがあるので、減量を考慮する
- ChE阻害薬の種類と特徴
- ◎アリセプト(ドネペジル):
- 初回投与は3㎎(忍容性の確認)→1~2週間後に5㎎(維持量)→4週後、重症例では10㎎まで増量
- アルツハイマー型認知症に対する当院でのドネペジルの治療成績は規定量の半分である2.5㎎が最も良かった(単施設の研究)
- コリンエステラーゼ阻害剤の過量投与は高度な嘔気、嘔吐、流涎、発汗、徐脈、低血圧、呼吸抑制、虚脱、痙攣及び縮瞳等のコリン作動性クリーゼを引き起こす可能性がある→アトロピン硫酸塩水和物の1.0~2.0mgを初期投与量として静注する
- 副作用:
- QT延長(0.1~1%未満)、心室頻拍(Torsade de pointesを含む)、心室細動、洞不全症候群、洞停止、高度徐脈(各頻度不明)、心ブロック(洞房ブロック、房室ブロック)、失神(各0.1~1%未満)心停止に至ることがある
- 錐体外路障害(アルツハイマー型認知症:0.1~1%未満、レビー小体型認知症:9.5%)
寡動、運動失調、ジスキネジア、ジストニア、振戦、不随意運動、歩行異常、姿勢異常、言語障害等 - 精神神経系(0.1~1%未満)
興奮、不穏、不眠、眠気、易怒性、幻覚、攻撃性、せん妄、妄想、多動、抑うつ、無感情
- アリドネパッチ(ドネペジルパッチ):
- 2022年に薬事承認
- (イクセロンパッチ、リバスタッチパッチ)リバスチグミン:パッチ製剤
- 覚醒作用が強く効果発現が極めて速い
- リバスチグミンは規定量の半分の9㎎でも過量投与になることが多く、高齢者の治療成績は4分の1量の4.5㎎あるいは2.25㎎が最も良い
- アセチルコリンエステラーゼ阻害とブチリルコリンエステラーゼ阻害を持つ
- レビー小体型認知症に対してはリバスチグミンが他よりも効果を有する
- ※ニュープロパッチはパーキンソン病治療薬
- (レミニール)ガランタミン:
- ニコチン性アセチルコリン受容体刺激作用を持つ
- アルツハイマー型認知症に対する2年以上の長期治療成績はガランタミン(レミニール)が最も優れていた(単施設の研究データhttp://www.hhk.jp/gakujyutsu-kenkyu/ika/181020-100000.php)
- ガランタミンは興奮などの副作用は少ないが、吐気、傾眠、めまい、失禁などが目立ち、半年以上の治療では体重の異常減少が目立つ
- 規定量で治療できることも多いが、時に患者の元気を奪うため上記二剤と同様に無理な増量は避けるべき
- NMDA阻害薬=メマリー(メマンチン塩酸塩):
興奮やソワソワして落ち着きがなくなる「焦燥感」などの症状を抑える- 初回投与は5㎎→10㎎→15㎎(BPSDの改善目的の場合は5~15㎎で維持)→20㎎(中核症状の改善目的)
- CCr<30ではmax10㎎までとする
コリンエステラーゼ阻害薬

- 認知症で障害されるのは家庭外IADL→家庭内IADL→BADLの順に障害される
- ADL(Activities of Daily Living、日常生活動作)
- IADL(Instulmental ADL、手段的日常生活動作能力)
買い物や家事、金銭管理など何かをするための少し複雑な動作 - BADL(Basic Activities of Daily Living、基本的日常生活動作能力)
食事や入浴、トイレ、着替えなど生活において最低限必要となる動作
- IADL(Instulmental ADL、手段的日常生活動作能力)
- BADLを評価する方法はいろいろあり、日本では主に次の2つが用いられる。
- Barthel Index(バーセル指数・バーセルインデックス)→『できる』or『できない』の2択で簡単にできる
- FIM(機能的自立度評価表(Functional Independence Measure))→項目が多く選択肢が微妙で再現性低い
脳血管性認知症VD
VD診断基準
認知症の発現が脳血管障害(脳出血、脳梗塞)後3カ月以内に発症する
障害を起こしやすい血管は決まっている→VD典型例がある

Lewy小体型認知症、Lewy小体病 Dementia with Lewy Body(DLB)
男女比2:1で男性に多い
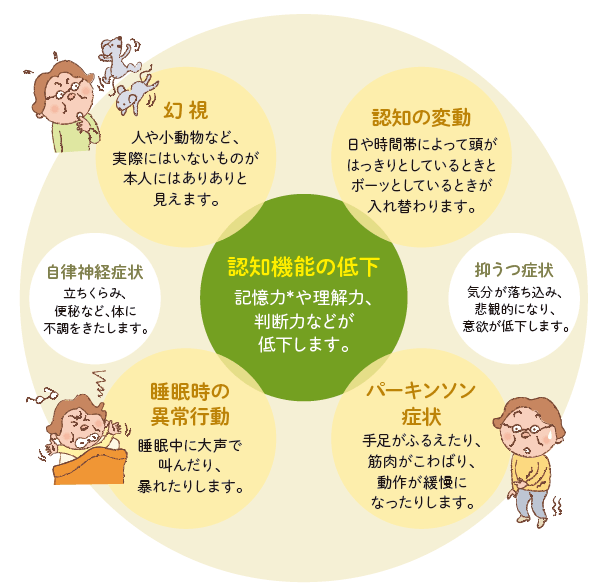
診断のためには4つの中核症状を探しに行く(=幻視、RBD、パーキンソニズム、認知機能の変動)
DLB薬物治療のポイント
医療保険の適応があるのはドネペジルであるが、リバスチグミンも効果が期待できる(保険適応なし)
シロスタゾールも効果的 (保険適応なし)
抑肝散が効果的で、幻視を改善させることもある
体が動かしにくいなどのパーキンソン症状にはレボドパ製剤を少量使用する
向精神薬などに過敏性を示すことがあり、過鎮静、意識障害、 転倒、誤嚥などの副作用を生じやすい
DLBに保険適応で使用できるChE阻害薬はドネペジルのみ(他2剤は保険適応外)
2018年7月、レビー小体型認知症に伴うパーキンソニズム(レボドパ含有製剤を使用してもパーキンソニズムが残存する場合)に対してゾニサミド(トレリーフ®、1日1回25㎎)が適応を取得した
DLB診断基準

- レビー小体は脳だけでなく、全身に張り巡らされた神経にも蓄積する。どこの部位に多くできるかによって症状が異なるため、別の病気と思われやすいが、「レビー小体病」として総称されている。
- 症状のあらわれ方にも個人差があるため、パーキンソン病やうつ病、アルツハイマー型認知症など他の病気と思われやすく、症状だけでは判断が難しい
- レビー小体型認知症では脳のドパミン神経が破壊される。ドパミン神経細胞は脳が全身の筋肉に運動の命令を出すのに必要な神経伝達物質ドパミンを作る神経細胞で、ドパミン神経細胞が壊れるとドパミン量が減って体がうまく動かせなくなりパーキンソン症状が出現する。
- 症状の特徴:
- 認知機能の特徴
- HDS-Rで遅延再生が保たれる(ADでは遅延再生が障害されやすい)
- 認知機能低下以外の症状から始まることもある→DLBと診断困難
- 症状の日内変動
物分かりがよく意識がはっきりしている時と、反応が乏しくぼんやりとしている時がある
- 幻覚
- 幻視・錯視
ヒトや虫などが見える、幻覚だと言っても修正できないため共感するほかない - 妄想・異常行動
- 幻視・錯視
- 自律神経症状
- 排尿障害→頻尿、尿意切迫、尿失禁
- 起立性低血圧
- 便秘
- レム睡眠行動異常症
- パーキンソン症状→DLBの診断に必須ではない、DLBの30%では陰性
- 動作緩慢・筋強剛・姿勢反射障害
- DLB のパーキンソニズムは,PDD と比較して静止時振戦や左右差が少ない
※PDの振戦は安静時振戦、本態性振戦は両手が動作時に震える、企図振戦は小脳の障害(=指鼻指試験で目標付近で震えが強まる) - 転倒を繰り返す
- 認知機能の特徴
- 診断:
- MRIやCT、SPECT検査を行う
- 鑑別疾患:
- パーキンソン病(PD)
- 認知症を伴うパーキンソン病(PD with dementia:PDD)
認知症がパーキンソニズムに先行した場合DLB, パーキンソニズムが認知症に 1 年以上先行した場合 PDD とする指摘もある.しかし,DLB と PDD の間に本質的な違いがあるという証拠はない

- 治療:
- △ドネペジル
- メマンチンや抗精神病薬に対する過敏な反応が出やすいのでドネペジルの投与を優先する
- 唯一の保険適応薬
- 極少量(0.5mg~0.75mg、細粒を使用する)から開始する→その量で維持できることが多い
- ◎リバスチグミン:
- 保険外使用になるがリバスチグミンはレビー小体型認知症には極めて有効であり、せん妄にも効果的
- 2.25mg(最少用量4.5mgパッチを1/2に切って貼布)~4.5mgで効果的
- ガランタミン:
- 保険外使用になる
- 海外ではDLBの認知機能改善効果が示されている
- ○抑肝散:
- 幻視や妄想がみられるレビー小体型認知症の人に使用される事が多い
- 認知の変動やレム睡眠行動障害に対しても効きめも現すことがある
- 抗精神薬による精神症状のコントロール
- 抗パーキンソン病薬による運動症状の改善
- 自律神経障害に対しての血圧コントロールなど
- レビー小体型認知症の患者さんでは抗精神薬への反応が過敏である事があり、少量より時間をかけて様子をみながら薬の内容を検討する事が必要
- 向精神薬は運動症状を悪化させる作用があるものが多く、逆に抗パーキンソン病薬は精神症状を増悪させる事があるため、薬剤調節は難しい場合もあり、個々の患者さんの生活や介護がしやすいように薬をうまく考える必要があります。
- アルツハイマー型認知症の治療薬が効果的な場合もあり、試みられることもあります。
- △ドネペジル
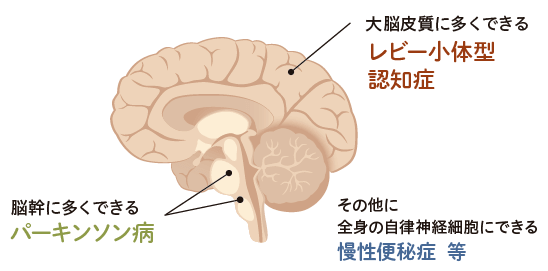
パーキンソン病とレビー小体型認知症はどちらも、レビー小体という脳の神経細胞に何らかの影響を与える構造物が出現する、 レビー小体病の一連の病態の一つということが最近証明された(2022年9月Nature誌)。さらに多系統萎縮症:MSA(オリゴデンドロサイトに豊富な繊維状 α-シヌクレイン封入体が存在する)も3 番目の主要なシヌクレイノパチーと考えられている。
レビー小体は主にα-シヌクレインというタンパク質が集まった凝集体であるが、まだ解明されていない部分も大きく、シヌクレイノパチーには根本治療が確立されていない。
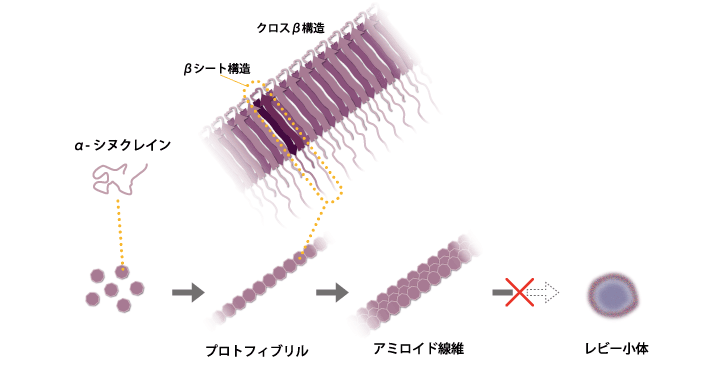
http://www.spring8.or.jp/ja/news_publications/research_highlights/no_87/
レビー小体のみられる範囲が脳幹か脳全体かによって鑑別されるが、生前に鑑別することはできない。パーキンソン病の方はそうでない方に比べ4~6倍の頻度で認知症をきたしやすく、 パーキンソン病の方の約3割、発症から10年以上経過した方では約7割に認知症がみられます。 パーキンソン病発症から1年以上経過後に認知症を発症した場合を認知症を伴うパーキンソン病、 それ以前に認知症を発症していた場合をレビー小体型認知症と呼び、別の病態として扱っている。
アルツハイマー病における脳損傷の主な原因は神経原線維変化と老人斑であると考えられているが、アルツハイマー病の人にレビー小体が発生することもある。 アルツハイマー病に典型的な神経原線維変化と老人斑が、レビー小体型認知症の患者に発生することもある。レビー小体型認知症、パーキンソン病認知症、アルツハイマー病の病態にはかなり重複する部分があり、これら3つの病気の関係を明らかにするためのさらなる研究が待たれる。

多系統萎縮症MSA
初発から病初期の症候が小脳性運動失調であるものはオリーブ橋小脳萎縮症(olivopontocerebellar atrophy:OPCA)、パーキンソニズムであるものは線条体黒質変性症、そして特に起立性低血圧など自律神経障害の顕著であるものはシャイ・ドレーガー症候群と各々の原著に従い称されてきた。いずれも進行するとこれら三大症候は重複してくること、画像診断でも脳幹と小脳の萎縮や線条体の異常等の所見が認められ、かつ組織病理も共通していることから多系統萎縮症と総称されるようになった。
向精神薬とは、中枢神経に作用し精神機能に影響を及ぼす薬物の総称
抗うつ薬(主にうつ病の治療薬)、抗精神病薬(主に統合失調症の治療薬)、抗不安薬(主に神経症の治療薬)、睡眠薬(主に不眠症の治療薬)などが含まれる
前頭側頭葉型認知症 FTD
全認知症患者の1%程度と少ないが、治療・介護抵抗性が高い
感情の麻痺、脱抑制、常同行動不穏・興奮症状の発現頻度はFTD(65%) > DLB(50%) > VD (40%) > AD(25%)(1施設のデータ)
- 認知症には「中核症状」と「行動・心理症状(BPSD)」という、大きく分けると2つの症状がある
- 中核症状によって引き起こされる二次的な症状のこと
- 中核症状が現れることによって、精神的に落ち込んだり、できないことに焦りを感じたり、不安になったり……このような性格や心理状況が原因となって起きる症状が行動・心理症状
- 例えば、「怒りっぽくなる」「妄想がある」「意欲がなくなり元気がない」「一人でウロウロと歩き回る」「興奮したり、暴言や暴力が見られる」などの症状
- 大切なのは、「行動・心理症状の方の混乱や不安の原因を理解すること」
- 治療には、非薬物療法を優先する
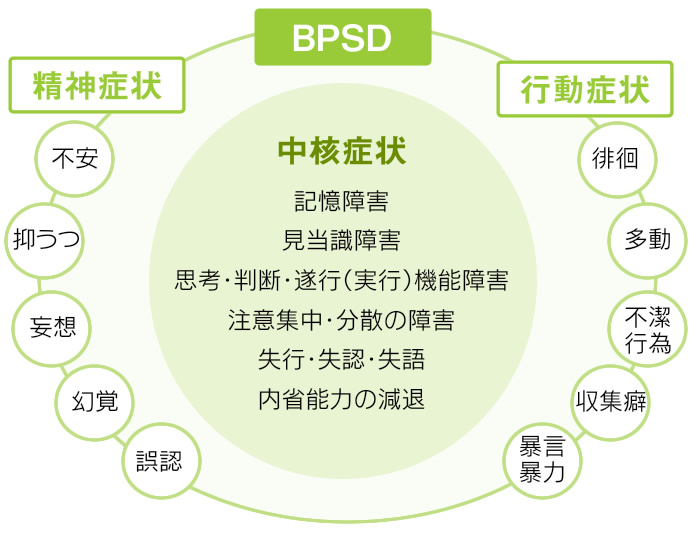
FTD診断基準

- 診断基準
物忘れ外来
- 物忘れ(記憶障害)は認知症の最も基本的な症状の一つ
- 認知症は誰にでも訪れる可能性があり、「一生ならない」ことよりも、いかに「なる時期を遅らせられるか」が重要
- 認知症は、体験したこと自体を忘れてしまったり、日常生活に支障が出たりすることがポイント
- 認知症は、70代前半では3%台、80代後半の40%、90歳以上では60%を超えるとされ、歳を重ねるごとにリスクが高まる
- 物忘れ外来では、その人の物忘れが、自然な老化によるものなのか、病的なものなのかを診断し、その症状に応じた適切な治療を行います。 早期診断、早期治療により、患者さまとそのご家族さまが一日も早くを穏やかな生活を取り戻せることを第一に心掛けます。
- 診断:問診、神経心理検査(HDS-R(長谷川式簡易認知機能スケール)や、MMSE(ミニメンタルステート検査))、CT、MRI、SPECT(脳の血流や代謝を調べる)、PET
- 治療
- アンチエイジング的には・・・
- 新しいことを覚えることが苦手になる
- 食事をしたことは覚えているが、何を食べたか思い出せない
- 人の名前がすぐに出てこないが、ヒントがあれば思い出せる
- 今まで通りの暮らしができている
- 正常な加齢反応ではなく、病気によって脳の神経細胞が損なわれたり脳の機能が低下したりする状態
- 食事をしたこと自体を覚えていない
- 知っているはずの人の名前を聞いても思い出せない
- 認知機能の低下により今まで通りの暮らしができなくなっている
- 認知症ではないけれど、以前に比べ認知機能が低下してきている状態を軽度認知障害(MCI:Mild Cognitive Impairment)という
- MCIの原因として最も多いと考えられているのは、「アルツハイマー病によるMCI」
軽度認知障害(MCI:Mild Cognitive Impairment)
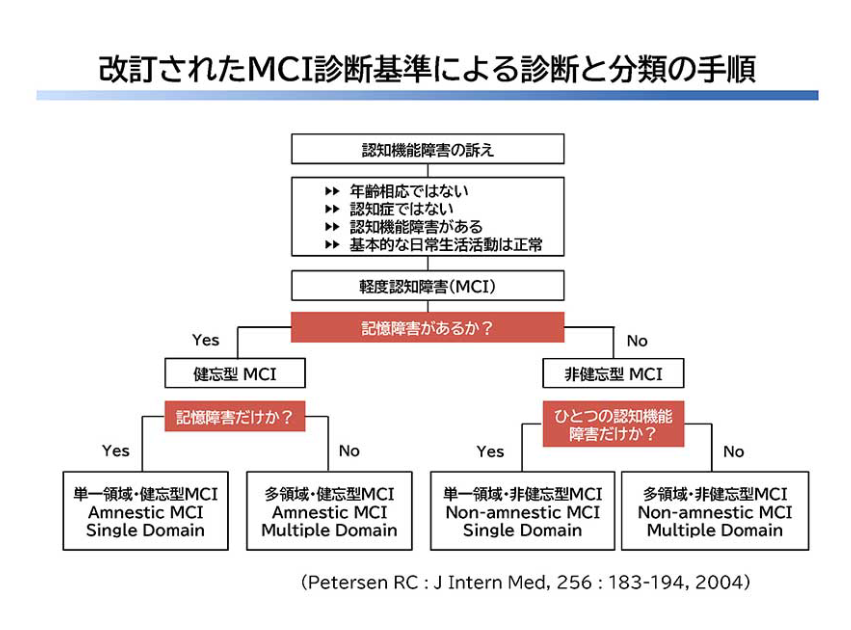
シロスタゾールによるMCIの進行予防はnegative studyだった。
副作用が多いので散剤を使い25㎎×2から使いこなすとよい。
頭痛を認める場合には高い確率で効果がある。
ただしシロスタゾールのジェネリック品では効果が得られないので注意を要する。
認知症治療を成功させるには各薬剤の特性を知ることが必要であり、患者に合った薬剤を選択した上で患者をよく観察し、投与量には細心の注意を払い、副作用を出すことなく治療することが大事である。
そして抗認知症薬のパフォーマンスを最大限に引き出せれば、治療成績は必ず上がる。
- 認知症ではないけれど、以前に比べ認知機能が低下してきている状態を軽度認知障害(MCI:Mild Cognitive Impairment)という
- 2012年の時点でMCIの高齢者は約400万人と報告されている
- アルツハイマー病によるMCIとアルツハイマー型認知症の違いは、自立して日常生活を送れるかどうかという点
- MCIの原因によっては現状が保たれたり、回復したりすることもあるため、MCIの方が必ず認知症になるわけではない。1年で5~15%の人が認知症に移行するとされる一方、1年で16~41%の人が健康な状態に戻ったとする報告もある。
- アルツハイマー型MCIでは、アルツハイマー型認知症と同様に脳内にアミロイドβの蓄積が認められる
- MCIの段階で早期発見して予防策を講じることで認知症への進行を遅らせることが重要である

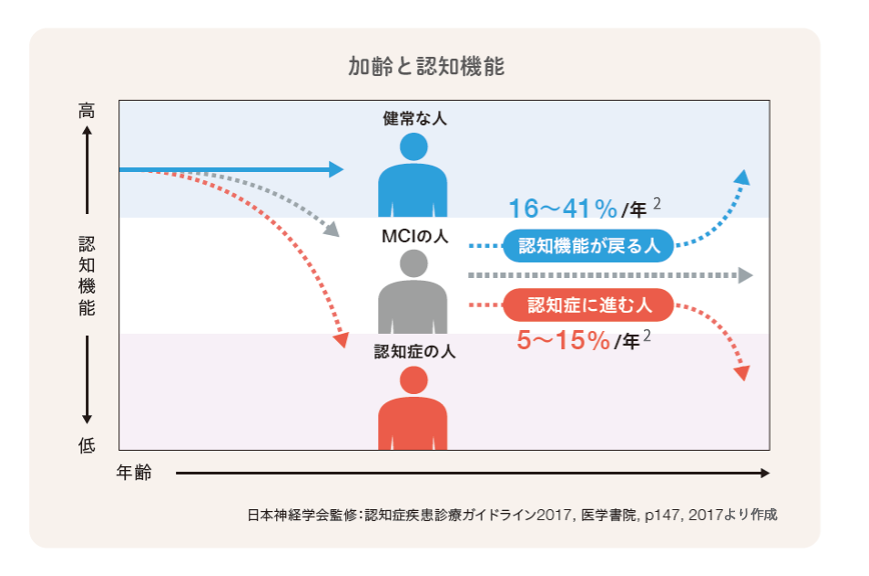
若年性認知症
- 認知症は、一般的には高齢者に多い病気だが、65歳未満で発症した場合、「若年性認知症」とされる
- 弱年性認知症は男性にやや多い(高齢者の認知症は女性に多い)
- 認知症は一つの病名ではなく、認知症を起こす原因疾患はさまざまで、多くの場合は脳の病気でありしかも進行性
- 若年性アルツハイマー型認知症が最も多く血管性認知症、前頭側頭型認知症、外傷による認知症、レビー小体型認知症/パーキンソン病による認知症が続く
- 若年性認知症は働き盛りの世代で発症するため、ご本人だけでなく、ご家族の生活への影響が大きくなりやすい特徴があります。
認知機能低下・認知症の実臨床
認知症診療の目標
『暮らしの障害』である認知症を持ちながらも、できるだけ満足のいく人生を送れるようにサポートすること
アルツハイマー病、DLB→ドネペジル試してもよい(脳血管性認知症には適応なし)
ドネペジルが無効/副作用で不耐の場合は薬剤変更または中止
認知症が進行し、意思疎通困難となった場合も即時中止する

認知症治療の効果判定基準

- 認知症患者の「良い状態」を表すサインで治療効果判定を行う
- 認知症ケアの理念の1つである「パーソン・センタード・ケア」(認知症患者を1人の人として尊重し、患者の立場に立って理解し、ともにケアに取り組む)の提唱者トム・キッドウッドがまとめたもの
- 本人の幸福度を評価するのと同時に、家族・介護者の視点も忘れてはいけない
BPSD治療総論

認知症の人は、「理性の世界」から「感情の世界」に移った人
→「優しい人だ」「ここは安心して暮らせる場所だ」と認知症の人が思えるような対応することが重要
BPSDの薬物治療は不確実性が高いということを理解してもらう
暴言・暴力は BPSD の中でも最も対応困難な症状
BPSD は認知症患者のおよそ 8 割に認められ,患者の苦痛はもちろんのこと,家族の心理・身体・社会的負担が大きく,そのため患者が施設に入所する主な原因の一つ
→非薬物療法としては安心させることが重要、ユマニチュード、バリデーション(否定せず聞く)など
①ほめる、感謝する
②同情(相づちをうつ)
③共感
④謝る、事実でなくても認める、上手に演技をする、嘘をつく
脳血管性認知症や、アルツハイマー病、DLBなどの病型によっても対処法が異なる
かかりつけ医のためのBPSDに対応する向精神薬使用ガイドライン第2版(厚労省)
→https://www.mhlw.go.jp/file/06-Seisakujouhou-12300000-Roukenkyoku/0000140619.pdf
http://tcm-kampo.com/crayondb/upload/TUtlXvxcFm6aXE8SIfzZFemi6um4ap.pdfも参照
https://www.jstage.jst.go.jp/article/jjghp/23/1/23_19/_pdf「BPSD薬物療法」も参照

BPSD非薬物治療の基本
すべての「不穏・興奮症状」に医学的介入が必要なわけではない
「不穏・興奮症状」の理由を明らかにし、適切な社会的・環境的・行動的介入を行い誘因を解消する
不穏・興奮症状になる[時間、人、その他]を注意して見ていく必要がある
不穏・興奮症状になる[時間、人、その他]とは?
[時間]
一日のうち、短時間のみ「不穏・興奮症状」を認めるのか?
ほぼ一日を通して「不穏・興奮症状」を認めているのか?
短時間の場合には、特定の時間や環境はないかを確認する必要があります。
日単位や2週間周期で「不穏・興奮症状」の増悪・軽快を認める場合もあります。
[人]
「不穏・興奮症状」を認める場合に、特定の人が周りにいないかを確認する必要があります。
仲の悪い、嫌いな人だけが誘因になるわけではなく、仲の良い、好きな人が誘因となることもあります。
また特定の人が居なくなった場合でも「不穏・興奮症状」を認めることもあります。
特に介護施設では、家族の面会後に「不穏・興奮症状」を認めることが多いです。
[その他]
日単位で変動する「不穏・興奮症状」の場合は、排便状況を確認する必要があります。
便秘を引き金に増悪することが多く認められます。
2週間程度の周期で増悪・軽快する場合には、レビー小体病(パーキンソン病、レビー小体型認知症)の合併を念頭に置き、パーキンソン病運動症状の有無を確認する必要があります。
視力、聴力など感覚の低下により「不穏・興奮症状」の増悪を認めることがありますので、感覚器の評価を行う必要があります。
- 介護的ケアでは
- 「安心させる穏やかな口調で話をする」「目的をわかりやすく語りかけ患者を驚かせない」など認知症患者全般にいえる対応が必要
- 誘因となっている状況や人から、患者を引き離すことが必要
- 特に介護施設入所直後は、家族の面会後に不穏・興奮症状が増悪することが多いので、家族の面会を控えて貰うことも必要
- 便秘を誘因としている場合には、排便コントロールが必要
BPSDに対する薬物療法
薬物療法(向精神薬)は長期予後不良という試験結果があるが、日常のQOLが優先される場合には使用せざるを得ない
ただし、6か月以上の長期投与はなるべく避けるべき→6か月ごとに減量や中止を検討してもよいだろう
BPSDに対する薬物療法ガイドライン

認知症診療ガイドライン2017


不安に対する治療

不安は,BPSD の原因や誘因になりうる重要な症状である.まずは安心させる声かけや態度で接することが基本
焦燥性興奮に対する治療

幻覚・妄想に対する治療

うつ症状に対する治療

徘徊等に対する治療

睡眠障害に対する治療

睡眠薬の適正な使⽤と休薬のための診療ガイドライン2022
BPSD薬物治療の実臨床
⓪BPSDをきたしうる薬剤を整理し、不要な薬剤は中止し、できるだけ薬剤数を減らす
①激しい精神症状(過覚醒の精神症状)の場合→抗精神病薬のみで治療を行い、抗認知症薬は併用しない
➁穏やかな周辺症状(低覚醒の精神症状)の場合→まず抗認知症薬(ガランタミンが推奨)で治療を開始
BPSDに対する抗精神病薬
脳血管性→グラマリール±抗てんかん薬
それ以外→レキサルティーが第一選択(米国では保険適応あり、副作用が少ない!)
オラ・クエはDM禁忌!!
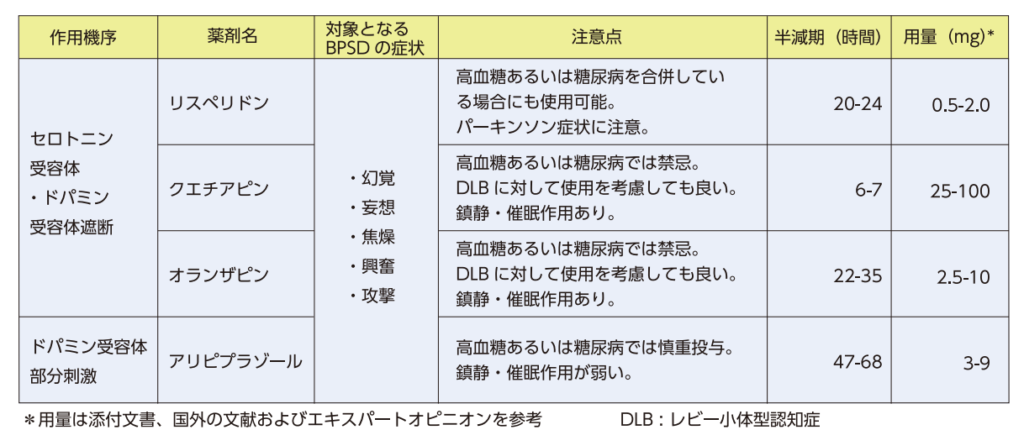

グラマリール(チアプリド)
リスペリドン0.5g=チアプリド50mg
半減期3.9時間→分3内服が必要、常時家族がいる人か施設入所者でないと内服できない
病態別BPSDの特徴と薬物療法
- 血管性認知症:
- メマンチンは使用できない(アルツハイマー病のみ)
- 怒ったり手をあげたりする言動が突然出現する→情動を発生させコントロールする脳神経細胞が障害されている
→抗痙攣剤が有効- カルバマゼピン(テグレトール)
- パルブロ酸ナトリウム(デパケン、セレニカ、バレリン等)
- ◎チアプリド(グラマリール)
- 脳梗塞後遺症に伴う攻撃的行為、精神興奮、徘徊、せん妄の改善に適応を有する
- 通常は3~6錠分3で使用するが、高齢者では2T分2から開始する
- アルツハイマー型認知症:
- 経過に伴い易怒性や暴言、興奮、不穏などの活発な周辺症状が出現あるいは増悪する
- 易怒性や暴言に対しての薬剤選択:
- アリセプト(ドネペジル):
- 副作用として不穏・興奮症状を認める場合にはアリセプトは減量・中止する
- ◎メマリー(メマンチン):
- メマンチンはNMDA受容体チャネル阻害作用により、その機能異常を抑制する
- メマリー(メマンチン)は本邦では重症例に対してアリセプトもしくはレミニール、イクセロン・リバスタッチ(リバスチグミン)と併用することが原則
- 1週間ごとに5㎎→10㎎→15㎎→20㎎で維持(10㎎で効果出る人は10㎎で維持してもよいが、認知機能の長期予後に関する臨床試験ではいずれも20㎎で維持した場合のデータであり、10㎎で維持は標準的ではないかもしれない、保険の査定対象となる恐れあり)
→1日1回5mgからの漸増投与は、副作用の発現を抑える目的であるので、維持量まで増量することと明記されている - 高度の腎機能障害(CCr:30mL/min未満)のある患者には、患者の状態を観察しながら慎重に投与し、維持量は1日1回10mgとすること
- Y先生はドネペジル無効例にメマリー10㎎単剤を投与していた
- メマリー無効の場合:
- グラマリール追加→混合型認知症
- 抗てんかん薬
- 一日のうち短時間だけ不穏・興奮症状を認める場合には、気分安定薬(抗てんかん薬)投与を第一選択
- 認知症疾患治療ガイドライン2010→テグレトール(カルバマゼピン)、デパケン(バルプロ酸)が有効
- テグレトール(カルバマゼピン)
- ◎デパケン(バルプロ酸)
副作用の面から,臨床場面ではバルプロ酸(デパケン,セレニカ)が用いられることが多い
バルプロ酸100 〜 200 mg の低用量でも,易刺激性,興奮,攻撃性,不眠などの症状に効果を認めた - エクセグラン(ゾニサミド)も、発作的な「不穏・興奮」に関して有効
- 抗精神病薬
- ほぼ一日を通して「不穏・興奮症状」を認めている場合には、抗精神病薬を使用する
- 最後の手段として使用する(易怒性や暴言などが我慢ができないほど重症の場合)
- 錐体外路徴候(薬剤性パーキンソニズム)や嚥下障害など多くの有害事象が見られる
- 適応外使用が認められている4種類、それ以外にもオランザピン、アリピプラゾールなどから選択
- ×定型抗精神病薬→BPSDには原則使用しない
- セレネース(ハロペリドール)
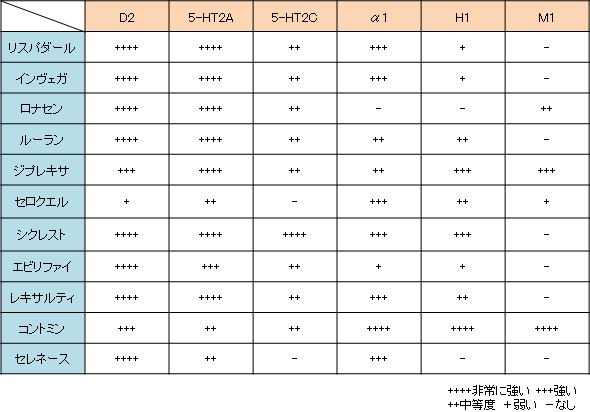
- ◎非定型抗精神病薬
- ルーラン(ペロスピロン):
夜間せん妄には4㎎眠前
常用量:成人1回4mg1日3回より始め、維持量として1日12〜48mgを3回に分けて食後経口投与
作用時間、力価ともにリスパダールよりマイルド
腎不全・透析患者のせん妄の第一選択
DMでも使用可能 - リスパダール(リスペリドン):
興奮が特に強いときに選択、0.5㎎から開始、過鎮静に注意
0.5mgを夕食後あるいは就寝前1回の服薬から開始し、1~2週後の状態を観察し効果不十分と判断するときには1mgに増量
易怒性から興奮、さらに暴力行為が逼迫する際の早急な鎮静には、リスペリドンかオランザピンを用いる
腎不全、透析患者にはルーラン(ペロスピロン)を使用する - セロクエル(クエチアピン):
強い鎮静作用があるが、抗幻覚妄想作用は弱い
半減期が短く眠剤としても使いやすい
糖尿病禁忌
錐体外路症状が比較的現れにくく,DLB に対しても用いられることがある
開始量は 6.25~12.5mg分1夕または眠前であり,75 〜 100 mg 程度を目安とする
75mgから100mgまで増量しても効果が発現しないときには、クエチアピン無効と判断する - ジプレキサ(オランザピン):
強い鎮静作用と強い抗幻覚妄想作用を併せ持つ→1日中、強いせん妄状態に使用する
半減期が22時間と長く、内服すると確実に翌日まで持ち越す
オランザピンの開始量は 1.25 〜 2.5 mg/ 日で 5 mg を超えると副作用が現れやすくなる - ◎レキサルティー(ブレクスピプラゾール):大塚製薬
ADのBPSDに世界初の保険適応を取得した抗精神病薬(日本でも効能申請中2023年10月)
高齢者にも安全に使用できる
0.5㎎錠剤を半錠(0.25㎎)くらいから始める方がよいだろう(統合失調症の極量はわずか4㎎) - エビリファイ(アリピプラゾール):
幻覚・妄想に効果があるが、鎮静作用は非常に弱い
副作用は比較的多い、他剤(抑肝散、メマンチン、クエチアピンなど)無効例に処方するイメージ
副作用観察と血中濃度安定するまで(2週間程度)は最小投与量(散剤で0.5~1㎎)で維持する
統合失調症治療では1日6〜12mgを開始用量、1日6〜24mgを維持用量、分1~2で投与
注意すべき副作用
CK上昇 、 振戦 、 傾眠 、 ALT上昇 、 不眠 、 神経過敏 、 不安 、 アカシジア 、 流涎 、 体重増加
- ルーラン(ペロスピロン):
- アリセプト(ドネペジル):
- レビー小体型認知症(DLB)
- DLBは、幻覚、妄想、興奮、うつ、レム期睡眠行動異常症など多彩な BPSD がみられるが、抗精神病薬に対する過敏性を認めることがあり、少量の抗精神病薬でも重篤な副作用が見られる場合があるため、特に注意が必要である
- 抗精神病薬を使用する場合は、オランザピンかクエチアピンを選択する
- ドネペジルはDLBにも使用可能だがDLBのBPSDに対して有効性は証明されていない
- せん妄予防:
- トラゾドン
- オレキシン受容体拮抗薬(デエビゴ、ベルソムラ)
覚醒を促す脳内物質のオレキシンが受容体と結合するのを阻害して、睡眠を促す
ベルソムラで脳脊髄液中のアミロイドβやタウのリン酸化レベルが低下する→アルツハイマー病の予防に有用である可能性を示唆する予備的な臨床試験の結果がでた→「Annals of Neurology」に2023年3月10日掲載 - メラトニン受容体アゴニスト(ロゼレム)
メラトニンのせん妄予防投与が注目される
併用注意が多いため、処方の際は慎重に!!! - https://seiwakai-shimane.com/blog/?page_id=779
- BPSDに対する漢方薬:
- 抑肝散
- いずれの認知症(AD、脳血管性認知症、DLB)にも効果的
- 抗コリン作用や錐体外路系の副作用を認めず、認知機能への影響がみられないことから認知症高齢者に対しても比較的安全
- 甘草が含まれるため低K血症の副作用あり→高齢者では5gから開始するとよい
- 抑肝散の効果は投与後 1 ~ 2 週間の早期に現れ、4 週間経過をみても効果がみられない場合,他の選択肢を考慮すべきである
- 抑肝散加陳皮半夏
- 抑肝散に陳皮と半夏が加味された漢方薬
- 標的症状は抑肝散と同じだが、より体力が低下した患者に用いられる
- 腹直筋に緊張を認める場合、抑肝散の効果が得られやすいと言われる
- 腹力が軟弱で腹直筋の緊張を認めず、大動脈の拍動をふれた場合、抑肝散加陳皮半夏の効果が得られやすい
- 黄連解毒湯
- 比較的体力があり、のぼせぎみで顔色が赤く、いらいらする傾向のあるひとに適した漢方薬で、効能効果は鼻出血、高血圧、不眠症、ノイローゼ、胃炎、二日酔、めまい、動悸、湿疹・皮膚炎、皮膚掻痒症など多岐にわたる。
- この漢方薬は脳血管障害の易怒性、不機嫌、不穏、興奮などの BPSD に効果が報告されている
- 副作用として、ときに発疹、消化器症状、肝障害がみられることがある
- 基礎研究では釣藤散、黄連解毒湯の脳虚血に対する保護作用が示されている
- 釣藤散(チョウトウサン)
- 釣藤散は、中年期以降、慢性に続く頭重または、高血圧の傾向のある虚証のひとに対する漢方薬である
- 139 例の血管性認知症を対象とした 12 週投与の結果、幻覚・妄想、不眠、せん妄に対する効果を認めた
- 抑肝散


頻用薬・処方カスケード、相互作用、注意事項→抗精神病薬を参照
アルツハイマー型認知症と血管性認知症の鑑別は可能か
認知症以外に麻痺や構音障害などの巣症状があれば脳血管性認知症を第一に考える。
認知症以外に能力低下を認めなければアルツハイマー病を第一に考える。
脳梗塞発症以前から認知機能低下を認めた場合は、アルツハイマー病を考える。
アルツハイマー型認知症の40%で脳血管病変の合併がみられ、血管性認知症の40%で剖検にてアルツハイマー病変を認めることが報告されています。両者は近縁の病態を示すことが近年強調されてきています。認知症に片麻痺などの運動障害がみられるとき、血管性認知症と診断しがちですが、脳SPECT検査を施行するとアルツハイマー型認知症に特徴的な血流低下を合併する事例もしばしば経験します。アルツハイマー型認知症を合併しているならばドネペジル(アリセプト®)の投与も可能となってくるので、血管性認知症と診断した患者さんでも脳SPECT検査を合わせて施行し、アルツハイマー病変の合併の有無を確認するほうがよい。
易怒性、暴言、暴力などのBPSD
BPSDに対する薬物治療の基本方針
⓪AD、DLB→メマンチンorチアプリド
脳血管性認知症→チアプリド(グラマリール)
から試す
混合性認知症→メマンチン+チアプリドの処方も可能
①BPSDに対して定型抗精神病薬を使用しないのが原則
定型抗精神病薬の BPSD に対する効果は非定型抗精神病薬と大きな違いはなく、副作用の発現がより多い
➁BPSD に非定型抗精神病薬を使用する場合
処方はじめはごく少量から開始し、1~2週間ごとに増量していく
変更する場合は1種類ずつ行う(副作用が出現した場合の因果関係がわかるようにするため)
とくに転倒、誤嚥に注意を要する
高用量や長期使用は副作用のリスクを高める→必要最低用量、かつできる限り短期間の使用に留める
家族が我慢できる程度に標的症状の軽減が図れたときには、3カ月を目安に減量から中止するのが理想的→中止の際には屯用で持たせても良い
③薬物療法の開始時における患者や家族・介護者への説明
BPSDの治療は不確実性が高く、すぐに成果が出るわけではないことを家族・介護者にきちんと説明し、今後の見通しや治療の方針を伝える
→家族・介護者は心構えができ、納得感や安心感が得られる
「期待される治療効果とその時期、そして治療の限界」
「起こりうる副作用」
「注意して経過観察すべき点」
「副作用を認めた場合の対処法」
「薬剤が有効でなかった場合の次の一手(精神科紹介も含む)」
1日中強い幻覚妄想興奮→DMなしならオランザピン
1日中強い幻覚妄想興奮→DMありならリスペリドン、アリピプラゾール
夜間の不眠・徘徊→クエチアピン、トラゾドン、テトラミド
幻覚妄想は強いが鎮静はなるべくしたくない→アリピプラゾール
脳血管性認知症の陽性症状→チアプリド(保険適応あり)
DLBの陽性症状→メマンチン、クエチアピンまたはオランザピン
アパシー、うつなどのBPSD
アパシー=やる気がなくなり活動性が低下した状態
→認知症の初期症状のこともある
まずは抗コリン薬、無効の場合は抗うつ薬に切り替えまたは上乗せする
気分をあげる効果としてはSNRI>SSRI(SNRIはノルアドレナリンの濃度も上昇させる)
- AD のうつに対してドネペジル(アリセプト)の効果が報告されている
- 大うつ病エピソードを満たす重度のうつ状態に対しては抗うつ薬が必要となる
→三環系抗うつ薬は抗コリン作用が強いため使用は控え,SSRI やSNRIを最低量から使用する
ミルナシプラン(トレドミンⓇ)
セルトラリン(ジェイゾロフトⓇ) - アパシーに対しても塩酸ドネペジルの効果が報告されている
- アパシーに対して抗うつ薬は無効の場合が多く,ドパミン伝達系を賦活する塩酸アマンタジン(シンメトレルⓇ),ペルゴリド(ビ・シフロールⓇ)などが有効な場合があるが、DLB では,ドパミン作動薬で幻覚,妄想症状が悪化することもあるため注意が必要である
ギリシャ語の a=失う、pathos=感情・苦悩を組み 合わせた言葉。
アパシーとは感情や苦悩を失ってしまうという状態を指す症状。
当然、喜びや楽しいと感じる心地よさ、美しいと感激する気持ちなども消えてしまう。
はたから見ていると、「何もしない」不活発な状態で、日がな一日、同じ姿勢でぼんやりとしている状態。
本人の主観では、「何もする気にならならい」 「つらいこともないし、何とも思わないから、このままでいい」というような状態になり、認知症の初期、脳卒中や頭部外傷の後遺症、パ ーキンソン病とその近縁疾患、甲状腺機能障害などのホルモン異常、薬剤の副 作用などでおきることが知られている。
どちらも「何もしない」不活発な状態に見えるが実は内面的には全く正反対である。
アパシーは内面的には「苦痛、悩みがない」「無関心」→本人的には困っていない。
うつ病は「苦痛、悩みが強い」、無関心どころか「あれこれ気にして考えあぐねる」があり、苦痛を伴う。
アパシーの特徴は「本人は困らない」が「周りが困る」ことが多い
うつ病は「本人も周りも苦しんで困る」
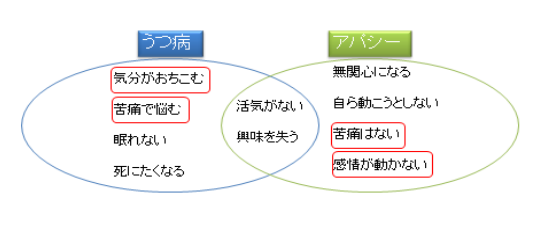
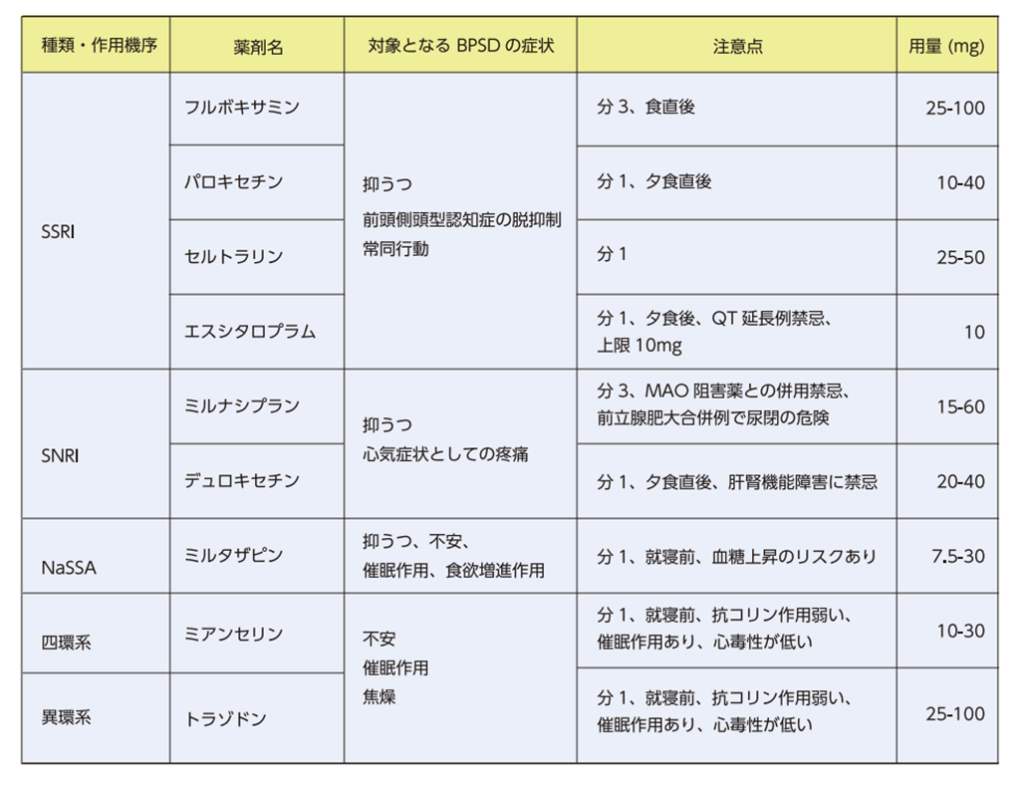
抗うつ薬
幻覚・妄想などのBPSD
- 症状が強く本人の苦痛が強い場合,少量の非定型抗精神病薬が用いられることがある
- 幻視を中心とした DLB の幻覚に対しては,ドネペジルが有効な場合が多い
- ドネペジルに無効の幻覚に対しては,抑肝散の効果が報告されている
- 程度が激しく興奮を伴う妄想(物とられ妄想など)に対しては,非定型抗精神病薬が必要となる場合がありAD の物盗られ妄想にリスペリドン(平均 1.1 mg/ 日)の効果が報告されている
- DLB の妄想はドネペジルや抑肝散の効果が認められている
ドネペジルはうつ,アパシー,不安,DLB の幻覚,妄想など BPSDのいくつかの症状に対して効果があるため,BPSD に対して新たに薬剤を追加する前にドネペジルの効果を評価する

末期認知症の緩和治療
肺炎・呼吸苦に対する緩和治療
オピオイドで呼吸困難が改善する COPD 患者の 70%が 10 mg/ 日以下(経口モルヒネ換算)の少量のモルヒネで改善しているとし、非がん性呼吸器疾患の呼吸困難に対するオピオイドの初期投与量は、屯用の場合 経口モルヒネ 2.5㎎、徐放剤では 10mg/ 日から開始すること、注射の場合は複数の(弱 い)エビデンスを挙げた上でモルヒネ注射剤持続注射 0.25mg/ 時以下(6㎎ / 日)から開 始すること、増量については、呼吸困難や副作用を十分評価した上で 1.3 ~ 1.5 倍に増量する
オピオイドの種類は、呼吸困難の緩和にエビデンスのあるモルヒネの使用が推奨される。
モルヒネの開始量は、屯用の場合経口モルヒネ 2.5㎎、徐放剤ではモルヒネ徐放剤 10mg/日から、注射の場合はモルヒネ注射剤の持続注射 0.25mg/ 時(6 ㎎ / 日)以下を基本とし、年齢や体重、腎障害や肝障害の状況により、モルヒネ の投与量を減量したり、ヒドロモルフォンやオキシコドンなどモルヒネ以外のオピオ イドの投与を検討する。 オピオイドの投与経路については、高度の嚥下障害を伴う重度認知症でも少量の水分摂取が可能であればモルヒネ塩酸塩水和物液*の内服が可能である。一方、嚥下反 射が消失し少量の水分の摂取も困難な末期認知症の場合は、モルヒネの皮下注や持続皮下注(continuous subcutaneous infusion:CSI)などの非経口投与が望ましい。
→在宅末期認知症肺炎診療と緩和ケア指針
- 肺炎の呼吸困難へのオピオイドの効果についての系統的レビューの結果、末期認知症に限らず、終末期の肺炎時の呼吸困難に対するオピオイドの有効性を示す質の高い研究は認められなかった。
- 非がん疾患の呼吸困難に対するオピオイドの有効性についてのエビデンスは、COPD において少量のモルヒネの全身投与が呼吸抑制などの副作用を引き起こすことなく呼吸困難を緩和できるという弱いエビデンスがあるが、それ以外の非がん疾患では、心不全や間質性肺疾患、ALS などで呼吸困難の緩和におけるオピオイドの有効性に関して 限定的なエビデンスがあるのみである。
- しかし、海外では末期認知症の肺炎の呼吸困難に対して広くオピオイドが使用されている。例えば、シンガポールでの末期認知症の在宅緩和ケアに関する前向き観察研究 (n=294) でも、疼痛と呼吸困難にオピオイドが用いられ、亡くなる当日には77.6% (228 例 ) にオピオイドが用いられていた。オランダのナーシングホームの前向き観察研究でも、肺炎発症後2週間以内に死亡した例の95%が亡くなる24時間前にモルヒネの投与を受けており、海外では末期認知症の肺炎の呼吸困難の緩和目的でオピオイドが広く使用されているという実態がある。
末期認知症の肺炎時および看取り期の気道クリアランス法(排痰法)
末期認知症の肺炎に伴う喀痰に対しては、標準的な気道クリアランス法(排痰法) の実施が困難となることが多いため、側臥位あるいは前傾側臥位による体位ドレナー ジを頻回に行い、必要に応じて呼吸理学療法を加える。
臨死期でも意識障害を伴わない場合
真性死前喘鳴とは考えず、基本的な気道クリアランス法(排痰法)を継続する。深い吸引は苦痛となるためできるだけ避けるようにし、体位ドレナージで口腔内に移動した痰を浅い吸引や手で拭うようにして排出する。
臨死期で意識障害を伴う場合
真性死前喘鳴として対応し、本人の苦痛はないことを家族に十分説明する。臨死期の死前喘鳴では前傾側臥位による体位ドレナージも困難となることが多く、輸液を中止して分泌物を減らすことが第一選択となる。 死前喘鳴の抗コリン薬の有効性に関するエビンデンスは限られているが、家族ケアの観点から抗コリン薬の投与を検討する。また、在宅医療では抗コリン薬(注射薬)の舌下投与(保険適応外)など治療負担の少ない投与法を検討してもよい。
- 抗コリン薬3剤の死前喘鳴に対する効果は、プラセボを用いた抗コリン薬の全身投与の効果が確かめられていないので、実際のところどれだけ効果があるのかはわかっていません。
- 一方、ハイスコ、ブスコパン、アトロピンの3剤間の比較試験では、アトロピン、ブスコパン、ハイスコも、それぞれの薬剤間ではほとんど差を認めませんでした。
- 投与例:ブスコパン1A、4回皮下注
- ブスコパン半減期は2~4.5時間(蠕動抑制効果は40分)
エビデンスは少ないがイプラトロピウム臭化物水和物吸入(アトロベント®エアゾル)の口腔内噴霧や硫酸アトロピン点眼、 ハイスコ注射薬 0.5A の舌下投与(いずれも適応外使用)などの方法もある。在宅末期認知症肺炎診療と緩和ケア指針より
体位ドレナージ法
早期離床、座位保持、前傾側臥位など
左(前傾)側臥位⇒仰臥位⇒右(前傾)側臥位の順で 1 時間~ 2時間ごとに体位変換を行うとよい。
肺炎の場所が分かっている場合、例えば誤嚥性肺炎で多い右側背側の肺炎の場合は右上の体位を多くとると効果的。
自動体位変換エアマット、マルチポジションベットも効果的。
運転免許の問題

脳循環代謝改善薬→処方してはいけない
脳循環代謝改善薬
脳血管の拡張作用などにより脳循環を改善し、脳梗塞後のめまいや意欲の低下などの諸症状の改善作用をあらわす
サアミオン(ニセルゴリン)
- 脳梗塞後は脳細胞のダメージがあったり、脳の血流が悪くなっている状態で、脳からの適切な指令が伝わりにくくなり、めまいや意欲の低下などの症状がおこる場合がある
- 脳血管を広げ血流をよくすることで脳循環を改善し脳にエネルギーや酸素が送られ、脳梗塞後の諸症状の改善が期待できる。
- イブジラスト徐放カプセル(ケタス)
- 適応症:脳梗塞後遺症に伴う慢性脳循環障害によるめまいの改善
- 禁忌:頭蓋内出血後止血が完成していないと考えられる患者
- 血管拡張以外の作用に関して
- 血栓の形成や神経の損傷を抑える作用などもある
- 抗アレルギー作用をもち気管支喘息などで使用する場合もある
- ◎ニセルゴリン(サアミオン)
- 既往症:脳梗塞後遺症に伴う慢性脳循環障害による意欲低下の改善
- 禁忌:頭蓋内出血後止血が完成していないと考えられる患者
- 散剤もあり、嚥下能力の低下した患者などへのメリットも考えられる
- 血小板凝集(血液が固まりやすくなる)を抑える作用などもある
- イフェンプロジル酒石酸塩錠(セロクラール)
- 適応症:脳梗塞後遺症、脳出血後遺症に伴うめまいの改善
- 禁忌:頭蓋内出血後止血が完成していないと考えられる患者
- 血小板凝集(血液が固まりやすくなる)を抑える作用などもある

抗認知症薬
抗認知症薬→コリン作動薬なのでとうぜん消化器症状でやすい!!!
食欲低下したら投薬やめるか、別の薬に変更する
日本は抗認知症薬が投与され過ぎている!!!
一人の患者さんに効果を示すためには10人に投与する必要がある(NNT=10)で、12人に投与すると1人に副作用が出現する(NNH=12)と報告されている
→有効例が多いはずもなく、効果がないのに漫然と処方されている症例が多い
副作用が多いことを説明したうえで、継続するか家族とも相談する
以下の副作用が出現した場合は抗認知症薬の中止を検討する
消化器症状、興奮、不眠、不穏、徘徊、不安焦燥の悪化、致死性不整脈(徐脈)、易怒性、攻撃性、幻覚妄想、めまい、抑うつ、錐体外路症状、転倒など
メマンチンのみが行動障害(徘徊、無目的な行動、常同行為など)、攻撃性(焦燥、暴言、暴力)に対して効果があることが示されており、これらの症状が前景に立っている場合(介護に困難を来す場合)には、メマンチンを考慮する
抗認知症薬使用における諸注意
https://www.tyojyu.or.jp/kankoubutsu/gyoseki/ninchisho-yobo-care/h30-5-2.html
- 治療薬の選択基準:
- ChE阻害薬同士の切り替え基準は存在せず(臨床試験がない)、多くは経験による
- 欧米のガイドラインではwashout期間をおかずに切り替えることとなっている
→ChE阻害薬が共通して持つ消化器系副作用の切り替え時の発現を抑える為 - ChE阻害薬の切替えとメマンチンの併用のどちらを優先させるかについてもRCTはない
→理論的にはベストなChE阻害薬とメマンチンの併用が進行抑制の上では望ましい
- 欧米のガイドラインではwashout期間をおかずに切り替えることとなっている
- ChE阻害薬同士の切り替え基準は存在せず(臨床試験がない)、多くは経験による
- 副作用対策:
- ChE阻害薬の消化器症状対策→PPIとナウゼリン(プリンペランはパーキンソニズム起こすので×)
- ドネペジルの下痢→減量もしくは、他のChE阻害薬に変更
- 食欲低下に対してはリバスチグミン貼付剤が有用である
- メマンチンでは、「眠気」、「ふらつき」が出現することが多い
→対策としては、腎機能チェック、夕方投与、緩徐な増量が有用であるとあるが、長時間作用型のため意味ないのでは?
- 処方時の注意:
- 心房細動や重度の徐脈がある場合は、基本的にはChE阻害薬は使用しない
- ChE阻害薬は基本的に肝代謝
- メマンチンは心機能に影響がなく投与可能であるが、腎不全では減量が必要
- 透析中の患者に対しては、何れの薬剤も添付文書には明確に示されていない
- 病態別の抗認知症薬の処方→プライマリケア メジャー診療科編➁参照
- BPSD対策→老年医学・在宅診療参照