腹腔鏡手術
ラパロ総論
セッティングの基本
モニターの位置はカメラと同軸線上
カメラ先端と対象物の距離は10㎝程度
対象臓器とポートが近いと大きな動作となり不適
作業効率が良いのは左右の手が120°となるとき
針は根元から1/3のところを把持する
針と鉗子の角度は90°以上
針を体腔内に入れるときは左手から(持ち替えが1回で済む)
操作性が悪いときは自分の立ち位置を修正するのもポイント
糸結び
- 素人は匍匐前進法
- 初心者は30秒で1結紮
- ロングテールは左手鉗子で持つ
- square knot:両手法はoverwap、持ち替えてoverwrap
片手法はoverwrap→underwrap - slip knot:square knotで1結紮目は緩めに。編み糸が◎。カウンタートラクションで縛りこむ。
- 単結紮は12㎝、連続縫合は20㎝
- 腹腔鏡手術は内ヘルニア多いため、基本的に間隙は閉鎖する
胃癌について(JSESガイドライン2019)
LDG
cStage I の外科的治療の選択肢の一つとしてLADG を推奨する(JCOG0901)
現時点では cStageⅡ以上の胃癌に対して LADG を推奨する根拠は乏しい
- 短期成績では早期癌,進行癌ともに死亡率,合併症率に両群間で差はないというRCTが多い
- 早期胃癌(cStageI)の長期予後→JCOG0912(RCTによる直接比較)にて5年無再発生存率で同等という結果となった
- 進行胃癌(>StageII)についての長期予後→JLSSG0901の結果待ち
- 長期成績を検討した複数のメタアナリシスでは,早期癌,進行癌ともに両群で同等と報告している
- 日常診療では膵液漏が開腹手術よりも増加するという報告もある(NCDではGradeB以上の膵液廔0.8% vs 1.0%)
LTG
JCOG1401 試験において EMR/ESD の対象とならない cStageIA/IB (T1N0, T1N1, T2N0:胃癌取扱い規約第 14 版)の胃上部癌患者に対する LATG/LAPG の
安全性が証明された(短期成績のみの試験、長期成績についてはJCOG0912を転用するという意見)
食道胃接合部癌に関する安全性は保証されていない
LADG 同様、cStage II以上の胃癌に関しては腹腔鏡下手術を推奨する根拠は極めて乏しい
- JCOG1401において主要評価項目である Grade 2-4 の食道空腸吻合部の縫合不全発生割合が 2.5%であり LATG/LAPG の安全性が証明された
- JCOG1401において在院中の Grade 3-4 の全合併症発生割合は29%であり、治療関連死は認めなかった
- LTGは開腹手術と比較して出血量、在院日数を有意に減少させ,合併症を減少させる可能性があるが,手術時間は延長する
- 膵液瘻ならびに縫合不全については,LTG と OTG とで同等とされている
- LTG D2 郭清において,膵尾部ならびに脾門部郭清を伴う術式で膵液瘻の発症が高い
- NCDデータ(N=32144)でもStageⅠA -ⅠB 症例ならびに Stage Ⅱ – Ⅳ症例の両群において LTG が OTG に比べて術中出血量、術後在院日数ともに有意に減少
- しかしNCDデータでは縫合不全,手術時間は LTG で有意に高い
大腸癌
- 総論
- IMV切離は性腺動静脈の同定ができてから行う
- JCOG0404
下行結腸癌
- 脾湾曲よりはIMA根部を温存し(+AMCA切離検討)FEEA再建
- SDJよりは通常の左側大腸癌同様+脾湾曲受動術
TAPP
- 前方アプローチと比較すると腹腔鏡下修復術の手術時間はやや長く,漿液腫は多いが,術後疼痛は軽度で血腫,神経損傷,慢性疼痛が少なく,社会復帰が早いと評価されている
- 再発率は腹腔鏡手術が5 %以下,前方アプローチが 4 -7.6%と報告されている
- 術後疼痛については腹腔鏡手術が10%前後,前方アプローチが20%前後で腹腔鏡手術の方が少ないとされる
- 漿液腫はTAPP法後では18%と報告されている
- 前施設ではパリテックスMサイズを使用していた
- タッキング不要のデバイスは再発多い
- セキュアストラップ
- 巨大ヘルニアの場合はVERSATEX15㎝×15㎝(それ以上のサイズもある)をカットして使用する
- Optical法は直視鏡でみながらねじりこむ。外腹斜筋→内腹斜筋→腹横筋筋膜→腹膜となり腹腔に入る
- TAPPやTEPでは内鼠径ヘルニアの際にはpseudo sacをエンドループで結紮するかCooperに固定することで漿液腫を減少させる方法がある
癌領域
胃癌
Stage
罹患率
死亡率
手術合併症
予後
当院のLDG手順
右側結腸癌
左側結腸癌
直腸癌
リンチ症候群
- ミスマッチ修復遺伝子であるMLH1,MSH2,MSH6,PMS2のいずれかの遺伝子の両アレルに不活化が起きており,そのタンパクの発現が消失した状態
- 第3番染色体上の MLH1 、第2番染色体上の MSH2・MSH6 、第7番染色体上の PMS2 が原因遺伝子とされる
- 1次スクリーニング(改定ベセスダかアムステルダム基準)
- 2次スクリーニング(MSI検査か免疫染色)
MSI検査(切除標本検体)は保険収載されている
MSI検査では5種類のマイクロサテライト領域を用いてその長さを比較し、2種類以上のマイクロサテライト長の変化を認める場合をMSI-Highと診断する - 免染は未収載、免疫染色検査の偽陰性率 は5~10%
MSIと免染の一致率は90%でガイドラインではどちらでもよい - BRAF V600E変異が見られた場合には、リンチ症候群である可能性がほぼ否定されるため遺伝学的検査を行わない
- MSI-High大腸癌は進行癌ほど頻度が少なくなる
MSI-Highは大腸癌全体の15%(10%が散発、5%がリンチ症候群)
StageIV癌におけるMSI-Highの頻度は4~8%(海外データ)、本邦では1.9~3.7%
外科救急疾患(各論)
急性虫垂炎
- 国際ガイドライン:WSESエルサレムガイドライン、2020初回改定
- 保存治療後5年の再発率39%
- いかなるときでもラパロが推奨されるが、SILSは推奨できない
- 断端埋没は不要(合併症率に差なし)
- 腹腔内洗浄、ドレーン留置に明らかなエビデンスなし
- 穿孔性急性虫垂炎保存治療後のIA→再発率は1/8人程度で一律には推奨できないと位置付けている
- 費用:ラパアッペは65万円前後、開腹は51万円前後かかる (100%自己負担時)
- 妊娠時虫垂炎→ラパアッペが良さそう、DPCデータベースで418例/3年間
- Uncomplicated appendicitisの場合、7割が緊急手術を受けている
- 膿瘍の経肛門ドレナージという方法もある
Alvaradoが提唱したスコアリングシステム(1986)は症状や血液検査所見の8項目からなり合計が10点です。それぞれの頭文字を取ってMANTRELS scoreとも呼ばれます。
- Migration to the right lower quadrant(右下腹部への痛みの移動):1点
- Anorexia(食思不振):1点
- Nausea and vomiting(悪心・嘔吐):1点
- Tenderness in the right lower quadrant(右下腹部痛):2点
- Rebound pain(反跳痛):1点
- Elevation of temperature>37.3℃(37.3℃以上の発熱):1点
- Leukocytosis(10000/μL以上の白血球数上昇):2点
- Shift to the left(好中球分画70%以上の左方移動):1点
7点以上であれば可能性は高いとされ,一方で3点以上では可能性が低くなります。
虫垂炎疑いの患者さんを診療するときは,特にこれらの項目の病歴収集,診察,検査を考慮しましょう。もちろん,他のバイタルサインやBlumberg徴候などの特異的な所見の有無も重要です。
S状結腸軸捻転
- PEGにようにPEC(経皮的内視鏡的結腸瘻造設)することで捻転防止と脱気が可能(保険適応外)
SMAO
・治療前に心エコーで左房内血栓評価する 、リズムの確認(Afでないか)
・治療選択肢は5択(血栓溶解、血栓吸引、血栓除去、腸切除、ヘパリン全身投与)
・一番確実な治療法は開腹血栓除去術(心外科コンサルト必要)
血栓溶解療法
- 適応:SMA本幹閉塞では5時間以内、SMA遠位部の閉塞では12時間以内
- 手技:SMAに親カテ留置、サイドホールあけたマイクロカテを閉塞内に埋め込んでUK注入
- Urokinase(UK)6万単位(1V)を生食10~20mLに溶解、毎分1~2万単位の速度で注入
- UK使用量は12~96万U程度(有効時は36万単位ぐらいで溶ける)
- 合併症:心房内血栓が一期に流れ出すshower emboli
(参照:2004日本血管造影・IVR学会技術教育セミナー)
血栓吸引療法
開腹SMAアプローチでの血栓摘出術
- 横行結腸間膜尾側でSMAにアプローチする
- SMA神経叢をむきむきにして外膜露出させブルドッグ鉗子でSMAクランプしたけど下痢しなかった(前壁は外膜ムキムキにするが、後壁はテーピングができる程度に神経の剥離を極力手控える。郭清しなければ下痢しない?)
- クランプ前に全身ヘパリン化(0.1mL/㎏=100U/kgをIVする)
- ヘパリン化3分後に中枢側末梢側をブルドックでクランプ
- クランプの間をSMAを尖メスの先で小切開
- 3Frフォガティ―カテ+1mL生食(0.1~0.2mL程度でインフレーション)
- 縫合は6-0両端針で両端から縫合、中央で結紮
- 結紮前にdistalからデクランプ→結紮→proximalデクランプ
- 治療が奏功するとその瞬間から腸管血流改善し色調が戻っていく
問題点は微小血栓が除去しきれない可能性がある点(臨床的には問題ないだろうが)
ベストはハイブリッドERで血栓除去後に造影するのがいい、術後に造影CTでもよい
腸切除
- 腸管気腫があれば原則切除+2nd loook
- 大量切除のときは血行再建の適応なし
- 小範囲切除の時はcotroversial
保存治療(ヘパリン全身投与)
- 腹部症状の乏しい症例
- DyCTや血管造影にて末梢造影効果を認める症例
短腸症候群の管理
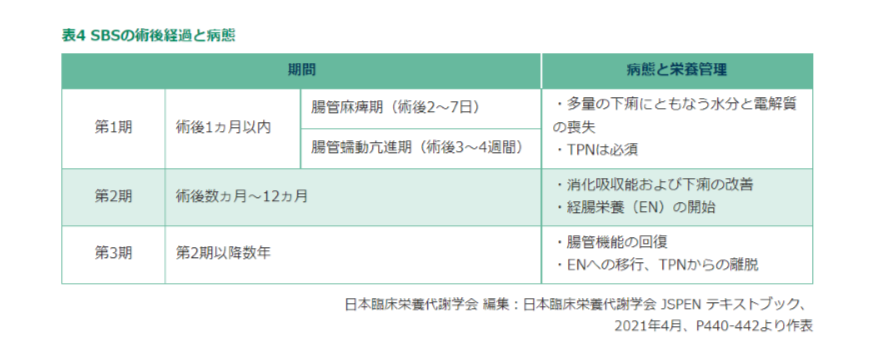
・短腸症候群治療薬レベスティブ皮下注が発売されたが薬価が高額すぎる(1日8万、連日投与)
・短腸症候群でもワーファリン吸収良好
・腸管粘膜の再生に急性期にGFOがよい
・長期的には低脂肪の経管栄養製剤がよい
レベスティブに含まれる成分のテデュグルチドは、天然型GLP-2よりも長く腸管へ作用する組換えヒトGLP-2アナログ。レベスティブ皮下注用は、回腸・結腸に存在する内分泌細胞のL細胞から分泌される天然型グルカゴン様ペプチド-2 (GLP-2)と同様に、腸管内における腸内分泌細胞・腸上皮下筋線維芽細胞に存在するGLP-2受容体に作用し、インスリン様成長因子-1(IGF-1)等を介した陰窩細胞の増殖及び腸細胞アポトーシスの阻害を通じて、絨毛高と陰窩深の増加を促進する。
・1瓶79302円、1日1回連日投与
内臓動脈瘤、消化管出血に対するIVR
・F部長の手技
・緊急は5frカテを使用(予定IVRは4fr)
・CeAはコブラでGDAにひっかけてボストンの2マーカーのマイクロカテ(BREAKTHROUGH2)とマイクロワイヤー(アサヒマイスター)を使用
・コイル塞栓では必ず2マーカーを使用する(マイクロカテの手前のマーカーをコイルのマーカーが通過した瞬間がコイルリリースのサイン!)
・Detachableコイルはボストンのインターロック(毛付きで太く硬い、デバイス自体も固い)とストライカーのTARGET(種類多いが腹部領域ではTARGET XLとTARGET XXLを使用する、TARGETのメリットは細く柔らかくいくらでも追従する感じ、デメリットは必然的にコイルの使用本数が増えるため大事な場面で使用する)
・仮性動脈瘤の塞栓の場合には、壁がしっかりあるところは硬めのインターロックで、壁が脆弱もしくは破綻しているところは柔らかいTARGETを使用しているような印象だった。
・XXLはXLの50%ボリュームアップで止血力が強化されている。多少XLより硬いが誤差範囲。インターロックの硬さに比べれば大した問題ではない。
・ストライカーのINZONEパワーサプライは位置決めしたら先端を挿入するだけ、OKがでたら1回白いボタンを押すと自動的にコイルが離断され、ピーピーピーとなったら透視見ながら抜去する。
・GDAの動脈瘤を塞栓するには3㎜、4㎜、5㎜のコイルを使用した。
・瘤内を超えて末梢にマイクロが入るかが勝負だがすんなり入っていた!さすが!!
・ふだんはトルネードも使用すると
・CHA造影は4の20、SMAは5の25
・インターロックは1本7万円で割と安い方
NOMI/OAM
- 死亡率50%にまで改善(施設間格差大きいだろう)
- 2nd look operationが基本、1回目は切除だけでOAMで終了
- 48時間後に手術を行う。72時間以上のOAMは感染リスク高くなる
- OAM→アイソレーション半分に切って穴開けて乗っけてドレーン入れてアイオバン貼る→中身が見えるのがよい
- 腸管虚血マーカー:I-FABP→粘膜障害、SM22→全層性壊死
術後縫合不全
- 術前低栄養で縫合不全のリスクが高い場合
カテーテル空腸瘻を考慮する
穿孔部の外置術を考慮する(=ストマ)
挙上不能ならTチューブドレナージを考慮する
保険術式名はK727 腹壁外腸管前置術
食道破裂
- 縦隔限局型は開腹アプローチのみでよい
- 術後は胸水たまるので最初からトロッカーいれておいてよい
- POD7でCT撮像+食道造影で胃管抜去する
- 縫合閉鎖は層々
- 胸腔内穿破型→左開胸もしくは斜め同切り
- 縫合閉鎖ののち、経食道裂孔的に胃底部で穿孔部をパッチする
AEF
大動脈食道瘻(aortoesophageal fistula:AEF)に対しては、胸部大動脈ステントグラフト(thoracic endovascular aortic repair:TEVAR)で病状を安定化させてから、食道切除術を行い、最終的にホモグラフト移植術と大網充填術を併せて行うという治療戦略が望ましいのではないか――。東京大学心臓外科の齋藤綾氏は、3月18日まで開催されていた第76回日本循環器学会(JCS2012)のシンポジウム「大動脈疾患に対する低侵襲治療の現状と課題」に登壇し、自らの見解を発表した。
今回われわれが行ったステントグラフト内挿術は,感染性動脈瘤に対して感染巣の除去を行わず異物を挿入する方法で,原則的に相対禁忌とされ,あくまで外科的血行 再建術の適応のない全身状態不良例や外科手術前の緊急避難的暫定処置に限られているとされている.しかし, 感染性動脈瘤に対して抗生剤投与とステントグラフト内挿術で良好な結果を得たという報告が散見されるように なってきた.消化管との瘻孔形成は予後不良であるが,大動脈食道瘻の場合絶食とすれば通過するのは基本的に唾液のみであり,消化液が通過する小腸や大腸と比較すると感染の制御は行いやすい.そのため大動脈食道瘻に関しては食道再建さえ行えば救命可能とする報告もある.
1次性:グラフト置換+食道抜去が基本(ハイリスクでは緊急回避的TEVARも選択肢)
2次性:一期的食道抜去+ステント抜去が基本
ショックの場合は根治手術までのBridge TEVARもある。
Bridging TEVAR is a useful adjunct in treating AEF patients with shock. One-stage surgery consisting of resection of the aneurysm and oesophagus, in situ reconstruction of the descending aorta and omental flap installation provided a better outcome in the AEF surgical strategy compared with conservative treatment.(神戸大学心臓血管外科)
左開胸で食道抜去するのがみそ。確か、大学でもAortaと食道がくっついてて大変だった。
閉塞性大腸癌
- BTSを前提としたステント療法が広まっているが長期成績に関するデータは乏しい
HCCrupture
- 輸血を準備、エコーで診断
- ゼラチンスポンジによるTAEを優先し次善策として開腹手術
- 待機的に肝切除術に移行するのがベスト
- 緊急TAEの塞栓物質はセレスキュー1枚+造影剤のみ(抗がん剤ストックない)
- 最初からシェファードフックでSMAG→SCAG→マイクロで選択した肝動脈造影という流れ
- 少量で塞栓終了(1~2mL、セレスキュー1/4枚程度)となることもある
- AngioやCTでextraが描出されることはまれ
- TAE中に肝臓と肋骨の間隙が増大傾向ならばすぐに開腹移行
- シェファードで右腎動脈、下横隔動脈造影、左胃動脈造影をオプションで追加する
- 左右肝動脈に入れ分ける長いマイクロカテ操作の場合はコブラをPHAまで進める
- 前医で造影CTが撮像されていても動脈相がないようなときはCT撮り直しも考慮
- TAE施行しても血腫による腹満はすぐには改善しない
- IVRの基本手技について
Mirizzi症候群
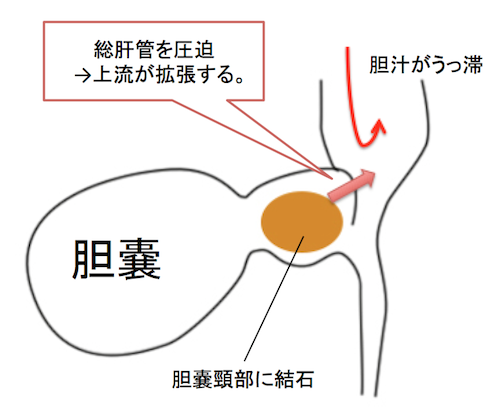
- Mirriziでは肝内胆管が拡張する
急性胆嚢炎




- TG18では耐術可能症例はすべて手術適応(=ラパコレ)となった
- 診療手順は
①急性胆嚢炎の診断
②重症度判定
③リスク評価(ASA-PS3以上またはCCI6点以上は保存治療)
④手術 - 抗血小板剤・抗凝固剤について
アスピリン単剤→継続のままESTもPTGBDも可
プラビックス→5-7日休薬してからEST/PTGBD
ワーファリンはINR治療域内なら内服継続のままEST
DOAC→ヘパリン置換なしに短期休薬でEST
EPBDは低出血危険度手技のためESTの代替療法となる
緊急手術の場合は抗血小板剤は休薬不要、抗凝固は出血量⇧のため個々に判断
大動脈解離のmalperfusionに対する術式
- 胸骨切痕や腹部エコーでAorta内のフラップを診断可能
- central repairが基本だがすでに形成された血栓はすぐには解除されない
- central repairでmalperfusionが解除されない場合は追加治療を検討する
- 追加治療の選択肢は①TEVARを追加②SMAへのVIABAHN③SMA分枝へのバイパス
- さらに試験開腹+silo closureで腸管血流をモニタリング(NOMIやDCSに準ずる術式)
- 吻合した場合もサイロクロージャ―にして吻合部を窓の下にモニタリングできる
- 無理に閉腹するとACSをきたし腸管壊死を悪化させるため3期的4期的閉腹も考慮する
- 小腸は漿膜色不良あっても保存治療が可能(結腸の漿膜色変化は切除の絶対適応)
SMV血栓症
- 静脈うっ血による腸管浮腫、腸間膜浮腫を呈する(絞扼性腸閉塞に類似)
→NOMIやSMAOでは動脈虚血がメインのため浮腫は目立たない - 血栓摘出(フォガティ―)や溶解療法(SMAからウロキナーゼ持続動注)を考慮する
- 80%が続発性(肝硬変、腫瘍、外傷、炎症、ピル)
- 先天性の素因検索(プロテインS/C、ATIII、プラスミノーゲン)
- 急性は腸管壊死にいたるが慢性SMV血栓症では壊死にならない
消化性潰瘍穿孔
- 保存治療の適応(ガイドライン2015)
①24時間以内の発症
②空腹時の発症
③腹痛が上腹部に限局
④腹水が少量
⑤重篤な合併症がなく全身状態が安定
※除外項目として70歳以上は基本的に手術 - 穿孔部閉鎖+大網被覆+洗浄ドレナージが推奨される
- 閉鎖が困難な場合は大網充填術が選択される
- 2015 年度には胃十二指腸潰瘍穿孔に対する手術の中で腹腔鏡手術の占める割合は 49.8%
- RCT の結果,術前リスク(穿孔発症後 24 時間以上経過,入院時収縮期血圧 90mmHg 以下のショック状態,ASA III/IV に相当する全身疾患)のない患者の場合には,腹腔鏡手術の方が開腹手術より優れている(JSESガイドライン2019)
憩室出血
- DyCTでEV+ショック+ならそのまま手術
EV+ショックーならCSもしくはTAE
EV-なら待機的CS - NSAIDS常用者は穿孔、出血のリスク上がるため休薬する
- 出血:5~15%(3.1%で生命に関わる出⾎) 憩室穿孔:4%
- 76~92%が軽快するが14~43%で再出血する(1か月以内が多い)
- 内視鏡治療後再出血率:11~38%, IVR後出血率:30%
- 早期にCS施行し内視鏡で右か左かくらいの目星だけでもつけておくべき
- 再出血時はニフレック1Lを内服しCS再検
- 出血部位が同定できない、止血処置困難な場合はバリウムパッキング
- 内視鏡下バリウム散布
散布チューブでまく
クリッピング後に散布することもある
バリウムは濃度50~100W/Ⅴ%(100gをTotal100mLにまで溶解すること)で。
バリウム濃度[w/v%]=バリウム量[g] / 出来上がり量[ml] ×100[w/v%]
バリウムパッキングには再出血予防効果あり(従来療法群42.5%、バリウム群14.8%) - 右側が出血量多い
- 憩室出血のCSは透視室で。クリップの位置を確認できる
- 大腸憩室症ガイドライン2017(憩室出血編)
- 憩室出血の死亡率1%
- 自然止血率は70~90%
- 再出血率は30~40%/2年
- アスピリンやNASAIDS(全種類)は出血のリスク
- CSは24時間以内に行う
- 早期施行群の方が出血源同定率が高かった報告がある
- 内視鏡止血が困難ならTAEを推奨する
- TAEが困難なら手術を考慮する
- バリウムパッキングは実施しないことを推奨する




憩室炎、憩室穿孔


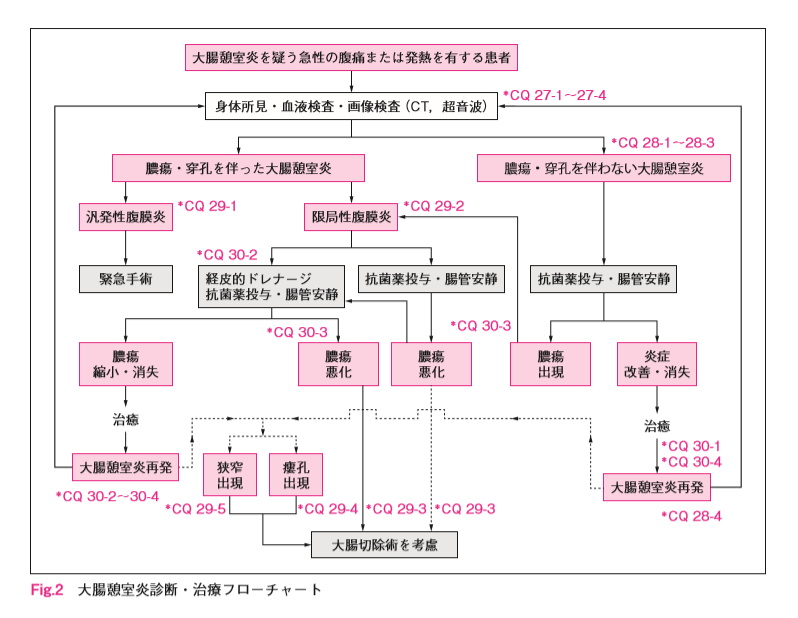
- REVIEW論文
憩室炎の70%はStage0-Ia→保存治療成功率93-100% - 20%がlocalized abcessに進展(StageIb-II)
- 膿瘍径<4㎝の保存治療成功率70%
- 6%が重症腹膜炎にいたる(死亡率14%)
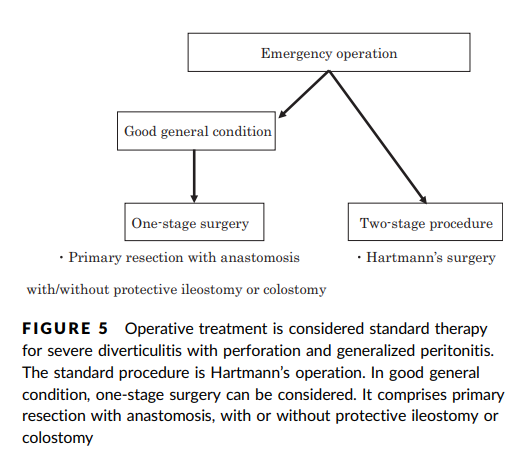
- 術式:2期的手術が一般的
- 全身状態よければ初回に切除再建+protective ileostomy or colostomyも選択肢
- laparoscopic colonic resection for Hinchey stage I-II diverticulitis is at least as safe and effective as traditional open surgery
- 保存治療後の再燃率18.1%(mean interval 4.7-5.9months)
- 大腸憩室症ガイドライン2017(憩室炎編)
- 喫煙と肥満が憩室炎の危険因子
- 保存治療後の再発率は高い
- NSAIDSについては相反するデータがある→可能なら中止
- JSESガイドライン2019(大腸編)

- 穿孔性の憩室炎(Hinchey 分類 3:膿性腹水を伴う汎発性腹膜炎)に対し,従来の開腹での憩室炎部分の腸管切除および人工肛門造設術(Hartmann 手術)に対して,腸管切除を伴わない腹腔鏡下洗浄ドレナージ術が有効率が高く,合併症も少なく,死亡率を悪化させることはない治療法と報告された 9, 10)。
- システマティックレビューでも死亡率は 5%未満であり,大多数の患者では人工肛
- 門手術が行われなかったと報告されている 11)。
- その後の 1 つの多施設ランダム化比較試験 12)では死亡率および重篤な合併症で差がなく,腹腔鏡下群で全入院期間が短く,再手術と最終人工肛門造設率が減少して有効であるとされ,Sweden のランダム化比較試験 13)でも腹腔鏡下の洗浄で再手術が減少し入院期間も減少するなどその有効性が証明されているが,2 件のランダム化比較試験 14, 15)では開腹での病巣切除との比較で重篤な合併症や死亡率で両群に差はなく有効性は見いだせなかったとしている。



食道静脈瘤破裂
- エコーでLCや腹水、胃内貯留物の確認
- ショックの場合は挿管が安全
- 緊急止血はEVLが第一選択、第2選択はSBチューブ(EVLとSBTで止血率に差はない)
- 緊急例の結紮は一発、他の部位の結紮はCRS+++なら行ってよい
- EVL後の瘢痕を有する食道静脈瘤では、それに続くEISが有効
- 治療歴を有する症例は粘膜吸引が不十分となる可能性がある
- 止血でき次第引き続き硬化療法に移行するため早期転院を目指す
- 入院中の食事は流動食程度まで
各種腸炎
- 鑑別疾患として、IBD、虚血性腸炎、感染性腸炎、自己免疫性疾患など
- 感染性腸炎の検査:
- 便培養でサルモネラやキャンピロバクターを
- 生検検体の鏡検でアメーバ原虫、ランブル鞭毛中
- 血液検査でアメーバ抗体
- クオンティフェロンTB – 2G
- 腸管スピロヘータ症(グラム陰性螺旋菌である Brachyspira属B.pilosicoli と B.aalborgi)
- 人畜共通感染症(ヒト,犬,豚,猿,ニワトリなど)
- 感染経路:主に糞便を介しての経口感染、免疫不全患者の日和見感染
- 感染頻度:大腸生検材料を用いた検討では慢性下痢患者の 0.7%、有症状者 の 5 %
- 主訴:下痢と血便
- 内視鏡所見:区域性の浮腫と発赤の集簇、潰瘍形成
- 治療はMNZ内服が著効する
- 病理検査:HE強拡大で粘膜表面のびまん性の好塩基性毛羽立ち(false brush border )を観察しWarthin Starry染色で確認する
- 発見契機の半数以上は、生検検体により偶然発見される
- 本邦では 1998 年に Nakamura らによって初めて報告
- 螺旋状の形体で活発な運動を行う菌群
- トレポネーマ属,ボレリア属,レプトスピラ属などがある
- トレポネーマ属はヒトや動物に寄生し,梅毒などの病原体となる
- ボレリア属は回帰熱,ライム病の病原体で,シラミ,ダニを介して感染する
潰瘍出血
- 止血にはHSE(10%NACl10mL+注射用水10mL+ボスミン1㎎)を1か所につき1mL程度局注する
- クリップ止血が安全、垂直にキツツキのように突き刺すイメージ
直腸潰瘍
- 大量の鮮血にて発症
- 止血しても再出血を繰り返しやすい
- 内視鏡的クリップ止血や経肛門的結紮止血術を行う
腸重積症
- 押し出すのが基本(→バリウム注腸と同じ原理)
マロリ ーワイス症候群
- 自然止血も期待できるが、出ている場合はクリップが良い。やわらかいのでガバッと大きくつかんでよい。ダウンアングルで吸引でクリッピング。
- マロリーの吐血は赤い鮮血
- 途中から赤い嘔吐が始まるのが特徴。NSAIDSやステロイドの内服歴とか聞く。
angiodysplasia/angi(o)ectasia
- 胃においては上部消化管出血の原因の5%未満
- 大腸出血の5%前後
- 小腸出血においては主要な原因の1つ(30%前後)
- 大腸においては管腔が広く,内圧が高い右側結腸に多い
- 小腸においては十二指腸,上部空腸に好発する
- 発生には局所循環障害に反応する自律神経を介する血管平滑筋の弛緩,腸管の平滑筋収縮と内圧上昇に伴う静脈還流の閉塞などで前毛細血管括約筋が慢性的に障害され動静脈吻合が生じるという説が支持されている
- 出血性angiodysplasiaは慢性腎不全,心臓弁膜症・心不全,門脈圧亢進症などの基礎疾患に合併する頻度が高い.
- angiodysplasiaは同時性,異時性に多発している場合が多く,1か所治療を行ってもその後の経過で他部位より出血することがある.
ヘルニア嵌頓
- 外鼠経ヘルニア嵌頓→腸切除なしならdirect Kugel(SAC処理なし)またはTAPP、腸切除アリならMarcy+IPTR
- 内鼠経ヘルニア→Direct Kugel 腸切除アリならIPTR
- 大腿ヘルニア→Direct Kugel 腸切除アリならモシュコビッツ+IPTR
- 閉鎖孔ヘルニア→DirectKugel 嵌頓非整復なら開腹手術
- 閉鎖孔ヘルニアの整復方法

- 整復は股関節を屈曲・外転位(開排位)にして行う。
肝膿瘍
- 穿刺が基本
- 18GのPTCD針→0.035ラジフォーカス→8Frダイレーター→7Frピッグテール
- 初回は造影しない(容易に造影剤が肝静脈に流れ菌血症を増悪させうる)
小腸腫瘍出血
- 栄養血管がJ2,J3であればラパロの小切開創から体外に挙上可能
その他の疾患(ヘルニア、ヘモなど)
胆嚢腺筋腫症 adenomyomatosis
・腺筋腫症が正しい(日本胆道学会)
・胆嚢壁内の Rokitansky-Aschoff sinus(RAS)増殖および周囲平滑筋細胞の壁内増生による胆嚢
壁の肥厚を主体とする病態
・腹腔鏡下胆嚢摘出術を施行した 2.5% に ADM を認める(日本内視鏡外科学会)
・ADM に合併した胆嚢癌は ADM の 1.4~6.6% と報告されている
・ADMは90%に胆石を合併する

化学療法
★★★最新のトピック★★★
・Stage2-3のMSI-H直腸癌は手術せずドスタルリマブ(PD1阻害薬)でCR率100%!第2相試験,USA,NEJM2022/6月
ICIとirAE
★投与量 :ニボルマブ投与量は癌腫により差はなく一定
・1回240mgを2週間間隔又は1回480mgを4週間間隔で点滴静注する。
・胃癌で併用療法の場合には3週ごとに360㎎。
・免疫チェックポイント阻害薬に減量という概念はない。
★投与中止基準→NCCNガイドラインに準拠する(下記に原則を抜粋)
https://www2.tri-kobe.org/nccn/guideline/supportive_care/japanese/immunotherapy.pdf
①一部の神経毒性・血液毒性・心毒性・呼吸器毒性を除いてGrade 1のirAEについては慎重にモニタリングのうえ、治療を継続することができる。
②多くのGrade 2のirAEについては治療を休止し、症状がGrade 1に改善した場合は投与の再開を考慮する。また、副腎皮質ステロイド(プレドニゾロン0.5~1mg/kg/日または同力価のステロイド)による治療を検討する。
③Grade 3のirAEについては治療を休止し、高用量の副腎皮質ステロイド(プレドニゾロン1~2mg/kg/日またはメチルプレドニゾロン静注1~2mg/kg/日)を開始する。症状が改善したら、副腎皮質ステロイドは少なくとも4~6週かけて漸減する。高用量コルチコステロイドによっても48~72時間で症状の改善が認められない場合は、インフリキシマブなどの免疫抑制剤の使用を考慮する。
④症状や検査値がGrade 1以下に回復後に投与の再開を検討する。しかしながら早期にirAEを発症した患者についての治療再開には特に注意が必要である。また免疫チェックポイント阻害剤の用量調整は推奨されない。
⑤Grade 4のirAEはホルモン補充によってコントロール可能な内分泌障害のirAEを除いて、免疫チェックポイント阻害剤の投与は中止する。
⑥ICI投与終了後にirAEが出現することもあるので注意(特に2か月以内)。

(小野薬品 https://www.iraeatlas.jp/general-remarks/basic-principles.html )
★日常診療の管理方法 https://www.gi-cancer.net/gi/fukusayo/fukusayo_15_2.html
・臨床試験では47%に何らかの有害事象が生じた(非小細胞肺癌)。
・出現頻度>5%:間質性肺炎、甲状腺機能低下、大腸炎、Infusion reaction、肝障害
・投与期間中は定期的(月1回程度)にTSH、FT3、FT4の測定を行うが、患者の自覚症状や検査所見に応じて、適時実施する。
・副腎機能低下症を併発する場合があるので、特に倦怠感が出現した際には甲状腺検査と併せてACTHやコルチゾールの追加測定を検討する。
・甲状腺機能障害に伴う症状の有無を確認し、FT4<0.9ng/dLもしくはTSH>10μU/mLを示した場合や、2回連続して異常値の場合、ホルモン補充療法としてレボチロキシンNa水和物25μg/日からの開始を検討する。しかし、副腎機能障害を合併している場合には、甲状腺ホルモンの補充のみを行うと、副腎不全を悪化させることがあるため、このような症例に対しては副腎皮質ホルモンの補充を先行する。
・PD-1阻害薬による治療を行う患者では、治療開始前にTgAb/TPOAb検査を行い、陽性であれば甲状腺エコー検査を行うことにより、甲状腺機能障害の発現リスクを評価できると考えられる。
・甲状腺機能亢進症では、軽度であれば経過観察し、全身症状が強い場合は対症療法としてβ遮断薬の使用を検討する。重症の場合はステロイドの使用を検討する。
・血糖値が300mg/dL以上など1型糖尿病を疑う血糖上昇を認めた場合は、インスリン治療の開始を検討のうえ、血清Cペプチド、尿ケトン体を検査する。糖尿病性ケトアシドーシスの場合には、輸液、電解質補充、速効型インスリン持続静注などの適切な処置を行う。
・劇症1型糖尿病発症時のHbA1cはあまり上昇しておらず、糖尿病関連自己抗体(20種類くらいある、抗GAD抗体が有名)も原則として陰性である。
・間質性肺炎→自覚症状や胸部画像検査、血清マーカー(KL-6、SP-D)、SpO2のモニタリングを行う。発症が疑われる場合には、胸部X線の画像所見やマーカーの確認を行い、呼吸器感染症(ニューモシスチス肺炎)や肺水腫との鑑別を行う。
・間質性肺炎ではGrade 1であっても免疫チェックポイント阻害剤の投与は中止し、症状の改善がない場合は副腎皮質ステロイドによる治療を検討する。
・なまワクチンは投与すべきでない。コロナワクチンは投与してよい(日本癌治療学会) http://www.jsco.or.jp/jpn/index/page/id/2379#qa3_3)
接種のタイミング: ICI投与予定日前の2,3日以内を避ける(ワクチン接種後2,3日は発熱を認めることがあるため)
化学療法総論
Infusion relaeated reaction(IRR)/インフージョンリアクション
・IRRとは分子標的薬をはじめとしたタンパク製剤投与時に多く発現する有害反応
・IRRの発現機序については詳細については明らかにされていない(サイトカインの放出?)
・IgE抗体を中心とした免疫応答が関与するI型の過敏反応とは異なる
・IRRの症状は非特異的なものが多く、明確な診断基準はないが重症例は少ない
・典型的な症状である発熱や悪寒、発疹、呼吸困難感、血圧低下から総合的に判断する
・IRRは抗原としての感作を必要とせず発症するため、ほとんどが初回投与時、かつ投与開始から24時間以内に生じる
・Trastuzumabでは初回には40%の発現率を示すが、次回以降の発現率は大幅に低下する
・CetuximabでもIRR発現の約90%は初回投与時であった
・IRRの場合、投与再開時には投与速度を減じて投与を行うことで治療継続可能

・アレルギー反応→蕁麻疹や潮紅、喉の絞扼感、呼吸困難感はアレルギー反応に多くみられる傾向があり、重症例では喘鳴や意識消失、循環不全等を伴う。発現リスクのある薬剤として、タキサン系やプラチナ製剤がよく知られている。
・一般的には、薬剤アレルギーのあった薬剤の再投与は原則行うべきではなく、安易な投与は避けるべきである

UGT1A1遺伝子多型
イリノテカンの代謝酵素UGTの1つであるUGT1A1。UGT1A1に相当する酵素には個人差、すなわち遺伝子多型が存在する。発現に影響を与える遺伝子で最も頻度が高いのがUGT1A1*28である。正常型ではUGT1A1のプロモーター領域のTAリピート数は6回[(TA)6TAA]であるが、変異型UGT1A1*28では7回[(TA)7TAA]となっている。また、他にUGT1A1*6も知られており、211G→Aに置換されている。
・UGT1A1*28の場合はUGT1A1の発現量が少ない。
・UGT1A1*6ではUGT1A1の活性が低下しているため、いずれもグルクロン酸抱合が遅延し、SN-38の体外排泄も遅延する。
・ホモ(9%程度の頻度)では重症化率80%のため減量が必須、ヘテロ接合であればまだ大丈夫。
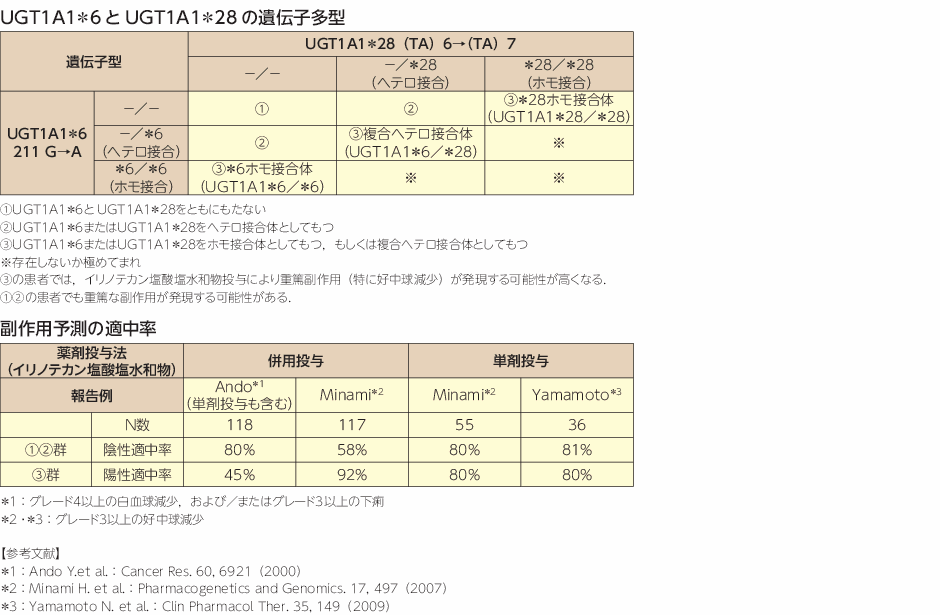
[頻度]
UGT1A1*6アジア人:11~23% 白人:0%
UGT1A1*28アジア人:7~16% 白人:30~40%
胃癌化学療法
胃癌ACT
大腸癌化学療法
- PARADIGM試験:国内第III相試験
原発巣が左側および全体のいずれの大腸がん患者さんにおいても、mFOLFOX6 +抗EGFR抗体薬併用療法がmFOLFOX6+抗VEGF抗体薬併用療法に対し、統計学的に有意な延長を示した(原発巣が左側の患者さんにおいて、パニツムマブ群mOS:37.9ヵ月、ベバシズマブ群mOS:34.3ヵ月)
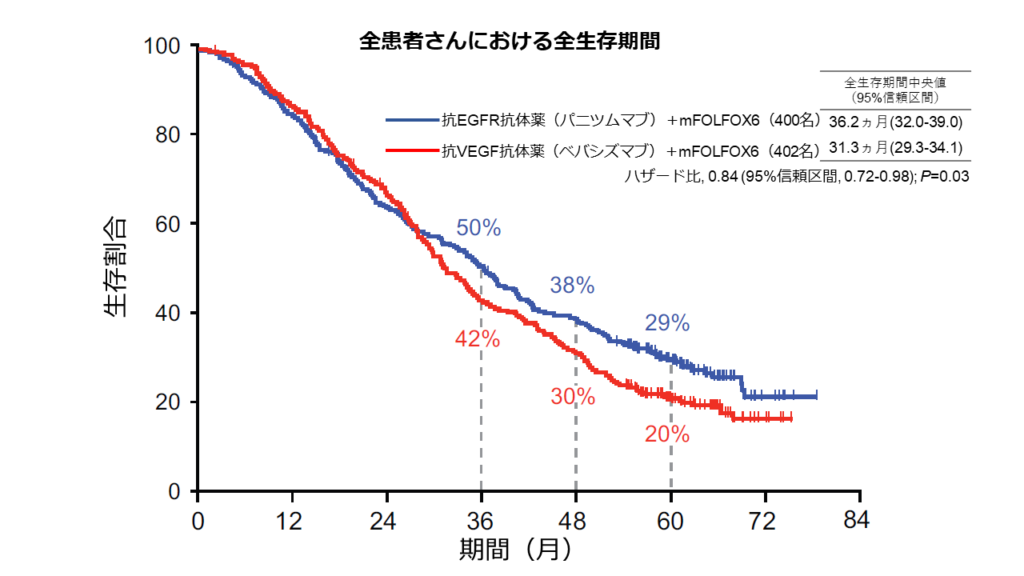
有害事象
3rd Line:Regorafenib
・3rd以降でプラセボに比べて+1か月のOS延長効果(OS6か月vs5か月)
・65歳未満ではregorafenib、65歳以上ではTAS-102の方が有効な傾向あり(REGOTAS)
・Rego後のTASは、Rego後プラセボに比べて予後延長効果あり( RECOURSE試験 )では逆は?
・RegoもTASも4週=1サイクルで同じ
緩和治療
疼痛コントロール
- がん疼痛の薬物療法に関するガイドライン(2020年版、日本緩和医療学会)
- がん診療ガイドライン、疼痛管理(日本癌治療学会)
- レスキュー投与経路は,定期投与されているオピオイドと同じ経路を使用することを原則とする
※薬剤の種類ではなく投与経路による制約である!!
- デュロテップ® MTパッチ(2008年~):
従来品の欠点であったリザーバー製剤でないので切ってもOK(規格も小さくなり使いやすい)
最小規格 2.1㎎(12.5μg/hr)=1926円、3日ごとに貼りかえる
薬物貯蔵層中に有効成分フェンタニルを含むゲルが封入されているリザーバー製剤とは異なり、フェンタニルを粘着層に溶解させた薄い半透明フィルム状の経皮吸収型製剤です。 - デュロテップ®パッチ:
従来品、リザーバー製剤のため切って使用できなかった、MTが出たのでもう使わない。 - フェントステープ:
フェンタニル製剤全般は消化器症状やせん妄が少ないとされる
1日ごとに貼りかえる製剤、協和発酵キリンと久光の共同開発
0.5㎎製剤はオピオイド先行投与なしで開始できる規格=オキシコドン10㎎相当、1日303円で安い - ワンデュロ:
フェントステープと同様に1日1回貼り替えるタイプのフェンタニル貼付剤である。
1日1回型のフェンタニル貼付剤は、症状に応じて24時間ごとに用量調節が可能な点が最大の特徴
デュロテップMTパッチで認められている「非癌性の中等度から高度の慢性疼痛における鎮痛」に対して、ワンデュロパッチは適応を有していない
主な副作用は、便秘・傾眠(各47.0%)、悪心(25.8%)、嘔吐(21.2%)など
腫瘍熱
がん患者の腫瘍熱は 5-27%と報告され、転移巣が多いほど腫瘍熱をきたしやすい。
診断基準(明確なものではない):
1)37.8℃以上の発熱が 1 日 1 回以上ある。
2)発熱の期間が 長期間である(おおよそ 2 週間以上)。
3)身体診察・検査所見 (培養検査を含む)・画像検査などにおいて感染症の根拠を認めない。
4)アレルギーによる発熱は否定的である。
5)感染が疑わしい場合、7 日以上の経験的な抗菌薬治療に対する解熱反応がない。
6)ナプロキセンテストによって速やかに完全に解熱し, ナプロキセンを使用中平熱が持続する。
対症療法:
●ナプロキセン(ナイキサン🄬)400~600mg 分 2~3 を定期投与することが勧められている。これで 12~24 時間後から丸 1 日を通して解熱すれば腫瘍熱と診断する。ナプロキセンが有効でない場合、他の解熱作用のあるNSAIDs(フルルビプロフェンアキセチル(ロピオン🄬)、ジクロフェナクナトリウム(ボルタレン🄬)、ロキソプロフェン(ロキソニン🄬))に変更することが有効な時がある。セレコキシブ(セレコックス🄬)といった COX-2 選択阻害薬は解熱効果が弱いため使用しない。またアセトアミノフェン 2.4~4.0g 分 3~4 を使用・併用することも可能である。
●上記の対応で症状緩和が困難である場合や食思不振・倦怠感など悪液質による症状がある場合は、少量のステロイド(デキサメサゾン・ベタメタゾン 2~4mg/回、ハイドロコルチゾン 100mg/回)を投与する事も検討できる。しかし、感染が完全に否定できない場合や 1 カ月以上の投与になる場合には、消化性潰瘍、血糖異常、ムーンフェイス、精神症状(不眠、せん妄、抑うつ)、易感染、ミオパチーなどの合併症を生じるリスクがある。またステロイド投与中に発熱が再発した場合、不顕性の感染が顕性化した可能性が高いので、感染の再検索が必要と思われる。
出典:http://www.kanwa.med.tohoku.ac.jp/student/pdf/manual/2019/04.pdf
呼吸困難
がん患者の呼吸器症状の緩和に関するガイドライン(2016年版)
低酸素血症がある場合のみ酸素投与が有効
塩酸モルヒネが第一選択。
塩酸モルヒネが使えない場合、オキシコドン、コデイン、ジヒドロコデインは使用可。
フェンタニルはエビデンス不足のため、ガイドラインでは使用しないことが推奨されている。
強い呼吸困難にはオピオイドにミダゾラムの併用が推奨される。
嘔気

- ドパミン受容体阻害薬
- メトクロプラミド◎ がん患者の嘔気に対するエビデンスあり
- ドンペリドン○ エビデンス少ないがメトクロ=ドンペリドンと考えられる
- 抗精神病薬◎→ブチロフェノン系を主に用いる
- フェノチアジン系〇
- クロルプロマジン(ウインタミン、コントミン) 眠気強い
- レボメプロマジン(ヒルナミン) エビデンス少ない 眠気強い
- プロクロルペラジン(ノバミン) エビデンス少ない
- ブチロフェノン系(ハロペリドール◎◎)
- フェノチアジン系〇
- 非定型抗精神病薬△ エビデンスには乏しい
- オランザピン
- リスペリドン
- 5-HT3受容体阻害薬◎
- コルチコステロイド△ 意外とエビデンスに乏しい
- H1受容体阻害薬△ エビデンスは少ないが体動時の前庭系が原因の嘔気に有効な可能性がある
- ヒベルナ
- クロルフェニラミン
- ジフェンヒドラミン
- ヒドロキシジン塩酸塩
- 抗コリン薬△ エビデンスは少ないが体動時の前庭系が原因の嘔気に有効な可能性がある
ブチロフェノン系抗精神病薬はフェノチアジン系と比較すると、アドレナリンα1受容体阻害作用や抗コリン作用、抗ヒスタミン作用は弱い一方で、錐体外路症状(錐体外路障害)が出やすいことや、長期服用で遅発性ジスキネジアの問題もある。

消化管疾患/内視鏡
上部消化管内視鏡
保険診療上の決まり
- 診療報酬の審査では、胃の内視鏡検査料(1,140点)を算定されていて、傷病名が、「逆流性食道炎」しか無かった場合には、「D306 食道ファイバースコピー 800点」に減点される可能性あり
- PPI維持療法を行う際には「維持療法の必要な難治性逆流性食道炎」が適応病名。8週間(または6週間)の期間をいつから数え始めるかについては、基本的には胃潰瘍や逆流性食道炎などの傷病名が付いた日からと考えるのが一般的。
- ピロリ菌の除菌、FDの診断・治療には胃カメラが必須
- 胃潰瘍、逆流性食道炎、十二指腸潰瘍の診断には胃カメラは必須ではない
- PPIで『NSAIDS、低用量アスピリン投与時における胃潰瘍または十二指腸潰瘍の再発抑制』に
- 保険適応があるもの:タケプロン、ネキシウム、タケキャブ
- 保険適応がないもの:パリエット、オメプラール等
画像強調内視(IEE)
- IEEの種類
- 光デジタル法:
- NBI:
照射光を 415nm と 540nm を中心波長とした狭帯域光に変更することで粘膜表層の表面構造と微小血管を強調して描出するIEE - BLI:
- LCI:Linked Color Imaging
LCIはBLI bright モードと同じ波長の照射で得られた画像を色変換処理している
粘膜の赤色調の濃淡を強調することで,赤いものはより赤く,褪色病変はより白っぽく観察される
白色光(WLI:White light imaging)では検出できない腸上皮化生や斑状発赤を呈する腸上皮化生もLCIでは特徴的なラベンダー色として観察され、より簡便に客観的に胃癌リスクを評価しうる
- NBI:
- デジタル法:
- TXI
- 色素法:
- 光デジタル法:
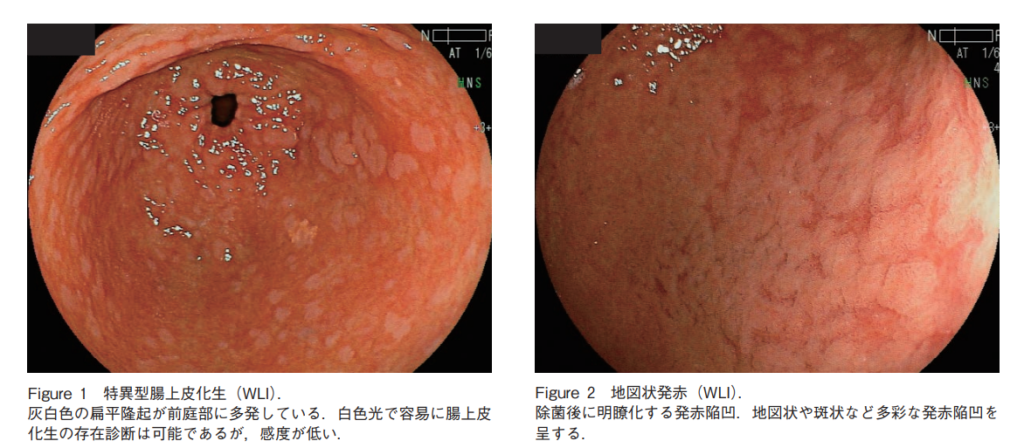
- 肉眼所見:WLIで前庭部に好発する灰白色の半隆起(LCIではラベンダー色の隆起)
- 病態:カイロミクロンの輸送異常を反映したものだが,本所見は特異度が高い一方,感度は体部小彎で6 %,前庭部大彎で 13%と非常に低い
- 非特異型の腸上皮化生は通常 WLIでは認識できないか,他の発赤病変などと鑑別できない
機材
- フジノン経鼻内視鏡の鉗子孔はΦ2.4㎜(オリンパス2.2㎜)で吸引効率大
- ディスポ―サブルクリップ HX-610シリーズ(オリンパス)
つめの角度が90度、135度、それぞれショート、ノーマル、ロングの6種類ある
上司はロング1択
咽頭観察:経鼻内視鏡+VALSALVA法
- 下咽頭喉頭観察時に,大きく息を吸った後,一気に息を吐きながら唇を結んで両頰を膨らませ続け,息を10秒程度こらえるという方法
- 梨状陥凹の観察時には『ウー』とか『エー』と発声させるとよい
食道のヨード染色
- 当院では1%、0.75%でもよい。Total20mLを散布チューブで散布する。
- C大は3%を使っていたが全例胸やけで大変だったと。 20㎝から散布チューブで巻き始める、奥へ奥へ。観察も手前から始める。
- 染まらないところは淡染か、不染か判断する→不染=癌疑いで生検する
- ヨードで染色したら食道はすぐに水で洗ってもOK
- 胃内のヨードを吸引。最後に中和剤まいて終了
酢酸インジゴ
- インジゴ5mL(20㎎アンプル1A全量)+1.5%酢酸(食用酢の1/3濃度)15mL、Total20mLを散布
- 酢酸を胃に撒布すると,酸に対する胃粘膜の防御反応によると思われる粘液が増加する.酸による粘液の産生性が腫瘍部,非腫瘍部で異なるため,腫瘍部ではインジゴカルミンの色素がwash outされることが多い反面,非腫瘍部では色素がしっかりと残存する.このメカニズムにより,従来の色素でははっきりしなかった病変の境界部が明瞭に描出され,境界診断に非常に有用である.
内視鏡的止血術(出血性胃潰瘍)
- コアグラスパー(ディスポ)の代わりにホットバイオプシー鉗子(リユーザブル)を利用しソフト凝固止血
- 鉗子でがっつり組織をつまんだら少し浮かせ気味にして何回かに分けて通電する
- トロンビン液2万単位+アルサルミン散2袋を混ぜたものをシリンジで局所にフラッシュして終了
食道ステント留置術
- OTWとスルーザスコープがあるが、カバー付きはOTWでしか留置できない
- 壁外圧迫→ノンカバーでもOK
- 食道癌→カバー付きステントがベター
内視鏡的バルーン拡張術(EBD)
- Boston社バルーン、上部と下部用がある、TTSとOTW法ともに使用可能だがTTSがスタンダード
- 初回治療時は内視鏡が通過しない病変→8/9/10または10/11/12を使用する
- バルーンは2.8㎜チャンネル対応→上部GIF260Qでも入るが経鼻スコープは入らない
- バルーンは6種類ある、それぞれ3段階までサイズ規定されている 、迷ったら大きい方で低圧で
- TTSだと20㎜径までしか製品ないがOTWなら50㎜径まである(アカラシア用)
- 拡張するのは1段階→2段階まで、3段階まで膨らませるときは次のサイズのバルーンにかえる(同じサイズであっても拡張圧が高くて危険!)
- インフレートはホールド1分→止血のため、間宮先生は2分ホールドしていた
- バルーンは7万円する。手技料は11万円。月に1回しか算定できない
- 食道、小腸、大腸でも算定できる→小腸病変はダブルバルーン内視鏡で到達して拡張する
- 透視下にガイドワイヤー付きのバルーンによる手技の方がより安全(TTSでバルーンをスコープ内に入れた状態でガイドワイヤーを狭窄部を通過させてからバルーンを挿入するが付属ワイヤーは硬いのでジャグワイヤーやラジフォーカスを用いるほうがより安全)
- 拡張中に内視鏡をバルーンに密着させると狭窄部を確認しながらダイレーションできる
- 拡張時間は1回の治療につき3分×3セットという施設もある
- 12㎜まで拡張されれば内視鏡を通過させて観察可能
- 最近ではクローン病による小腸狭窄にもEBDが普及してきている

上部消化管内視鏡所見
RAC
- RAC陽性症例は 95%の正診率で H. pylori 未感染正常胃と診断できる
- RAC の判定は胃体下部や胃角部で行う
スクラッチサイン
- クラッチサイン(scratch sign)は,おもに胃体中部から胃角部大彎において観察される,胃の長軸方向に伸びた赤い線状痕を指す
- 通常の胃内操作のみでは認めず,十二指腸へスコープを挿入した後に認められる→スコープの擦過に伴う胃粘膜表層の腺窩上皮の剝脱
- スクラッチサインは H. pylori 未感染または既感染症例に特徴的な所見
“フジツボ”様所見
- H. pylori 現感染でも認められることがあるがまれで,除菌後の症例で所見は明瞭である.
- 胃角部から胃体部にかけて認められることが多く,除菌前の萎縮が軽度(木村・竹本分類で Closed type)の症例での症例で好発する.
- 病理組織学的には胃底腺組織に囲まれた腸上皮化生で,集合すると地図状に進展する可能性がある病変である.
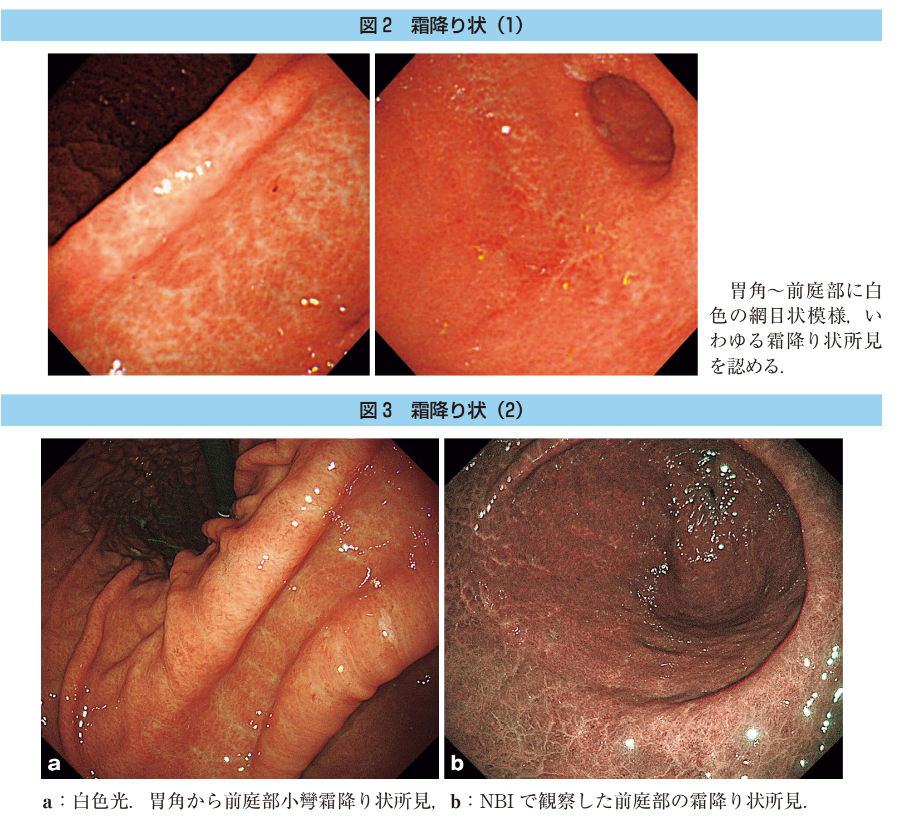
霜降り状
- NHPHの内視鏡所見としては,“鳥肌”が報告されてきたが,鳥肌以外に胃NHPHの内視鏡所見として報告されたのが,“霜降り状”所見である.
グリコーゲンアカントーシス
角化上皮を伴う表在型食道癌との鑑別が重要、その他として食道epidermization

NBI(narrow band imaging)拡大内視鏡像では,正常粘膜よりも密度が低く細い線状の乳頭血管が規則正しく分布している様子が観察できる
表面に毛様突起が認められることがある(→上皮内乳頭の増生=乳頭腫と類似の組織像か?)
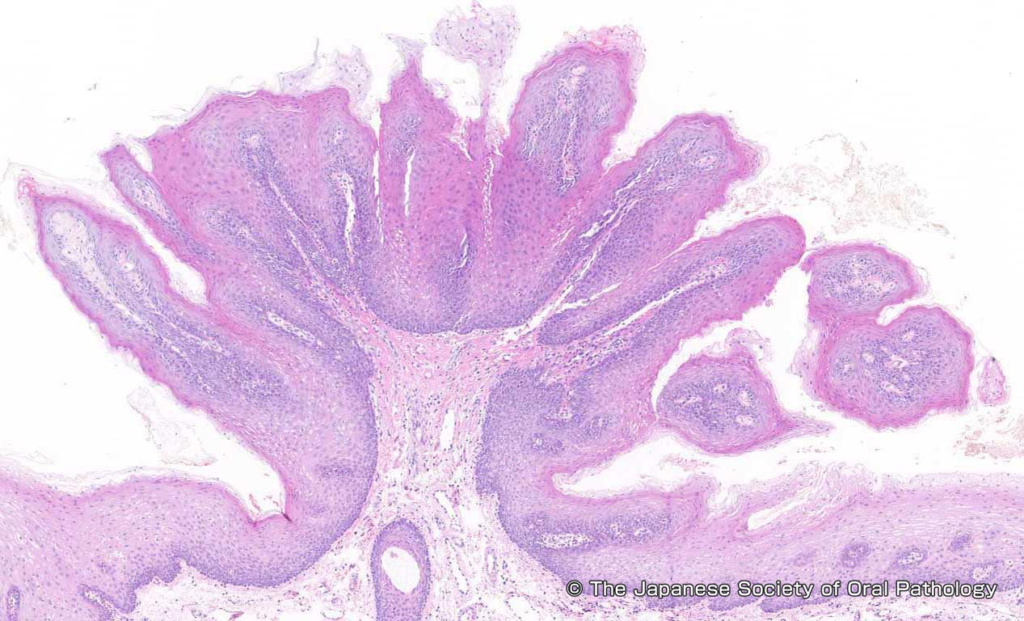
乳頭腫はヒトパピローマウイルス(Human Papilloma Virus: HPV)の感染に関連するとされる
腸上皮化生
LCIでのラベンダー色粘膜=腸上皮化生と考えてよい
非拡大 NBI での腸上皮化生診断能は感度 69%,特異度 91%で,拡大観察を併用することで感度 84%まで上昇
京都分類では体部まで腸上皮化生があればIM2とする、IEEでの評価はWLIでの評価と区別して記載する
- 観察法と所見
→①https://www.jstage.jst.go.jp/article/gee/59/4/59_465/_pdf/-char/ja
②https://www.jstage.jst.go.jp/article/gee/61/11/61_2445/_pdf/-char/ja- WLI(白色光):観察できるのは限定的な所見のみ→特異型腸上皮化生(白色隆起)と除菌後の地図状発赤のみ
- IEE(NBIorBLI&LCI):
- LBC(Light Blue Crest):NBIやBLI
- 腸上皮化生の診断能は感度 89%,特異度 93%
- LBC は拡大内視鏡観察による所見であるが,非拡大 NBI 観察でも腸上皮化生は青白色調の斑状領域として認識され化生部と非化生部には色調差を生じる
- WOS(White opaque substance):NBIやBLI
- 腫瘍や腸上皮化生の上皮内に観察光を透過させない白色の物質(=脂肪滴)が存在し,上皮下の微小血管像が透見できない現象
- 萎縮やPPI投与など胃内pHが高い状態でないと観察できない(→除菌後には観察できなくなる)
- 腸上皮化生に対する診断能は,感度 50%,特異度 100%,正診率 70%であり,さらに WOS と LBC を組み合わせることで,感度 87.5%,特異度 93.8 %,正診率 90%と診断能の向上を認めた
- ×MTB(Marginal turbid band):NBIやBLI
- 腸上皮化生の腺窩辺縁上皮は化生のない腺窩辺縁上皮と比較して,白濁して観察される
- MTB の視覚化される機序は,腺管と腺管の間,すなわち窩間部が拡大・短縮するため
- LBC を伴わない早期の腸上皮化生にも出現する
- 腸上皮化生に対する診断能は感度 100%,特異度 66%,正診率 82%
- ◎ラベンダー色の粘膜:LCI
- ラベンダー色=腸上皮化生と考えてよい
- 特異型、非特異型いずれの腸上皮化生にも適応される
- LCI で腸上皮化生がラベンダー色に観察されるのはNBI や BLI で青白色斑として観察されるのと同様
- ミンクリア散布するとラベンダー色がより鮮明となる
- ◎foveola type(腺窩型)と groove type(腺溝型):
- foveola type は萎縮・腸上皮化生のない固有腺の円型の腺開口部を反映
- Groove type は萎縮・腸上皮 化生を認める腺管の溝状の腺開口部を反映→腸上皮化生の頻度が高い
- LBC(Light Blue Crest):NBIやBLI





潰瘍とびらんの鑑別
- 本来は病理学的に行う
- びらん:粘膜欠損が粘膜筋板までにとどまる
- 潰瘍:粘膜欠損が粘膜筋板断裂し、粘膜下層に達する
- 内視鏡的には潰瘍(=粘膜筋板の断裂)はひだ集中を伴うと判定している
SPHG(Stomal polypoid hypertrophic gastritis)
- 残胃吻合部近傍に発生するポリープ状隆起のこと
- Gastritis cystica polyposa (GCP)ともいう
- 胃癌の発生母地と考えられている
食道アカラシア
- esophageal rosetteまたはGingko-leaf sign【=イチョウの葉】
下部消化管内視鏡
CSPとCFP(対義語はHSP、hot snare polypectomy)
- cold polypectomy の適応は内視鏡的にがんを疑わない 10 mm 未満の病変
- CFP は 3 mm 以下の病変に施行することが望ましい
- CSP では細いワイアの専用スネアを使用したほうが高い完全切除割合を得られる
- 3 mm 以下の病変に限れば CSP と CFP の切除能は同等である可能性が高い
- コールドスネアポリペクトミーガイドライン
- 適応病変:腺腫と術前診断された 10 mm 未満の病変に限定することが推奨される
- デバイス:10㎜/13㎜、ラウンド型/6角形がある
- CSP による 4 ~ 9 mmのポリープ完全切除割合は HSP に劣らない(98.2% vs. 97.4%)
- 10 mm 以上のポリープにおいて,CSPは一括切除および断端陰性の割合が低く推奨されない
- CSPとEMRを比較したRCTにおいて6~9mmでの不完全切除割合は EMR(1.5%)よりも CSP(8.5%)で有意に高く、CSPの適応は腺腫に限定し,完全一括切除が望ましいがんを疑う病変ではEMRを選択すべきである
- 5 mm以下と7mm以下のポリープのいずれにおいてもCFPよりCSPは完全切除割合が高くcold polypectomyとしてはCSPを推奨する
- 3 mm 以下のポリープであれば CFPも許容されるがその際は,生検鉗子よりもカップ径の大きいジャンボ鉗子を用いる
- 通電を伴う内視鏡切除における偶発症の発生頻度は,ポリペクトミーと EMR で,それぞれ術中穿孔率 0.02~0.05%,0.09~0.58%,後出血率 1.1~1.3%,1.4%と報告されている
- 抗血栓薬内服継続下の小病変(10 mm 未満)に対して cold polypectomy は,抗血栓薬の中止による血栓症リスクや,ヘパリン置換術により生じる後出血リスクを回避する可能性はあるが,現時点のエビデンスレベルは十分ではない
- CSP で切除される粘膜筋板は一部分のみであり,粘膜筋板まですべて切除することは困難→CSPでは深達度診断、深部断端および粘膜下層浸潤の評価が困難なため、癌治療には不適切な治療法である
- 側方断端に関しても陽性/不明となる割合は CSPで EMRより高い(EMR:38% vs CSP:57%)。ただし,側方断端陽性/不明 67.1%に対して,実際に切除部位の追加 EMR 検体内に腫瘍遺残を認めたのは 3.9%のみと乖離が認められており,側方断端のみで腫瘍遺残を評価することも困難
- 病変の組織学的質的診断は同等もしくは優れていると考えられるが,断端診断は劣ることが多い(EMR検体は標本を引き延ばした状態でホルマリン固定する影響もあるし、熱変性がないため断端が不明瞭という影響もある)
EMR
- カットのときは、スネアをほどよくしめあげないといつまで通電しても切れないし締めすぎると生焼けでちぎれる
- 1回の通電時間は0.3~0.5秒と極力短時間にしないと熱損傷する
- 大きいポリープは1回取り出してもう一度挿入する
- スネアはポリープサイズに応じて選択する、大きめの場合は20㎜スネアを使用
留置スネア(ディスポーザブル結紮装置:オリンパス)

- 適応:茎長が1.5~2㎝程度ほしいところ、それ以下ではEMRがベター
- 留置スネアから5㎜くらいのところでスネアで切離(凝固でなくカット、1発でバッサリと)→留置スネアが熱で溶けないように!!!腫瘍側も5㎜mくらいのマージンがとれるように!
- 局注は不要!留置スネアが抜けないようにクリッピング追加する場合もある
抗凝固と内視鏡
薬の種類に限らず、1剤のみの場合は生検可能(DOACでも抗血小板でもOK!)
2剤以上の場合は、生検の可否は個々の症例で判断、治療内視鏡は休薬が必要

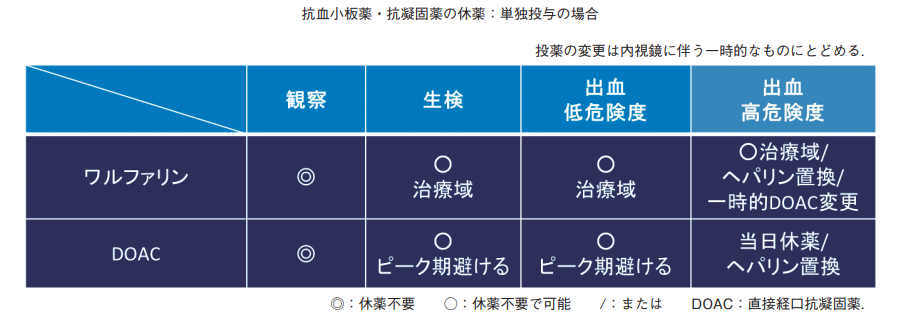
- 抗血栓薬服用者に対する消化器内視鏡診療ガイドライン2012:日本消化器内視鏡学会
- DOACを含めた抗凝固薬に関する追補2017:日本消化器内視鏡学会
- 生検では抗血栓薬服薬の有無に関わらず,胃では 0.002%,大腸では 0.09% に出血が合併する
- 出血低危険度:生検、マーキング(点墨、クリップ)、ステント留置、内視鏡的乳頭バルーン拡張
- 出血高危険度:ポリペク、EMR、ESD、EST、PEG、バルーン拡張、など
- 低危険度手技での出血率は抗凝固なし0.32%、抗凝固あり1.67%
- 高危険度手技での出血率は抗凝固なし1.39%、抗凝固あり4.80%(うち重篤4.24%)
- ポリペクのうち、コールドポリペク(CFP/CSP)はHSPよりも出血低リスク(CFPは生検と同程度)だが、明確な推奨はまだ存在しない
ピロリ菌感染症
- 2009年1月に日本ヘリコバクター学会から「H. pylori感染の診断と治療のガイドライン2009改訂版」が発表
- 2013年より「H. pylori感染胃炎」に対する除菌治療が新たに保険収載
- 除菌を行う際にはGSよる胃癌の除外の他,pylori感染の有無と胃炎の評価を行う
- 除菌治療の普及により現感染者は内視鏡検査対象者の10%程度にまで低下
- ピロリ菌陽性者の生涯胃癌罹患率は男性17%、女性7.7%と高い →Kawai et al:Int J Cancer 150:18-27,2022
- ピロリ菌感染が成立するのは胃酸分泌が未熟な小児期(ほぼ5歳まで)のみとされる
- 治療:
1次除菌はボノサップ、2次除菌はボノピオンが除菌効果高い(従来70%の一次除菌率→90%) - 関連疾患:胃癌,胃潰瘍,十二指腸潰瘍, 低悪性度胃MALTリンパ腫,胃過形成性ポリープやITP,貧血など
- 鑑別:その他の胃炎:自己免疫性胃炎(1%)、NHPH胃炎(1~3%)、好酸球性胃炎(0.02%)
- 検査:
2021年、ヘリコバクター学会→抗体検査ではなく現感染を確認できる検査を推奨している(UBTや便中抗原、RUT)
便中抗原検査はPPI中止しなくても可能だが、保険診療ではPPI中止が算定要件になるためPPI休薬が必要
内視鏡で胃炎がある場合には、ピロリ菌の検査は2つの方法で確認する方がよい
バリウム検査でもピロリ菌の感染診断が90%の精度で可能らしい(GSより優れているって本当か?)
2022年11月より、CAM耐性遺伝子検査が保険診療で測定可能となった - ピロリ菌の検査・治療にはGSおよび胃潰瘍、胃炎、十二指腸潰瘍の保険病名が必須!!!
- UBTによる除菌後効果判定:
- ガイドライン上は除菌終了後4週間以上あけて(除菌不成功の場合30日で95%が菌数回復)、一般的には8-10週間後が推奨されている
- 2週間前からPPI、P-CABの休薬が必要
- 感度97.7~100%、特異度97.9~100%と、ともに高い検査
- カットオフの数値は2.5‰(パーミル)
- PPI使用により閉経後女性の大腿骨頸部骨折のリスクが35%増大し、喫煙歴がある場合は50%以上高くなる
- 病理学的変化:胃底腺の嚢胞状拡張、壁細胞の過形成・空洞化による内腔突出といった変化
- 内視鏡的変化:胃底腺ポリープの増大、多発性白色扁平隆起、過形成ポリープ、敷石状粘膜、ひび割れ粘膜
10 U/ml未満は陰性の判定になるが、3〜10 U/ml未満となった方の10〜40%にピロリ菌が棲息する感染者が存在していることがわかっている。胃癌発症リスクはピロリ菌抗体価が陰性の人と比較して、陰性高値では2.8倍、陽性では6.5倍、統計学的に有意に高いとする研究データもあるが、最も大きなリスク因子は萎縮性胃炎の程度であった。
- 3 U/ml未満 陰性(未感染)
- 3〜10 U/ml未満 陰性高値→判定要注意!!既感染、現感染の可能性あり 他の方法で再検査を
- 10 U/ml以上 陽性(現感染)
人間ドック、健康診断によっては血清抗体検査が3 U/ml以上を陽性として説明されている場合もある。ピロリ菌感染によって胃粘膜萎縮が高度になると、ピロリ菌が棲息できなくなりピロリ菌検査で陰性となることがあり、胃癌の最高リスクと考えられている。
- ピロリ菌除菌の胃がん罹患に対する相対リスクを推計する19件のメタ・アナリシスを行ったところ、非除菌群に比べ、除菌群では胃がん罹患リスクは0.42(95%信頼区間;0.35-0.51)と有意な低下が見られた。
- 胃がんに罹患したことのない人(健常人)を対象とした10件の観察疫学研究のメタ・アナリシスでは、ピロリ菌除菌群における胃がん罹患リスクは0.34(95%CI:0.25-0.46)と有意な低下が認められた。
- 内視鏡的切除を受けた早期胃がん患者を対象とした9件の研究に限定したメタ・アナリシスにおいても、除菌群は異時性(複数の腫瘍あるいは病変で、初発腫瘍と後発腫瘍の間隔が2か月を超える場合)の胃がん罹患リスクが0.50(95%CI:0.39-0.66)となり、内視鏡的切除後の早期胃がん患者でも除菌により異時性胃がん罹患リスクが低下した。
Asaka.M.et al:Hericobacter15;486-490.2010に掲載された論文
→29歳までに除菌した場合、99.9%胃がんを抑制する効果がある
49歳までの場合は92%
59歳までの場合は76%
69歳までの場合は49%と年齢とともに低下していく。
できるだけ早い(30歳までに)除菌が理想だが、50歳でも遅いという事はない(→禁煙と一緒)。
後期高齢者に対する除菌療法の考え方は?
→除菌療法は胃癌リスクの低減だけではなく(高齢者の場合はその恩恵を享受する前に死亡する可能性が高い)、潰瘍やその他の疾患、消化器不定愁訴とも関連するため、何歳からでも除菌療法は適応と考えてよいだろう。
NHPHとして、H.suisをはじめ、H. heilmannii や H. ailurogastricus などが知られている
日本では、 ヒト胃に感染する NHPH のうち、菌種が同定できた 27 症例中 20 症例(74%)が H. suis、7 症例(26%) が H. heilmannii あるいは H. ailurogastricus であることが報告されている
H. suis などの NHPH 感染はピロリ菌除菌後の患者でも認められることが報告されている
NHPH 感染はピロリ菌とは異なり、全世代におい て感染リスクがある可能性を考慮する必要がある
H. suis が培養できるように なったことにより、今後 H. suis をはじめとする NHPH 感染症の感染経路の解明や、ピロリ菌との 感染病態の違いを明らかにする基礎研究が推進していくことが期待される
【ヘリコバクター・スイス感染症】
【菌体】大型らせん状菌(ピロリ菌より大型で強いねじれ)
【宿主】ブタなどの動物、ヒト。養豚の半数以上が感染
【感染経路】ヒトへの感染経路は不明
【疫学】感染率0.5%以下。ピロリ菌との重複感染6.5%
【病原性】急性胃粘膜病変、胃炎、鳥肌胃炎、胃潰瘍、MALTリンパ腫、胃癌
【内視鏡所見】前庭部の萎縮性胃炎、霜降り状(white marbled appearance)、ひび割れ状粘膜。
【検査・診断】鏡検(ギムザ染色)、培養、 PCR、抗体検査
【治療】ピロリ菌に準じる
ERC
- WGC:wire-guided cannulation
造影剤の試験注入を行わずに Guidewireを用いて胆管深部挿管を行う方法。
WGCは,Guidewireを Preloadしておいた Sphincterotomeで十二指腸乳頭へのアプローチを行い,Sphincterotomeの刃の調整により胆管方向へ Guidewireを先進させて Cannulationする方法。
ERCP後膵炎の減少が期待され汎用される。
ヒスタミン食中毒
- ヒスタミンを多く含む食品を食べた直後~1時間程度で生じる
- 症状は顔面紅潮、頭痛、吐き気、じんましん等のアレルギー様症状
- 主な原因食品はサバ、マグロ、イワシ等の赤身の魚
- ヒスチジンというアミノ酸を多く含む食品を室温等の不適切な温度で保存した場合に、食品に付着したモルガン菌等のヒスタミン産生菌によってヒスタミンが産生される
- ヒスタミンは加熱しても分解されず、無味無臭
ヒスタミンは1種類しかないが、ヒスタミン受容体はH1 受容体,H2 受容体,H3 受容体,および H4 受容体の4種類ある。それぞれ発現部位が異なり、アンタゴニストも異なる。H1 受容体は,主に,血管内皮細胞,平滑筋,副腎髄質細胞,神経細胞に分布している。H2 受容体は,消化管,心臓,神経細胞などに分布している。
機能性消化管疾患 -総論-
- 消化器症状があるにも拘らず、内視鏡検査などで器質的異常を認めないもの
- 機能性消化管疾患診療ガイドライン2021(オンライン版あり)
- IBS
- 機能性ディスペプシア
- GERD診療ガイドライン2021
食道胃逆流症GERD→2つに大別、4つに細分類された
- びらん性GERD(30~40%)と非びらん性GERD(60~70%)に分類される
- 2016年のRomeIVで4疾患に分類された(広義のNERDが3つに細分類された)
→診断のためには食道インピーダンス・pH検査が必要で現実的な診断分類ではない - NERD(非びらん性GERDと同義):
- 病的な酸逆流を認める症例ではPPIが有効
- 逆流性知覚過敏:症状と逆流との関連が見られる
- 機能性胸やけ:病的な逆流がなく症状と逆流の関連がない、胸やけを起こす原因不明の病気=精神科寄り
- 食道知覚過敏には、ストレスによる自律神経の乱れが大きく影響している
- 実臨床ではQUESTやFスケール、改定Fスケールなどの問診表を用いて予診をとる
- ロサンゼルス分類はGERDではなく、逆流性食道炎の分類
- 治療(2021年GERDガイドライン3版で症状別の詳細な推奨が出た)
- 重症逆流性食道炎→タケキャブ20mgを4週間→長期投与はタケキャブ10㎎(重症の場合内服中止すると再燃が多い)
- 軽症逆流性食道炎→PPIとタケキャブは同等、長期投与はPPI>タケキャブを優先
- 非薬物療法として減量、禁煙、早めの夕食摂取、就寝時の頭位挙上を推奨
- NERD治療→上記治療+六君子湯の上乗せ
- 逆流性知覚過敏症・機能性胸やけでは酸逆流の関与が乏しくPPI等は無効→三環系やSSRIが検討される
- 日常生活の留意点:GERDの発症には生活環境も影響する。腹部の締め付け、重いものを持つ、前かがみになる、右側を下にして寝る、肥満、喫煙などは逆流を防ぐ機能を低下させるといわれている。また、食べ過ぎ、香辛料など刺激の強いもの、寝る前の食事、脂肪を多く含んだもの、柑橘類、多量のアルコール、炭酸飲料、喫煙などは影響を及ぼしやすいといわれている。
- カルシウム拮抗薬もLES圧を低下させ逆流を増悪させるといわれている
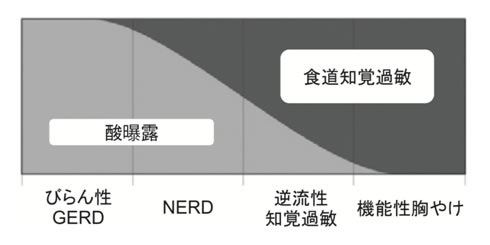
一般に寝るときの姿勢で逆流を減少させることが証明されているのは、枕を少し高くしたり、ベッドを少し起こして頭を高くして寝る姿勢。
横向き派の人の場合には、左側を下にし、横向きで寝ると良いといわれている。 睡眠姿勢が右側臥位の者では食道での酸曝露時間が長いという研究結果による。理由としては、左側を下にしたほうが下部食道括約筋への圧が低下するため、胃酸が逆流しにくいとされている。たしかにバレット癌も右側に好発する。
→頻用薬・処方カスケードのページ参照
機能性ディスペプシア:FD
- 症状:4大症状として食後の胃もたれ、早期満腹感、みぞおちの痛み、みぞおちの焼ける感覚
- 内視鏡的にはFD疑いの患者の91.2%で対応病変がない→内視鏡検査は除外診断であって確定診断には不要
- 日本人の FD の有病率は,健診受診者の 11%~17%、欧州で 11.0~23.8%,米国で 15%
- 病院受診者を対象とした FD の有病率は,上腹部症状を訴えて病院受診した患者の 45~53%
- 2013年にH.pilori感染胃炎、機能性ディスペプシア(FD)の保険病名が追加
- 2021年『機能性ディスペプシア診療ガイドライン2021』、日本消化器病学会
- 日本の定義:症状の原因となる器質的,全身性,代謝性疾患がないのにもかかわらず,慢性的に心窩部痛や胃もたれなどの心窩部を中心とする腹部症状を呈する疾患(症状の詳細は問わずRomeIV基準より広い)
- 世界の定義(2016年RomeIV基準):症状を説明できそうな器質的,全身性,代謝性疾患がないにもかかわらず,食後膨満感,早期満腹感,心窩部痛,心窩部灼熱感の 4 つの症状のうち 1 つ以上を有するもので,6 ヵ月以上前にこれらの症状を経験し,しかもこの 3 ヵ月間この症状が続いているもの。4 つの症状のうち,前二者を有するものを PDS(postprandial distress syndrome;食後愁訴症候群),後二者を有するものを EPS(epigastric pain syndrome;心窩部痛症候群)と呼んでいる。
- H. pylori 感染を伴うディスペプシア患者は,FD ではなく H. pylori 関連ディスペプシア(Helicobacter pylori-associated dyspepsia:HpD)として取り扱う→除菌後に症状軽快した場合などにHpDと診断する
- 治療:
- 治療目標は患者の満足度を高めることだが、FD発症は多因子性で薬物有効性は50%とされる(効果判定は4-8週間)
- FDではプラセボ効果が大きい(5~90%、平均56%で奏功した)、医師患者関係も重要
- 生活習慣の改善:(満腹まで食べない,高脂肪食を避ける,禁煙指導を行う,飲酒・コーヒー摂取を避ける)
- H2受容体ブロッカー(H2RA)やプロトポンプ阻害薬(PPI)は有用であり,使用することを推奨する
- タケキャブの推奨度は弱→H2RAやPPIが優先される(推奨度:強)
- 消化管運動機能改善薬(機能性消化管疾患の治療薬として開発された薬剤)が有効
アセチルコリンエステラーゼ(AChE)阻害薬>ドパミン受容体拮抗薬>セロトニン 5-HT4 受容体作動薬
アセチルコリンエステラーゼ(AChE)阻害薬:アコチアミド(アコファイド)、推奨度:強
ドパミン受容体拮抗薬:メトクロプラミド,ドンペリドン,スルピリド,イトプリド、推奨度:弱
ドパミン受容体拮抗薬は有害事象の懸念から長期投与しない
セロトニン 5-HT4 受容体作動薬:モサプリド(ガスモチン), テプレノン,tegaserod、推奨度:弱 - 六君子湯は有用であり,使用可能、ガイドラインの推奨度:弱
- 三環系抗うつ薬と抗不安薬も推奨度:弱で使用可能
- 非薬物療法:禁煙、睡眠、心療内科での認知行動療法
※注意※FDという保険病名ではPPIやアコファイドを除く消化管運動機能改善薬を使用することは出来ない
- 治療抵抗性の FD 患者における治療変更時期の目安はおおよそ 4~8 週間
- 過敏性腸症候群(併存率66.9%),胃食道逆流症,機能性便秘,および不安障害などは FD と併存しやすい
- 保険診療に関すること
- FD診断前にはGSが必須(1-2年以内)
- FDと慢性胃炎、FDと逆流性食道炎の病名併記は可能
- 8つの生薬(人参、半夏、茯苓、白朮、大棗、陳皮、甘草、生姜)配合
- グレリン(食欲をコントロールするホルモンの1つで、摂食促進、消化管運動促進、胃酸分泌促進などのさまざまな作用をもつ)の作用を増強させる


喉頭癌
- 頭頚部癌の中で最も頻度が高く、約3000人/年が罹患する
- 男女比は9対1で、50歳以上の男性に多い
- 声門(声帯)に発生するがんが60~65%を占め、声門上は30~35%で、声門下は極めて少なく1~2%
咽頭癌
- 上咽頭癌で約800人、中咽頭癌で約1,800人、下咽頭癌で約1,900人といずれもまれな疾患(大腸癌は16万人/年)
- 経口挿入で観察できるのは中咽頭以下(上咽頭は鼻腔のレベル)
- 舌根や扁桃は中咽頭にはいる
- 下咽頭癌発癌部位の頻度は梨状陥凹60-70%、輪状後部20%、後壁10%の順
白板症
- 口腔粘膜、とくに頬粘膜や舌、ときには歯肉にみられる白い病変で、こすっても剥離しないもの。病理学的な診断基準はなく、臨床的あるいは病理学的に他のいかなる疾患の特徴も有しない白色の板状ないし斑状の病変を白板症といい、組織学的な異形成の有無に関係なくこの名称を用いることにし、現在はこの定義づけに従っている。
- 有病率は2~3%程度とされ、とくに舌にできたものは悪性化する可能性が高いため、前がん病変(口腔潜在的悪性疾患の代表的なものとされています。びらん(粘膜の浅い欠損)をともなうこともあり、ものが当たると痛かったり(接触痛)、食べ物がしみたりします。
- 喫煙やアルコールによる刺激、義歯などによる慢性の機械的刺激、ビタミンAやBの不足、さらに加齢や体質なども関係するといわれています。
紅板症
- 紅色肥厚症(こうしょくひこうしょう)ともいわれ、舌、歯肉、その他の口腔粘膜に発生します。鮮紅色でビロード状、表面は平滑な病変です。境界は明瞭なものが多くみられます。初発症状として多くの症例で刺激痛が認められます。一般的に50歳代以上の高齢者が全体の80%を占めています。
- 紅板症の50%前後が悪性化するといわれています。
- 治療は外科的切除
再発性アフタ
- アフタは直径数ミリ大の円形の浅い潰瘍で、潰瘍の表面は灰白色~黄白色の偽膜で覆われ、潰瘍の周囲は赤くなっています。食物や歯ブラシなどがちょっと触れただけもズキッとした強い痛みを覚えます。また刺激性の食物や熱いもの、塩辛いものがしみたりします。アフタは何もしなくても1~2週間で治ります。アフタが再発を繰り返す場合に再発性アフタといいます。 なお、慢性再発性アフタはベーチェット病の一症状として生じることもあります。
- 原因は不明です。機械的刺激、遺伝性、極端な疲労、ストレス、あるいは片寄った栄養摂取などいろいろな要素が絡み合って発症するといわれます。ベーチェット病では遺伝的素因が注目されています。
- 鑑別疾患:
- ヘルペス性口内炎:単純性ヘルペスウィルスによる初感染で、疱疹性歯肉口内炎(ほうしんせいしにくこうないえん)ともいわれます。一般には無症状の感染(不顕性感染 ふけんせいかんせん)ですが、数パーセントが顕性感染(けんせいかんせん)としてヘルペス性口内炎の形をとります。大半が小児にみられますが、近年では核家族化に伴い大人にもみられます。
- 帯状疱疹
- ヘルパンギーナ:エンテロウイルス属、流行性のものは特にA群コクサッキーウイルスによる感染で軟口蓋から口峡部に発赤および多数の小水疱を認め、小水疱は破れて小アフタとなります。ヘルペス性口内炎が口腔の前方に症状を呈すのに対して、これは口腔の後方と咽頭での発症が特徴です。夏に流行しやすく、小児にみられることが多いのですが、まれに大人にも発症します。
- 手足口病:コクサッキーA16、あるいはエンテロウイルス71などによる感染で、口腔内の小水疱が破れてアフタ様病変となることに加え、手足の小水疱を特徴とするウイルス感染症です。
バレット食道
バレット食道の治療は、バレット食道をこれ以上広げず、食道がんを予防すること。
PPIがバレット食道癌のPPIの発癌抑制効果はほぼ確実。
とくにLSBEの方、逆流性食道炎の症状も頻繁にみられる方、内視鏡でのびらんが強い方には定期的なPPIの内服が推奨される。
- バレット食道からの発癌リスクは年率でLSBE0.4%、SSBE0.19%
- 逆流性食道炎がバレット食道の原因であり、プロトンポンプ阻害薬(PPIやP-CAB)などの胃酸を抑える薬を服用しながら、経過観察が一般的
咽頭乳頭腫・食道乳頭腫
- 食道良性腫瘍の8%を占める
- 内視鏡所見:無茎性ないし有茎性の隆起を形成し表面は穎粒状あるいは平滑で白色調
- 病理:重層平上皮の乳頭増殖からなり細胞異型を認めることは稀
- HPV感染との因果関係は否定的
- 治療はPPIやヨクイニンが奏功する可能性がある(→HPV感染症とされる尋常性疣贅に有効)
十二指腸腫瘍性病変
- 十二指腸は小腸の一部であり,空腸や回腸と同様の小腸型粘膜上皮に被覆されているが,前胃に相当する乳頭部あたりまでは,ブルンネル腺という特異的な構造があり,胃型の細胞もしばしば出現する.このことを知っておけば,十二指腸非乳頭部上皮性腫瘍の成り立ちが理解しやすいと思う.さらに,乳頭部では胆道系の上皮が腫瘍の発生母地の一員に加わるのである.
→十二指腸病変は多彩な背景母地があり、その病理診断も複雑であることから内視鏡診断は困難→あやしいものは必ず生検する!!!
大腸がん検診(便潜血検査:FOBT、fecal occult blood test)
便潜血検査では
早期がんの約50%、進行がんの約20%が偽陰性となる
LGAは健診精査CSの約30%(170/500例)に見つかる
→毎年受けることが重要
- アメリカのデータでは、逐年検診で32%、隔年検診で22%の死亡率減少効果が示されている
- TCSによるスクリーニングは、現在RCTが進行中である
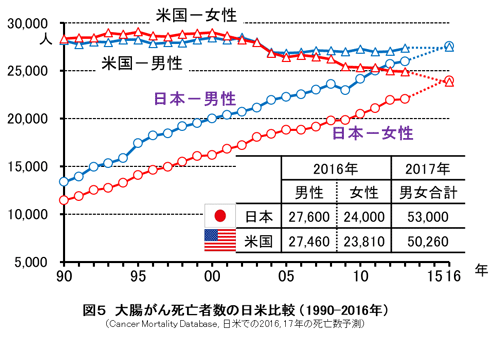
- 男女合わせると、大腸がんはがん全体の中で死亡率2位、罹患率は1位(約16万人/年)
- 毎年約5万人が大腸がんで死亡→アメリカよりも日本の大腸がん死者数が多い(検診受診率の差)
- 化学法については複数の RCT により,免疫法単独については 1 件の症例対照研究により,免疫法+化学法については複数の症例対照研究により死亡率減少効果があることが示されている
- 大腸癌死亡率および罹患率が 40 歳代から上昇することから,大腸がん検診は 40 歳から開始する
- 化学法:偽陽性が多く食事制限も必要なため現在は行わない
- 免疫法(FIT):食事制限不要で化学法よりもはるかに感度が高く,特異度はやや低い程度で遜色なく広く用いられる。糞便中のヒトの血液を 100ng/㎖(1㎖中に 1,000万分の1グラム)以上のレベルで検出する
- 一般集団における陽性率は約6%であり、陽性者のうちで、がんは2~4%、つまり便潜血陽性者 30 人に 1 人程度が大腸がんの確率であると言われている。また、偽陰性率(陰性であってもがんである確率)の問題があり、2回法でも進行がんで5~10%の偽陰性の報告がある。
→統計的には600人が検査受けると30人が陽性となり1人の大腸癌が見つかることになる - FIT1日法、2日法、3日法で大腸癌に対する感度が、それぞれ56%、83%、89%であり、1日法と2・3日法で有意差がみられた。特異度はそれぞれ97%、96%、94%で3日法が1・2日法より有意に低かった→感度・特異度のバランスを考慮して 2日法が好ましいとしている
- 特異度96%→偽陽性が4%→10000人検査すると400人が偽陽性で精検にまわり、精検受診者のうち真の陽性者は検診受診者24人に1人程度

- 日本の大腸がん検診受診者数は253万7352人、うち精密検査が必要と判定された人(要精検者)は15万4004人(要精検率6.07%)、精密検査を実際に受診した人(精検受診者)は10万5826人(精検受診率68.7%)(2017年度、日本対がん協会調査)
- 米国での大腸内視鏡検査は数十万円かかり、米国では50歳を過ぎた国民に大腸内視鏡検査を無償で1回提供している→大腸がん検診受診率は約70%と高い一方、日本の検診受診率は約20~40%と低いうえにFOBT陽性でも約60%の人しか精査を受けていない

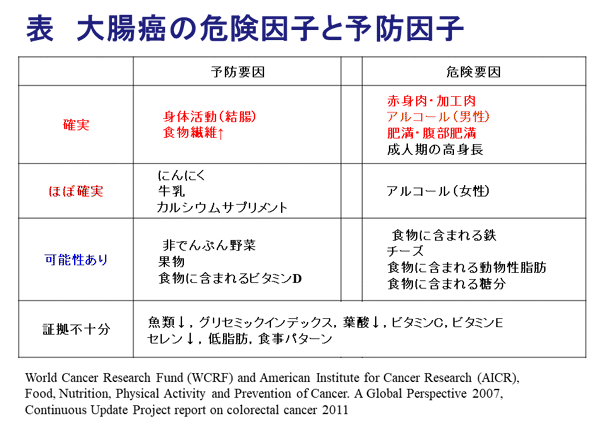
大腸ポリープ
- 大腸ポリープ診療ガイドライン2020年(日本消化器病学会)
→2020年に改定された大腸ポリープガイドラインでは、「発見した大腸腺腫は大きさにかかわらず、将来の癌への進展予防を目的として内視鏡切除を弱く推奨する」とされた - 大腸内視鏡スクリーニングとサーベイランスガイドライン2020年(日本消化器内視鏡学会)
- National Polyp Studyという米国の大腸ポリープ切除に関する研究では、径1~5mm では2%,6~10mm では5%,11~15mm では10%,16~20mm では12%,21~25mm では20%,26~30mm では18%の高異型度腺腫率
- 2 回大腸内視鏡検査を行った症例をもとに,先に行った大腸内視鏡検査での大腸腺腫の見逃し率をみた研究では,径 10 mm 以上で 2.1%,径 5~10 mm で 13%,径 1~5 mmで 26%の見逃しがあったと報告されている
- 再検査の期間:初回の十分なスクリーニング大腸内視鏡検査でポリープがなく,その後 10 年以内にフォローアップ内視鏡検査を実施した集団の径 9 mm を超えるポリープの罹患率(発見率)は,1~5 年後 3.1%,5~10 年後 3.7%であった.なお,前処置不良,盲腸まで未到達など初回が不完全な検査であった場合,1 年以内の再検査で 6.5%に径 9 mm 超のポリープを認めた.以上,欧米のデータからは,全大腸内視鏡検査は初回検査で病変がなければ,次回検査は 10 年後に実施することが可能と推定される.ただし,初回検査が不完全な検査であった場合は,1 年以内の再検査を考慮する.
- CSPの適応病変:10㎜未満の非有茎性腺腫だが、できれば5㎜未満が推奨される
- CFPの適応病変:3㎜未満
- SSA/P
- 右側結腸に好発、粘液付着していることが多い、癌化率は1.5~20%
- 10㎜以上は治療適応
- TSA
- 左側結腸に好発、発赤調
- 通常の腺腫と同様に扱う
大腸腫瘍内視鏡切除後のサーベイランス間隔
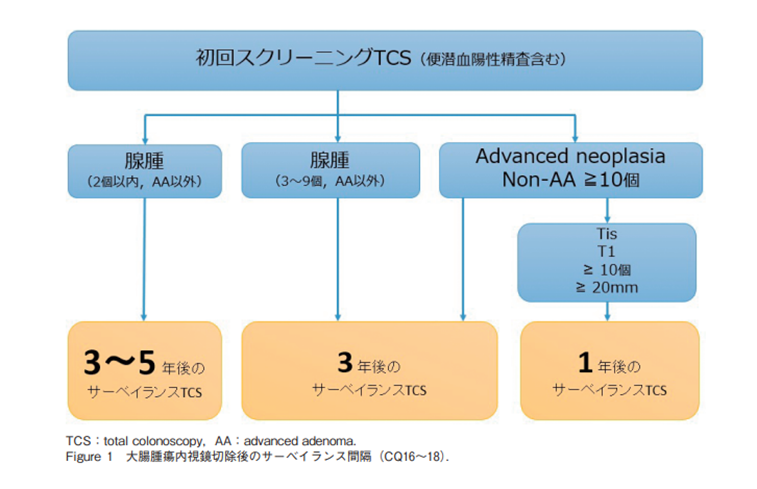
Advanced neoplasia:AA+浸潤癌

大腸鋸歯状病変はSP(serrated polyp)やserrated lesionと呼ばれ,腺管が鋸歯状の管腔構造を呈する病変である.現在のところ病理組織学的にHP(hyperplastic polyp),SSA/P(sessile serrated adenoma/polyp),TSA(traditional serrated adenoma)と3つのカテゴリーに分類することが提唱されている.
従来,大腸の鋸歯状腺管構造を有するポリープは病理組織学的に過形成性ポリープと診断され,非腫瘍性病変であり癌化の危険性はない病変と考えられていた.しかし近年,HPやSSA/Pを介した新しい大腸癌の発癌経路である“serrated pathway”が提唱されるようになり,特にSSA/Pとされる病変は右側結腸に発生する遺伝子不安定性(microsatellite instability ; MSI)陽性大腸癌の前駆病変とされ注目されている.しかしわが国におけるSSA/Pの診断基準はいまだコンセンサスが得られておらず,現在,大腸癌研究会プロジェクト研究において検証中である.またその内視鏡診断についても学会・研究会にて種々報告されている最中である.

- 米国消化器病学会の方針は?
→発見した全ての腺腫性ポリープを切除(=Clean colon)を目指すことが基本(Clean colon達成した場合には大腸癌による死亡率抑制効果が明らか)
“Resect and Discard strategy”というスタンスもある(医療コスト削減のため) - Resect and Discard strategyとは、切除した大腸ポリープを回収せずに、病理診断を省略する戦略ですが、全ての大腸ポリープに対して行うわけではなく本当に治療が必要なポリープで、かつ”がん”を疑わない場合にのみ、切除したポリープの病理診断を行わないという戦略のこと
- クリーン・コロン達成ののちのフォローアップ方法は?
→上述のガイドライン通り - 初回の大腸内視鏡検査でポリープがない場合のフォローアップは?
→FIT2回法要精査のため TCS を受けて腫瘍性病変を認めなかった場合には,TCS による経過観察ではなく,FIT を用いた大腸がん検診プログラムに戻ることが提案される(検診に戻るまで最大5年間の猶予が考慮できる)。本邦において初回スクリーニング法として TCS が導入された場合においても,腫瘍性病変がない場合には5 年後のスクリーニング TCS を考慮する(大腸内視鏡スクリーニングとサーベイランスガイドライン2020年より)
一方、欧米ガイドラインでは10年保証と明記されている(初回のスクリーニングの内視鏡検査でポリープの指摘がなく、その後10年以内にフォローアップとして内視鏡検査を実施した場合の9mm を超えるポリープの発見率は、1~5年後で3.1%,5~10年後で3.7%であった。初回の検査が不完全な検査であった場合(大腸が前処置できれいになりきらなかった場合など)には、1年以内の再検査で、6.5%の方に9mm 超のポリープを認めた。この結果より、欧米においては大腸内視鏡検査は初回検査で病変がなければ、次回検査は10年後に実施することが可能であるとガイドライン上明記されている)
TCS における挿入困難の予測因子は,高齢・女性・腹部/骨盤手術歴・低 BMI,前処置不良等である.
- CO2 送気は TCS の受容性向上に寄与する.
- 病変がない場合でも観察時間は 6 分以上を提案する.
- インジゴカルミン散布による色素観察,先端フードの使用は病変検出割合を有意に向上させる
- 拡大観察は大腸病変の質的診断に有用であり,スクリーニング大腸内視鏡検査を行う際に拡大内視
- 鏡の使用を提案する
IBD/炎症性腸疾患
- 新しいバイオマーカー(保険上、3か月以上のインターバルが必要)
- LRG(ロイシンリッチα2グリコプロテイン)
- 便カルプロテクチン
IBS/過敏性腸症候群
- 機能性消化管疾患診療ガイドライン2020
- 有病率は10%と言われている
- 機能性消化管疾患の診断基準:RomeIV(2016年版)
- 週に1回以上の腹痛が必須条件
- その腹痛が排便に関連し何度も繰り返され便秘や下痢を伴うことが必要
- 薬物治療:
過敏性腸症候群の治療薬としては、主に高分子重合体(ポリフル、コロネル)や消化管運動調節薬が用いられている。下痢型過敏性腸症候群では、基本的には、まず、高分子重合体や消化管運動調節薬(イリボー)を投与する。本剤は消化管腔内環境調整目的で、第一選択薬としてしばしば選択される。また、便秘型では高分子重合体に加えて、緩下剤(リンゼスなど)を併用することもある。
便秘症
- 慢性便秘症ガイドライン2017
- ブリストル便性状スケールで評価する
- 食物繊維を摂取するように指導する、食物繊維不足(極度の偏食など)による便秘にはポリフルが有効、ポリフルは下痢にも便秘にも有効性が期待できる
肝硬変
飯塚病院肝臓内科ホームページ(福岡県)参照https://aih-net.com/liver/medical/letter/backnumber.html
https://www.jstage.jst.go.jp/article/naika/111/1/111_58/_pdf
肝予備能評価スコア(CP、MELDS、ALBIなどの計算→日本肝臓学会HPより)https://www.g-station-plus.com/forpatient/hcv/score
総論
肝硬変診療ガイドライン2020(3rd、日本肝臓学会、日本消化器病学会)
定義:「肝臓全体に再生結節が形成され,再生結節を線維性隔壁が取り囲む病変」
肝臓の機能
- 栄養分の合成
- 栄養分の貯蔵と放出
- 胆汁の産生
- アンモニアの代謝
- アルコール・薬物・毒物の代謝
アンモニアは脳などへの毒性があり、発生すればすぐに処理して血中濃度を低く保たなくてはなりません。アンモニアの代謝経路は、肝臓の尿素回路と、筋肉や脳にあるグルタミン合成経路の 2 つですが、後者も結局はグルタミンで肝臓に運ばれて尿素回路に回って処理されるしくみになっている。
糖新生とは、運動時や飢餓時などのグルコース不足時に、ピルビン酸、乳酸や糖原性アミノ酸(アラニンなど、糖新生に使われる 10 数種のアミノ酸)など、糖質以外のものからグルコースを作ることで、糖新生にはグルコース 6 ホスファターゼという酵素が必須で糖新生は肝臓でしか行われない。
アミノ酸はアミノ基(-NH2)があるので、分解(異化)されていくと必ずアンモニア(NH3)が発生する。また運動時の筋肉では、エネルギー源の ATP が消費されるとアンモニアが発生する。アンモニアが発生した筋肉細胞のその場での処理としては、基本的に一旦はグルタミン酸にひっつけてグルタミンにして血流で肝臓に送り肝細胞に取り込まれたグルタミンの代謝に伴ってアンモニアが再度発生し、これが尿素回路で処理される。また消化管からは、消化吸収されたタンパク質からできたグルタミンが、やはり肝臓に流入して肝細胞内でアンモニアの源となるほか、ウレアーゼ産生菌が腸内の窒素源から産生したアンモニアも直接肝臓に流れ込み、やはり尿素回路で処理される。
肝硬変の肝臓では、原因肝疾患の進行にともなって、きちんと働ける肝細胞が減少することにより、処理できるアンモニアの量が低下していくと同時に、門脈大循環シャントにより肝臓への血流低下が血中アンモニア濃度を上昇させる。
便秘(アンモニアの産生と吸収が増える)、消化管出血(=アンモニア産生の原料となる)、脱水、感染症、アルコール
病態
肝硬変は,肝実質細胞の減少,線維化と構造改築による血流障害,門脈―大循環シャント形成等により,門脈圧亢進,腹水,肝性脳症,肺障害,心障害,腎障害,血清ナトリウム低下等を引き起こす.腸内細菌叢のdysbiosisや腸管透過性の亢進が生じ,肝性脳症や易感染性等と関連している.また,肝硬変では肝癌のリスクが極めて高く,注意が必要.
肝硬変は,肝機能が良く保たれ臨床症状がほとんどない代償性肝硬変と肝性脳症,黄疸,腹水,浮腫,出血傾向等肝不全に起因する症状が出現する非代償性肝硬変に分類される.
我が国の肝硬変の成因は,C型肝炎の比率が減少し,アルコール性や非アルコール性脂肪肝炎(non-alcoholic steatohepatitis:NASH) の 比率が増加している.
肝硬変の症状
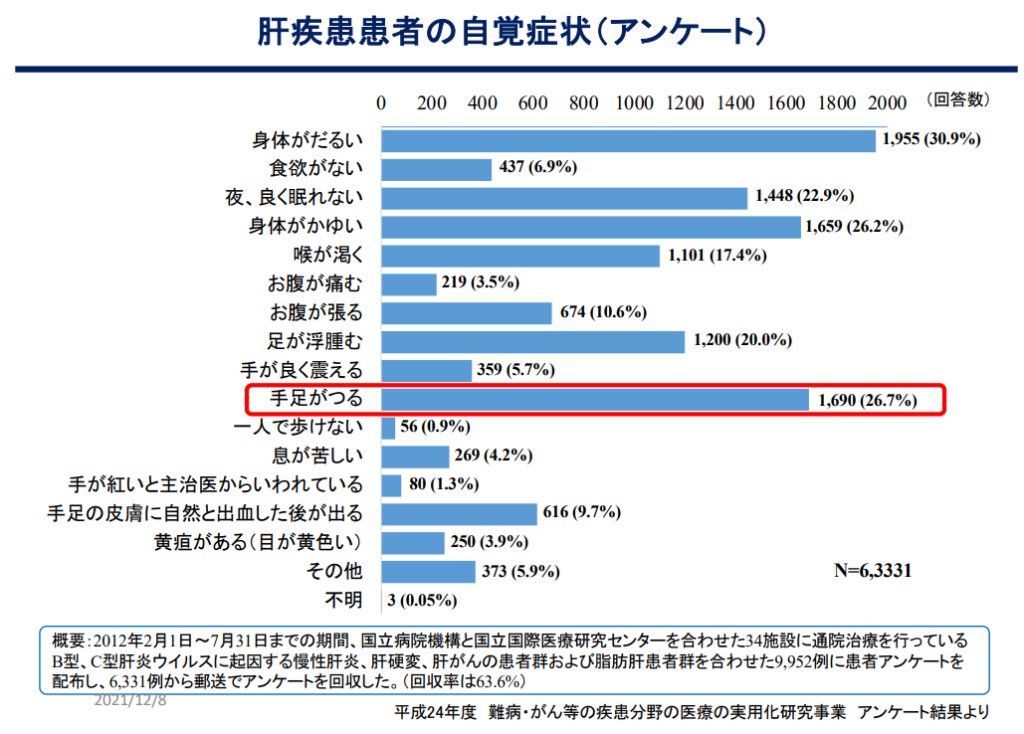
肝硬変の治療
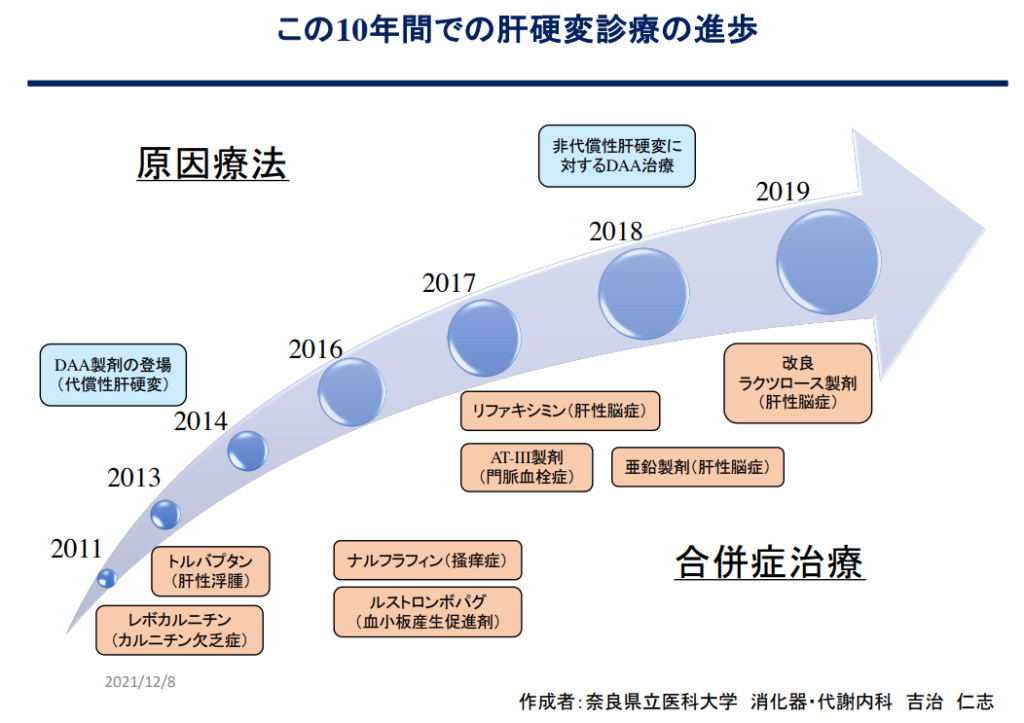
肝硬変患者の栄養指導
エネルギー摂取量
耐糖能異常がない場合 25~35 kcal/kg(標準体重)/日
蛋白質必要量
蛋白不耐症がない場合 1.0~1.5/g/kg/日を基本とする
飢餓状態を短くするために,約200kcal程度の就寝前軽食(late evening snack:LES)を含めた1日4~6回の分割食が推奨されている.
低アルブミン血症(血清アルブミン≦3.5 g/dl)を認め,経口食によって十分な蛋白質摂取ができない場合は,分岐鎖アミノ酸(branchedchain amino acid:BCAA)製剤の投与を考慮する.
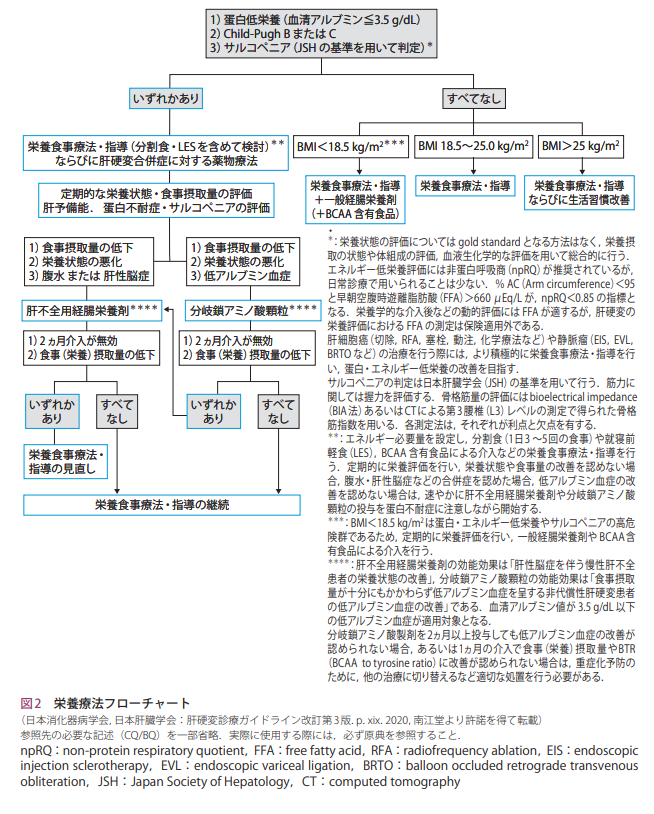
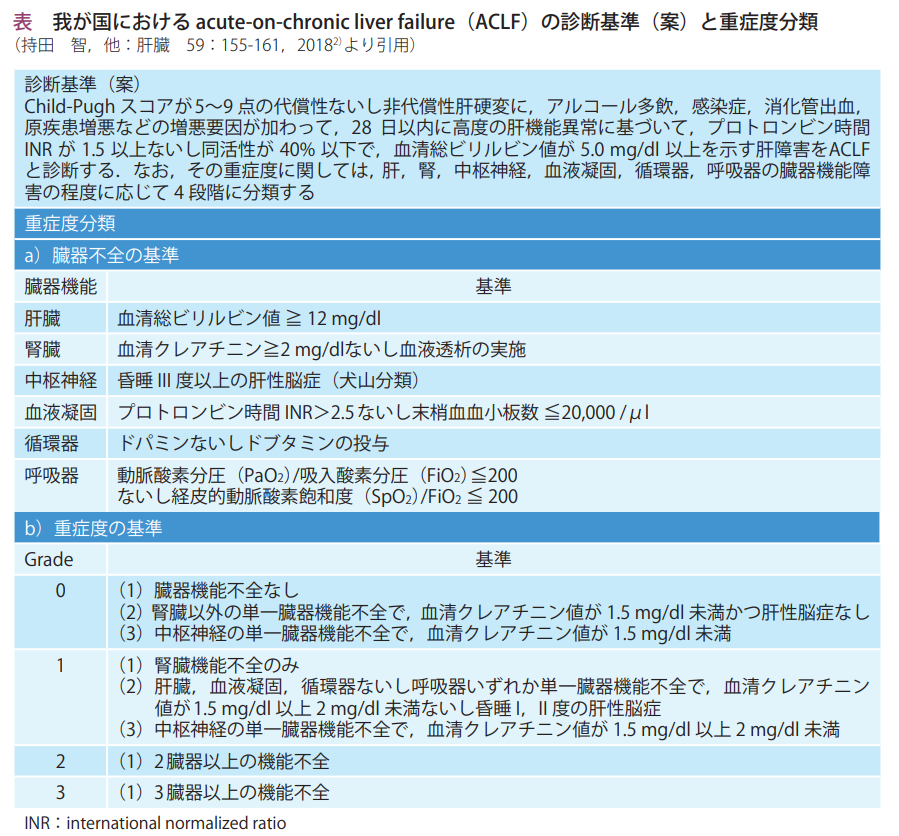
ACLF診断基準/重症度分類
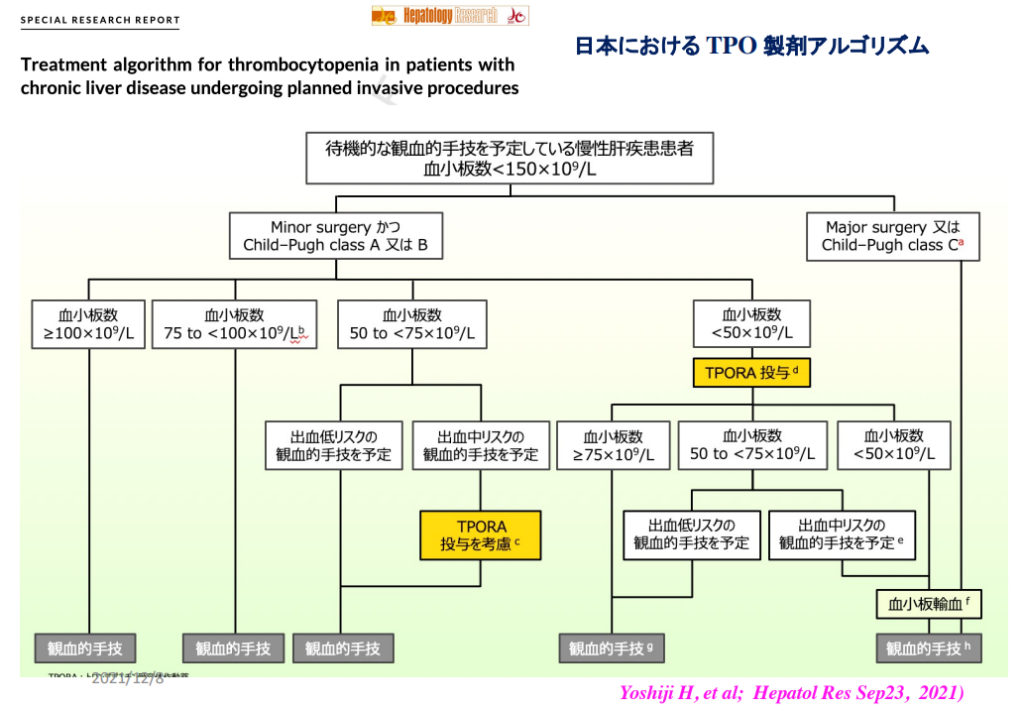
血小板減少に対する支持療法

肝性脳症
飯塚病院HPに詳しい
https://aih-net.com/liver/medical/letter/51.pdf
https://aih-net.com/liver/medical/letter/52.pdf
肝性脳症の分類(欧米の診療ガイドライン同様)
Type A:急性肝不全に起因するもの
Type B:主に門脈―大循環シャント・バイパスに起因するもの
Type C:肝硬変に起因するもの
脳症発症機序と原因
原因
①血中アンモニア濃度の上昇
②血中フィッシャー比の低下
肝性脳症の発症にはさまざまな要因の関与が考えられているが,なかでもアンモニアの関与がこれまで想定されている.通常,アンモニアは門脈を経て肝臓に入り,ここで肝細胞の尿素回路により尿素に代謝され最終的に尿中に排泄される.しかし,肝硬変患者では肝細胞障害によりアンモニアの代謝能が低下しており,そのため血中のアンモニア値が上昇して血液脳関門を通過し脳に到達することで肝性脳症が発症するとされている.アンモニアはアミノ酸の代謝過程で発生したり、腸内細菌によって産生されたアンモニアが腸管から吸収され、門脈系シャントを介して体循環に入る。
また、血中フィッシャー比の低下によって、脳内神経伝達に異常が生じることも要因と考えられている。肝臓の働きが悪化すると、肝臓でしか代謝されないAAAの血中濃度が相対的に上昇し、筋肉や脂肪組織で代謝されるBCAAは、エネルギーやグルタミン酸の供給源となってアンモニア処理に使われたりするために相対的に減少する。実際にある程度までの脳症であれば、分岐鎖アミノ酸(アミノレバンⓇなど)の点滴投与で速やかに症状が改善するため、この機序の存在も明らかと思われる。
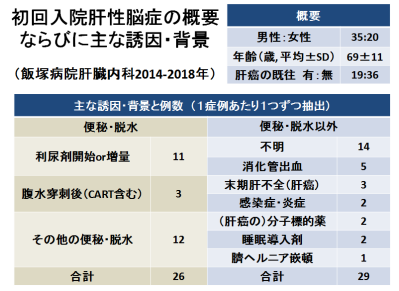
「便秘・脱水」が半数近くと多い。「便秘・脱水」に至る経緯では、経験上、利尿剤導入直後や腹水穿刺排液後に多い印象があった。非代償性肝硬変での腹水と肝性脳症の併存への対処について、欧米には「‘ wet and wise’ rather than ‘ dry and demented’」意訳すれば「絞って脳症より腹水がまし」という標語があり腹水があっても自宅で過ごせますが、肝性脳症では難しくなるので利尿・除水はほどほどに、という意味です(飯塚病院HPよりhttps://aih-net.com/liver/medical/letter/52.pdf)。
血液検査・診断
アンモニア濃度測定
肝性脳症では血中アンモニア値は一般に高値を認めるが,臨床症状と時相的なずれがあり得るので値が正常域の場合もあり注意が必要である
血漿遊離アミノ酸濃度
アミノ酸分析ではBCAA/AAAモル比(フィッシャー比)の低下を確認する
肝性脳症重症度分類
肝性脳症の意識障害の程度については,本邦では以前より犬山シンポジウムで提唱された昏睡度分類が長らく使用されてきた.欧米のガイドラインでは,West Haven Criteria(WHC)及びInternational Society for Hepatic Encephalopathy and Nitrogen Metabolism(ISHEN)が用いられており,本邦で使用されている犬山シンポジウムの昏睡度分類はWHCのGrade I~IVを5段階に分類したものである
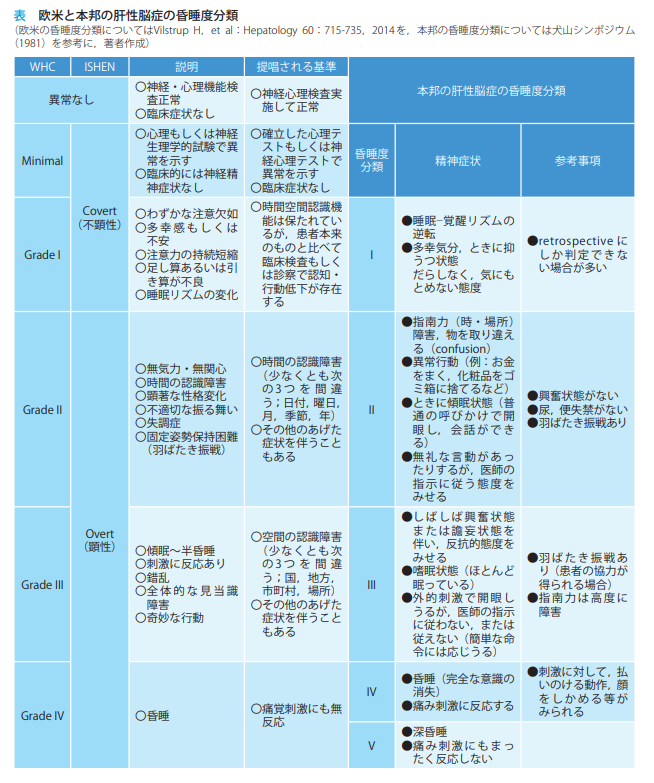
肝性脳症の治療
肝性脳症の治療としては,誘因の除去と栄養・薬物療法が大きな柱である.
肝性脳症の誘因
便秘,蛋白過剰摂取,消化管出血,感染症,脱水,利尿薬の過剰投与等
栄養療法
長期にわたる蛋白制限食はサルコペニア等を悪化させて予後に悪影響を及ぼすことより前版同様に行わないことを提唱している
薬物療法
合成二糖類,BCAA,腸管非吸収性抗菌薬等が中心となり,カルニチン製剤や亜鉛製剤,さらにプロバイオティクスの有用性についても新しい肝硬変診療ガイドラインで言及されている
具体的な治療方法
II 度の肝性脳症ならばGE浣腸とアミノレバン点滴でほぼ当日中に覚醒させることができる
分岐鎖アミノ酸製剤点滴のみでは、一旦覚醒しても大腸内に大便が残っていると、ウレアーゼ産生菌が増殖し
てアンモニアがすぐに上昇してしまうため、急性期の対処としては、十分に排便させることが最も重要
再燃予防に関しては①アンモニア産生防止が柱で②BCAA製剤投与は補助的
- 食事療法(低蛋白食,高カロリー食:分岐鎖アミノ酸製剤の経腸栄養製剤)
- 利尿剤の中止
- 脱水補正
- アミノレバン
- 透析
- 合成 2 糖類:ラクツロース、モニラック、ラグノスゼリー
ガイドライン上の第一選択、グリセリン浣腸も有効(モニラック浣腸とGEは治療成績同等→廃れた)
合成 2 糖類の作用機序
浸透圧性下剤としての作用
腸内 pH を下げアンモニア産生菌の発育を抑制する作用
腸内細菌により乳酸に分解され腸内 pHを低下させ NH3を NH4+に変換(NH4+は細胞膜を通過できない)
近年のメタ解析(24 の比較対象試験 1487 症例)では、脳症だけでなく生存率も改善した
内服困難な場合には、訪看による定期的な浣腸も重要 - BCAA製剤:
再発防止としては補助的なもので、直接的な脳症予防効果が実感されることはなかなかない
期待される効果
1)血中及び脳内のアミノ酸インバランスが是正される
2)脳内神経伝達物障害の改善 - リファキシミン(リフキシマ):1 錠の薬価はカナマイシンの 5 倍、200mg=204円、1日1,200円
ラクツロースと併用する
国内臨床試験において、本剤の12週間を超える使用経験はないため、12週間を超えて投与する際はその必要性を慎重に判断すること。
合成 2 糖類単独で肝性脳症の再燃が防止できないことも多いので、追加するのが非吸収性抗生物質
2016 年末からリファキシミン(リフキシマ)が「肝性脳症による高アンモニア血症」に適応となった
合成 2 糖類と比べて怠薬が少ないことや、便中でアンモニアを作る菌の増殖を抑えているため、排便に神経質にならずに済む
また、後ろ向き研究ですが、リファキシミンにも肝細胞癌のない非代償性肝硬変患者の死亡リスクを低下させるという報告がある - 亜鉛製剤:
肝硬変症では,しばしば亜鉛欠乏がみられ,肝性脳症等肝硬変合併症の病態に関与していることが近年明らかになっている.亜鉛が欠乏すると尿素回路機能低下が起こり,肝臓でのアンモニア処理が滞るために血中アンモニアが上昇し,肝性脳症の発症につながる.本邦からも亜鉛製剤の投与で有意にアンモニア値を低下させたとの報告もされている - カルニチン:
1.5~3.0gを分3で投与する- 内用液:エルカルチンFF10%内用液15~30mL分3
- 錠剤:エルカルチンFF錠250mg6~12錠分3
- ×注射:エルカルチンFF静注1000mgシリンジ→3~6時間毎の投与が必要なため在宅適応なし
- プロバイオティクス:
肝硬変患者では,胆汁酸産生能の低下や門脈圧亢進症,腸管バリアの破綻等が起こり腸内細菌叢異常を呈し,肝性脳症の発症に関与することが報告されている.- PPIは中止すべき?(腸内細菌叢に影響する)

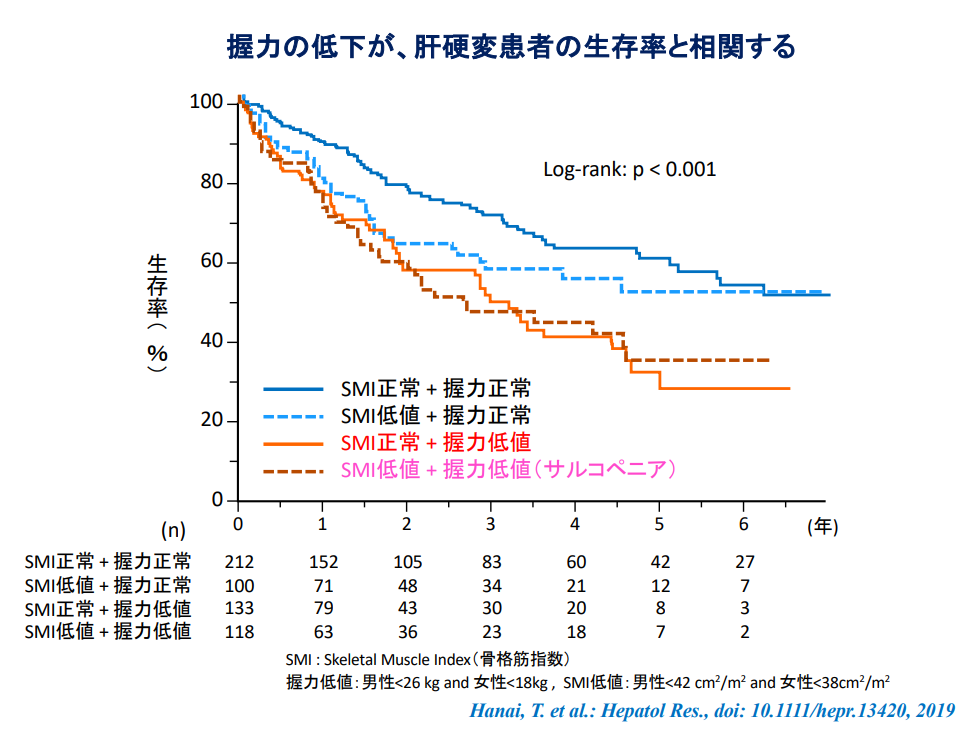
サルコペニア
肝硬変→サルコぺニアになる→最終的には寝たきりになる
サルコペニアの肝硬変患者→アミノ酸代謝が不利で肝性脳症になりやすい
サルコペニアは肝硬変の病態や予後に影響する.2016年に日本肝臓学会から提唱された肝疾患に特化したサルコペニア判定基準では,肝疾患ではPEM等に起因する二次性サルコペニアを来たし得ることから年齢を除外し,測定の困難さから歩行速度の測定を除外し,握力と筋肉量のみを用いる.肝硬変に伴うサルコペニアの治療は,栄養・運動療法が基本となる.薬物療法についてはBCAA製剤やL-カルニチン等が有効であるという報告があるが,大規模な臨床研究がなくエビデンスの高い結果が得られていない.
骨格筋量低下状態「サルコペニア」と肝性脳症の有無の相関を調べた 6 つの研究論文のメタ解析では、サルコペニアと肝性脳症の存在が関連している(オッズ比 2.74、95%信頼区間 1.87-4.01)と報告されています(J Formosan Med Assoc. 118;833-842:2019)。また、経口での BCAA補充は、肝性脳症の再発頻度は改善しないものの、非顕性肝性脳症や筋肉量を改善することが報告されています(Am J Gastroenterol 106;1081-1088:2011)。肝硬変は低栄養・サルコペニアになりやすく、骨格筋量の低下を防止することは、肝性脳症の症例の予後改善につながると考えられるため、日本のガイドラインでは BCAA の使用が推奨されています(日本消化器病学会 肝硬変診療ガイドライン 2015)。
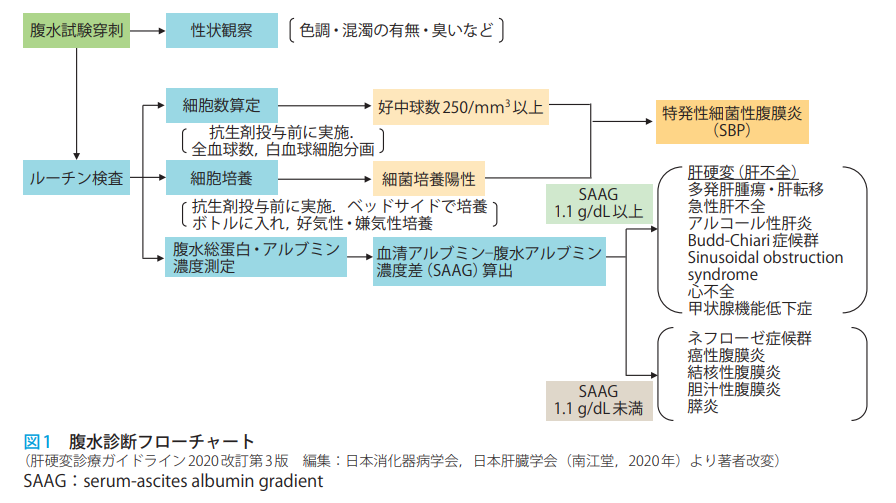
肝性腹水
機序
門脈圧亢進や低アルブミン血症、血管内脱水によるアルドステロン亢進等を起端として液性因子等を介した体液貯留の機序により肝性腹水の病態が形成される
治療
塩分制限+利尿剤
- 利尿剤
- スピロノラクトンが第一選択
- ループ利尿薬を追加
- だめならトルバブタン

肝腎症候群
肝腎症候群(hepatorenal syndrome:HRS)の本態は,肝硬変により低アルブミン血症及び門脈圧亢進が進行する中で,末梢血管の拡張に伴い循環動態がhyperdynamic stateとなり,血中エピネフリン濃度が増加することに由来し,この結果,心拍出量は増加するが,腎臓では腎血管の収縮により腎血流低下を来たし,腎機能の著しい低下が惹起されることによる.感染,エンドトキシン血症の出現でさらに腎機能障害は進行する.本症候群は従来,腎障害が急激な経過をとる1型とより緩徐な経過をとる2型に分類されてきた.現在の定義では,1型HRSは急性腎障害(Acute Kidney Injury:AKI)の診断基準に合致するものであり,HRS-AKIと呼ばれる.一方,2 型ではAKIの定義には合致せず,non-AKIHRSあるいはNAKI-HRSと呼ばれる.HRSの治療の基本は,アルブミン製剤投与下で循環血漿量を確保しつつ血管収縮薬を投与することである.現時点において我が国では,アルブミンとノルアドレナリンの併用投与を行う.肝移植によりHRSの予後は改善するが,肝移植待機中のHRSにおいて,HRSに対する治療反応性が重要な予後規定因子となる.
肝胆膵
胆石発作
- ボルタレン(臨床試験ではdiclofenac75mg筋肉注射)はRCTでプラセボや鎮痙薬に比べて有意に鎮痛および胆嚢炎進展抑制作用を認めた
→胆石発作の第一選択として使用してよいが、処方には別途の保険病名が必要
脂肪肝
脂肪肝の分類
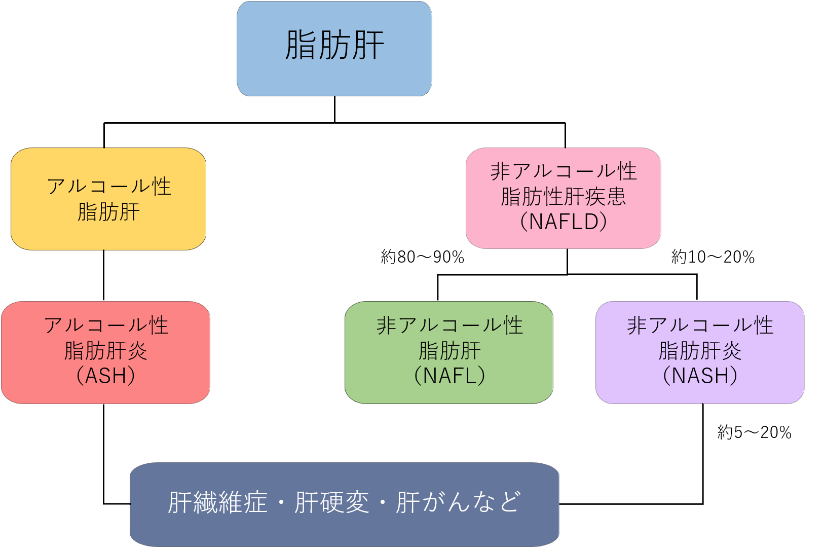
- 脂肪肝の定義:脂肪性肝疾患とは肝細胞に中性脂肪が沈着して、肝障害をきたす疾患の総称で、日本肝臓学会、日本消化器病学会の診療ガイドでは「大滴性の脂肪滴を 5%以上の肝細胞に認める場合」をいう
- 単なる脂肪肝は予後との相関性が乏しく、評価の必要性は必ずしも高いとは言えず、近年では肝線維化が最も重要な予後因子であるということがわかっており、線維化の程度を把握することがより重要
- 画像評価方法:
脂肪肝を拾い上げたら線維化も評価する必要がある→画像所見および血液生化学検査にて評価- 超音波B モード所見では 30%以上の肝臓内脂肪化を有する場合には感度/特異度は良好だが、それ以下では感度特異度ともに低下する
- 高輝度肝(bright liver)
- 肝腎コントラスト ( hepatorenal echo contrast)
- 肝脾コントラスト(hepatosplenic echo contrast):通常肝実質のエコーレベルは脾実質とほぼ同等
- 深部減衰(attenuation)
- 肝内門脈枝・肝静脈枝の不明瞭化(vascular blurring)
- 超音波の減衰に着目した手法が近年報告され、5%以上の肝脂肪化の検出も可能と報告されている
報告されている方法としては、CAP(Echosens、Paris、France)、Attenuation imaging(ATI:キャノンメディカルシステムズ、東京、日本)、Ultrasound-guided attenuation parameter(UGAP:GE ヘルスケア・ジャパン株式会社、東京、日本)、Attenuation coefficient (ATT:日立製作所、東京、日本)がある - 肝臓の脂肪成分が 30%の場合は肝臓と脾臓のCT 値の比(L/S 比)が 0.9~1.1 である
- 肝内の脈管が肝実質の CT 値より視覚的に同等以上の場合は肝臓の脂肪成分が 30%以上とされる
- 超音波B モード所見では 30%以上の肝臓内脂肪化を有する場合には感度/特異度は良好だが、それ以下では感度特異度ともに低下する
- 血液検査所見・肝生検
- ALT、ASTの値が50~100前後に上昇
- 脂肪肝か、脂肪肝炎かの鑑別には肝生検が必要となることがある


- スコアリングシステム
- FIB-4 index(フィブフォー・インデックス)
- NFS
- APRI
- M2BPGi
- オートタキシン
- ヒアルロン酸、IV型コラーゲン、IV型コラーゲン7S、III型プロコラーゲンN末端ペプチド(P-III-P)、M2BPGi
- エラストグラフィーによる肝線維化の画像診断(MRI>超音波)
MRエラストグラフィーが保険認可された
いろいろあるが、複数の検査結果を総合して評価することが望ましい

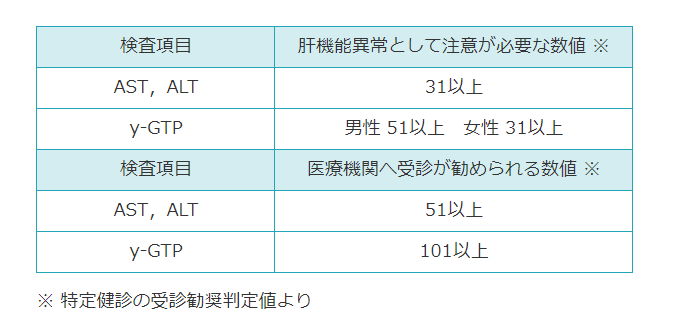
- AST、ALTはいずれもトランスアミナーゼとよばれる酵素で、アミノ酸をつくる働きをしている
- 血中半減期はASTでは11~15時間、ALTでは40~50時間
- ASTは肝臓のみならず心筋や骨格筋、赤血球などにも広く存在する
- ALTは主に肝臓に存在
- アルコール性肝障害ではAST優位が特徴で、AST/ALT比が2近くまで上昇する。エタノールによってALT合成が阻害され、かつ障害がミトコンドリアに及んでAST-mが逸脱するためとされる。
NAFLD/NASH
NAFLD/NASH+サルコペニアは明らかに予後不良群
治療薬はなく、生活習慣の是正による改善を目指す(肥満やDM、HTなどの併存症があれば治療する)
- NAFLD/NASH診療ガイドライン2020(改訂第2版、日本)
- 日本消化器病学会のNAFLD診断基準
①画像診断あるいは組織学的に脂肪肝を認め,②アルコール摂取が男性で30 g/日,女性で20 g/日以下,③脂肪化や慢性肝疾患の原因となる他の要因がない,という3項目をすべて満たすものをNAFLDと診断する. - 病期分類:Matteoni の分類
1999年にMatteoniらがNAFLDをType1~ 4 の 4型に分類しType1とType2をNAFL,Type3とType4をNASHと定義した.この区分の根拠としては,肝がん,肝不全,食道静脈瘤破裂などによる肝疾患関連死との関連を検討したところType1、Type2では8年間の観察期間で死亡率が1.7 %であったのに対し,Type3,Type4では11 %と有意に高く,またその後10年の観察期間でも2.7 %と17.5 %と有意にType3,Type4での肝疾患関連死が高いことが明らかになったことによる - CT/エコーで脂肪肝と診断されたら、予後良好なNAFLか慢性肝疾患として精密検査と治療が必要なNASHか鑑別する
- NAFLD=NAFL(非アルコール性脂肪肝)+NASH(非アルコール性脂肪肝炎)
- NAFL:肝細胞に脂肪が沈着するのみの単純性脂肪肝、NAFLD全体の9割
- NASH:脂肪沈着とともに炎症や線維化がおこる脂肪性肝炎(NAFLDの1割)、人口の2~3%程度と推定される
- NAFLからNASHへの進展に関わる病態は現在でも全ては解明されていないがMultiple parallel hits hypothesisが提唱されている
- NAFLDは国内で2200万人と推定されている(ドック有病率は男性40%、女性30%)
- 慢性肝疾患におけるNAFLD・NASHの罹患率は、欧米では49%
- NAFLDに脂質異常の合併は70%に見られる
- NAFLDに高血圧の合併は40%に見られる
- NAFLDに高血糖の合併は20%に見られる
- NAFLDにメタボリック症候群の合併は40%に見られる
- 初期は肝脂肪化がメインだが、徐々に線維化が進行すると脂肪化はむしろ低下する
- 肝線維化が最大の予後規定因子でNASHの5~20%が肝硬変に至る
- NAFLDのからの肝発癌率は低率(0.44/1000人・年)であるが、肝病態の進展とともにリスクは上昇し、NASHでは5.29/1000人・年、肝硬変では0.45~22.6/1000人・年であるとされる
- NIT(非侵襲的診断法)が一般診療では用いられる
- 治療:
- NAFLD/NASHに適応のある薬剤はない
- 高血圧合併ではARBが肝線維化を抑制する可能性あり
- DM合併例では、若年でも線維化進行しやすくピオグリタゾンに加えてSGLT-2阻害薬やGLP-1作動薬が推奨される(ガイドライン2020)→現在、第一選択薬としての優劣性についてRCTで検証中
- DM非合併NASHにはビタミンEが有効(ガイドライン)
- 薬物療法では、脂質異常症治療薬や糖尿病薬を活用することが重要
- 予後:
- NAFLD/NASHの生存率は、肝臓の線維化が進行にともない悪化する
- NAFLD/NASHの死因の第一位は心血管疾患、2位が悪性腫瘍、3位が肝疾患とされている
アルコール性肝障害
- JASBRAアルコール性肝障害診断基準 2011年版
- 診断基準:長期(通常5年以上)にわたって、「1日の平均飲酒量が約60g以上」であり、「禁酒で血清AST・ALT・γ-GTPが明らかに改善」「肝炎ウイルスマーカー・抗ミトコンドリア抗体・抗核抗体が陰性」のもの
アルコール性脂肪肝
ASH(アルコール性脂肪肝炎)
AIH
ウイルス性肝炎
B型肝炎
- 1964年に発見
A型肝炎
- 1975年に発見
C型肝炎
- 1989年に発見、それまでnonAnonB肝炎とされていた
HCC
- 肝がん診療ガイドライン2021
- SURF試験の結果から『3㎝、3個以内』に対してはRFAと手術は同等の成績となった
- 使用できる分子標的薬は6種類
胆道癌
- 胆嚢癌に対する系統的肝切除(S4a+S5)は不要(胆嚢床切除と治療成績同等)
- T2N0胆嚢癌では、予防的肝外胆管切除は不要
- m、mp胆嚢癌は追加切除不要(SS胆嚢癌以上は追加切除)
- 化学療法はGC療法、GS療法、GCS療法が一次治療として選択できる(OSはGCS>GS=GC)
- 二次治療はmFOLFOX(まだ保険適応外かも)、S1単剤
- 遺伝子パネル検査も保険適応→ペミガチニブ、ラロテレクチニブ、ペムブロリズマブ
- 切除不能肝内胆管癌に対する粒子線治療も保険適応となった(2022年4月~)
胆嚢腺筋腫症/ADM
- 胆嚢壁内におけるRokitansky-Aschoff sinus(以下、RAS)の増殖により胆嚢壁の肥厚、壁内の嚢胞性変化(拡張したRAS)、上皮の増殖、平滑筋細胞の増生を特徴とする疾患
- 底部型が最も多い、底部型>分節型>びまん型だが、臨床では混在型も多い
- 分節型(輪状型)は、胆のう中央付近の内壁が全周性に肥厚し、胆のうに「くびれ」ができるため、胆汁が胆のう内にうっ滞して、結石(胆石)ができやすい
- 砂時計様変形をきたし、濃縮胆汁を認める(MRIT2WIで低信号化する)場合には無症状でも相対的手術適応とする施設もある(胆道2020p163-174:胆嚢腺筋腫症の疫学と診断)
- 胆嚢腺筋症でもよい
- 頻度は胆嚢摘出標本の2~14%、人間ドックの0.12~0.49%
- 好発年齢:40~60代、やや男性に多い
- 胆石合併率は全体で4.8%(分節型10.8%>びまん型3.3%>底部型1.7%)
- 胆石症の7.5%でADMを合併する
- 胆嚢癌手術例の8.9~12.4%にADMを合併しており、ADMの4.3%(分節型の6.4%)に胆嚢癌を合併していた
- 明確な画像診断基準がなく、正確な診断のためには病理診断による必要がある
- 超音波検査:小嚢胞構造(感度80%、特異度85%)、コメット様エコー
ガイドライン、学会での最新知見
消化器外科学会2022
膵癌 3万人超/年の死亡者数(2017年)
切除可能膵癌(5OS=20%)にもNAC(GS療法)が推奨されるようになってきた
ACT:日本ではS1半年間、欧米ではmFOLFIRINOX半年間
課題:すべての症例にNACが必要か
Prep-02/JSAP05 試験:術前NAC(GS2コース) vs 手術先行+ACT(S1)のRCT
medianOSはNAC-GS2コース 群 が 36.7 カ 月(28.7~43.3 カ 月),Up-S群が 26.7 カ月(21.0~31.3 カ月),ハザード比 0.72,p=0.015 と有意に NAC-GS 群の治療成績が良好であった
→膵癌診療ガイドライン2019では『切除可能膵癌にNAC-GS療法を行うことを提案する、推奨度:弱い』となっている
胆道:非拡張胆管(CBD径8㎜以下)は良性胆道狭窄のハイリスク(狭窄発生率12%)
非拡張胆管の吻合方法は連続縫合16%で高率に発生し、結節縫合で3%と結節縫合が良い(愛知県がんセンター単施設研究)
術前胆道ドレナージした方が術後狭窄少ない
肝臓 高難度腹腔鏡下肝切除
大阪府立医大、国がん、埼玉がんセンター、佐賀大学、大垣市民、北里大学など
肝門部でLaennec被膜を肝臓側に温存しながらグリソン鞘を剥離していくが、グリソン鞘を損傷しないことが重要で多少肝実質に入り込んでもよい
ラパカンではnegative stainingが主流
S7Positive stainingはICG1000倍希釈、3-5mL注入するが染まりムラがある→Chairmanより動脈クランプすればよいとアドバイスあり(北里)
S7亜区域切除にはいろんなアプローチがある
後区域グリソンテーピングは引き算か、尾状葉先行離断してから後区域のみテーピングする方法がある
上尾中央総合病院でも腹腔鏡下S7切除は平均6時間かかる
アンカーと呼ばれるGlisson鞘と肝実質を固定する細かな索状構造
→杉岡 篤,加藤悠太郎,棚橋義直,他:肝切除術に必要な外科解剖.消外 39:1035-1048,2016
その他(周術期管理、消化器一般・内視鏡・デバイスなど)
神経因性膀胱
男性→シロドシン+ウブレチド
女性→エブランチル+ウブレチド
※ウブレチド単独では投与禁忌(膀胱破裂することがある)
膀胱留置カテーテルによるテネスムス
- ボルタレン座薬25㎎
- アセリオ1000㎎
日本の有名外科医
中山恒明(M43‐H17,94歳):
高崎健: 東京女子医大肝臓外科、中山弟子
比企 直樹: 癌研→北里大学教授
高田忠敬