集中治療
敗血症・敗血症性ショック
qSOFAでスクリーニング(ただし感度は0.46と半分ほどしか拾えない)し、2点以上ならSOFA!
SIRSは特異度0.24となんでも拾いすぎるので使用しにくい


- 現在の定義『感染+臓器障害』、診断基準は『感染+SOFAスコア2点以上の増悪』
- ショックは『敗血症のうち循環不全により死亡リスクが増加した状態』
- ERではqSOFAを敗血症診断の目安にする
- pH<7.15(→カテコラミン不応性を招く)のときはCRRTでアシドーシス補正を考慮する
- CRRT開始前~開始早期はメイロンでアシドーシス補正(100~200mL/hr程度)してもよい
- 敗血症性ショックでNAD反応不良のとき心臓の動きもチェック→動き悪ければ少量持続ボスミン、動き良ければピトレシンを追加する
- 重症ショックの場合はdose upより併用(ステロイド±ピトレシンorボスミン)が効果的
- ボスミン5mL+生食45mLで使用する(0.3~0.4γ程度、NADと同様)
- ボスミン持続はNOMI引き起こすので極力短時間にとどめる
- 急性期はカテコラミン増減の効果を迅速に反映させるため押し水を80mL/hrなどに早める
- カテコラミン投与ラインのカテ入れ替えのときは2セット用意して併用しつつ入れ替える
- カテコラミン不応性の原因となるためアシドーシスの改善を目指す
→その手段としてCHDF、メイロン100~200mL/hrなど - 大量FFP(10~20単位)、ソルコーテフ、ピトレシンで早期にボスミン終了目指す
- ソルコーテフは100㎎のbolus後に200㎎の持続投与がよい(300㎎/日以下が推奨される)
- ピトレシン20単位+生食100mLの9mL/hrでほぼ最大投与量
- ピトレシンを残してNADを先に減量する
- 抗生剤初回量は目標濃度と分布容積の大きさによって決定され、排泄能力に影響されない
- 腹膜炎に対するMEPMは腸球菌カバーできていない→PIPC/TAZの方が良いかも
- 敗血症性急性腎不全では抗生剤減量不要、無尿でもCRRTしていればMEPM1g8qでよい
- RBC/FFP大量輸血後は低Ca血症きたすため補充を考慮する
- 乳酸高値の場合、ラクテックは避けた方が無難(→添付文書上は禁忌)

- non-renal indication CHDFの導入基準
→過剰な炎症性サイトカインを除去し免疫調整による病態改善が目的- 敗血症性ショックでカテコラミンサポートを要する状態
- PMXか、PMMAか
- 外因性物質(エンドトキシンなど)と内因性物質(各種サイトカイン)のどちらがSepsisの増悪因子か?というスタンスの違いにより治療法選択肢が異なる
- 原因物質の除去の方法は濾過(=限外濾過のみ)、透析(=拡散+限外濾過)、吸着の3パターン
- PMX-DHB(ポリミキシンBカラム)→エンドトキシン吸着療法 数時間で終了
- CHDF
- PMMA膜→サイトカイン吸着能を有する膜(=透析=拡散+限外濾過)、安全に溶質除去が可能
- セプザイリス(AN69ST膜)→HMGB-1吸着能が優れている
菌血症
- GPC、カンジダ血症→フォローアップ血液培養で血液培養陰性化を証明することが診療ガイドラインで推奨されている
DIC
急性期DIC診断基準(日本救急医学会、2005年)を用いる

- FDPやDダイマーが高値を示すとき,同時にフィブリノゲンや血小板の減少が認められる場合はDICが疑われるが、急性期DICスコアはフィブリノゲンを含まない
Dダイマー:安定化血栓が形成され、線溶の最終過程で上昇するマーカー(DVTや肺塞栓、大動脈解離など)。FDPはフィブリノゲン分解(一次線溶)とフィブリン分解(二次線溶)を総合的に反映するが、Dダイマーは二次線溶だけを反映する。急性期線溶亢進よりも血栓のマーカーとして利用される。
FDP:フィブリン・フィブリノゲン分解産物のことで、
- FDPの上昇がない出血症状と凝固異常(PLT低値、凝固能低下は出血でも起きる)は単純に出血源のコントロールができていないという可能性もある
輸血関連
・血液型の検査(ABO式)は表試験とウラ試験で決定、表裏の結果が一致することが重要
・交差適合試験には主試験と副試験とがある(主試験のみでOK)
・クロスマッチ主試験に必要なのは患者血漿!!血球ではない!!
・不規則抗体陽性の場合は、抗原陰性のRBC血液を輸血する必要がある
・現在、血液センターではすべての血液について37℃で反応する不規則抗体のスクリーニングを実施し、不規則抗体の認められない血液を供給しているため、患者の血液型検査が適正に行われていれば、副試験は省略することができます。
・不規則抗体は輸血や妊娠等によって産生されることがあり、特に通常の輸血ではABO型とRh(D)型だけを適合させているので、その他の赤血球型抗原に対する同種抗体が産生される可能性があります。
・不規則抗体陽性の場合は、FFPについては一致の必要性なし。
・抗原陰性の頻度(=適合血液)は不規則抗体の種類によって異なる。
・赤血球の交差試験(副試験)は省略してもよい
・血漿・血小板製剤の交差適合試験は省略してよい
・T&Sの適応:出血量が500~600mL以下と少なく、術中の輸血の可能性が30%以下と低いことが予想される待機的手術。その際、患者のABO・Rh血液型と不規則抗体検査を実施し、ABO血液型に異常がなく、Rh(D)陽性で、不規則抗体陰性の場合には術前に交差適合試験を実施せず、輸血用血液製剤のABO式のみ確認する。
DVT治療/予防
- 近位DVT→ヘパリン+ワーファリンが基本
- プラザキサ以外のDOACはヘパリンブリッジ不要
- DOACの欠点は高価、中和剤なし
- DVTの一過性の危険因子(例,不動状態,手術)を有する患者は,通常3~6カ月後にワルファリンの服用を中止
- 遠位DVT(膝窩静脈以下、後脛骨V, 腓骨V, 前脛骨V, 腓腹筋, ヒラメ筋の静脈の血栓症)は治療対象外とする意見もある
・高リスクで30%、最高リスクでは50%のDVT発生率→DVT予防は必須
・低用量未分画ヘパリン→打つだけ、モニタリングしない(できない)
分子量3000~30000(低分子ヘパリンは分子量5000)
8時間もしくは12時間ごとに未分画ヘパリン5,000単位を皮下注射する方法。
通常は凝固能のモニタリングを必要とせず,簡便で安く,安全な方法である。
長期予防が必要な場合,未分画ヘパリンからワルファリンに切り換えて抗凝固療法を継続する。
・用量調整未分画ヘパリン→APTTでモニタリングする投与方法
ヘパリン類/新しい経口抗凝固薬の種類

①未分画ヘパリン(いつものヘパリン、ヘパリンNa、ヘパリンCa=旧カプロシン)
・ヘパリンNa5000単位=156円
・XaもIIaも阻害する→だから分子量がでかい!
・ヘパリンCaの方が容量少ない(1万U/0.4mL)→皮下注向き
・APTTモニタリング可能
②低分子ヘパリン(一般名ダルテパリン、エノキサパリン、商品名フラグミン、クレキサン)
・Xaのみ阻害する
・プロタミンで最大 60%程度しか拮抗できない
・半減期2-4時間
・腎機能による調整が必要
・モニタリング不可能
③合成ヘパリン(フォンダパリヌクス(アリクストラ))
・分子量1700
・Xaのみ阻害する
④新しい経口抗凝固薬(合成Xa阻害薬)
・2022年現在、予防で保険適応となっているものはない(整形外科術後など限定的)
・ワーファリンは2/9/7/10をすべて阻害するので出血リスクが大きい
・DOACは食事による影響がない
・DOAC:direct oral anticoagulants→国際的にDOACで統一された
・NOAC:novel oral anticoagulants→現在は使用しない名称
・出血性合併症のリスクも低い
・https://www.jspc.gr.jp/Contents/public/pdf/shi-guide07_08.pdf参照
→ガイドライン通りにいくと内科疾患のDVT予防はヘパリンCa皮下注一択だが当院採用なし
循環不全、各種ショック、Af tachycardia、心不全
・術後のショック→エコーで血管内ボリューム、心機能評価、Aline波形からまずは脱水評価
・ ショックの種類を鑑別→ポンプ、タンク、パイプ! 心エコーもチェック(Volume+壁運動+右心負荷)、PEも除外、ショックの原因は敗血症だけではない!
・敗血症性ショックの血圧管理目標はMAP>65mmHg
・アシドーシス補正のためにも術後早期のCHDF導入は有効
・重症心房細動でショック→まずはVolume Rescitationで、さらにジゴキシン(1A+生食100mL点滴)、オノアクト+NAD(0.5㎎+生食45mL→3mL/hrで0.1γ(50㎏換算)、血圧低下するならばNAD追加)、フェンタニルフラッシュ+ アンカロンDIV、DC療法、なども選択肢
・CHDFはセプザイリス(一番閉塞しやすい)、除水ゼロ、QB100でスタートする、入り口圧とTMPをみるとよい。
・ブラッドアクセスカテは頸CV交換ではなく新たに鼠径部から追加すればよい
・敗血症性ショックにはNAD→バソプレシン→ステロイドの順に追加する
・Af tachy+ショックのレートコントロールはβブロッカーとしてビソノテープかオノアクト、追加するとすればジゴキシン
心不全
「定義」
心不全とは、なんらかの心臓機能障害、すなわち、心臓に器質的および/あるいは機能的異常が生じて心ポンプ機能の代償機転が破綻した結果、呼吸困難・倦怠感や浮腫が出現し、それに伴い運動耐容能が低下する臨床症候群
「原因」
1.虚血性心疾患
2.高血圧
3.糖尿病
4.心筋症 (心筋自体の病気)
5.弁膜症
6.不整脈
7.先天性心疾患・心奇形
8.sepsis、薬剤、甲状腺機能、アルコール、ウイルス感染症などの全身性の疾患
最も多いのは虚血性心疾患で、次いで高血圧症、弁膜症の順
「分類」
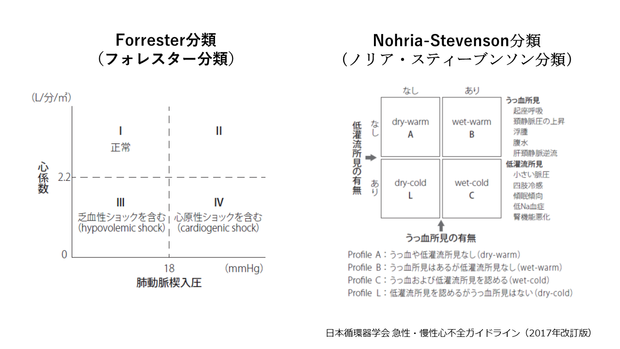
①Forrester分類(フォレスター分類)は右心カテーテル検査で得られる血行動態指標(肺毛細血管楔入圧、心係数)を用いた心不全重症度分類で、観血的検査であるため慢性心不全の重症度評価などはできません。
②Nohria-Stevenson分類(ノリア・スティーブンソン分類)は、身体所見から得られる低灌流所見およびうっ血所見から心不全患者のリスク層別化をする分類です。簡易で、非観血的に評価できます。
③クリニカルシナリオ(clinical scenario; CS)分類は循環器専門医以外の医師が救急外来での初期対応導入を迅速に行えるように作られた、血圧および病態による分類

「治療」
・症状の緩和:利尿薬,硝酸薬,またはジゴキシン
・長期管理と生存期間の延長:ACE阻害薬,β遮断薬,アルドステロン拮抗薬,アンジオテンシンII受容体拮抗薬(ARB),またはアンジオテンシン受容体/ネプリライシン阻害薬(ARNI)
使用薬剤の選択は,患者ごとの特徴と心不全の病型に依存する。現在最も一般的に用いられている心不全の分類では,患者を次のように層別化している:
- 駆出率が低下したHFrEF
- 駆出率が保持された心不全HFpEF
・HFrEFでは,これら全ての薬物クラスが研究されており,長期管理に有益である
・HFpEFでは,十分に研究された薬剤が比較的少ない。しかしながら,HFpEFの治療には一般にACE阻害薬,ARB,およびβ遮断薬が使用される。ARNIは依然として研究段階にある。複数のランダム化比較試験により,アルドステロン拮抗薬は有益であるが,硝酸薬はおそらく有益でないことが示唆されている。重度のHFpEF患者では,重度の拡張機能障害のため一回拍出量が比較的固定されているため,心拍数を(β遮断薬などにより)低下させると,症状が悪化する可能性があり,このような患者の場合,心拍出量が心拍数に依存しているため,心拍数を低下させると安静時および/または労作時の心拍出量も低下する可能性がある。
肥大型心筋症の患者では,ジゴキシンは効果的ではなく,有害となる可能性がある。
利尿剤
・別のループ利尿薬に切り替える場合は,同等の用量で薬剤を変更すべきである。フロセミド40mgはブメタニド1mgと同等であり,これらはトラセミド20mgと同等である。
・ループ利尿薬は低Na、低K、低Mg血症となる場合がある
・高容量ループ利尿薬使用時は低Kにならないようスピロノラクトンを併用する
・サムスカは心不全や肝硬変に使用可能、電解質を喪失しない
・サムスカ7.5㎎=1000円、転院時にネックとなることもある
・アゾセミド抵抗性の人がいる→この人はラシックス使用するしかない
・ARBは妊娠中は禁忌である
・硝酸薬はHFrEF患者の心不全症状を単独で緩和でき,急性呼吸困難には舌下ニトログリセリンスプレーの頓用を,夜間または労作時呼吸困難にはパッチ剤を使用するよう患者を指導することが可能である。HFrEFでは,硝酸薬は安全かつ効果的で忍容性も良好であり,特に心不全と狭心症を呈する患者に役立つ。有害作用としては低血圧や頭痛などがある。HFpEFに対する一硝酸イソソルビドの試験では,有害作用(例,頭痛)の増加および身体活動の減少との関連が示された。したがって,HFpEFでは長時間作用型硝酸薬のルーチンな使用は避けるべきである。
血管拡張薬/硝酸薬・その他

AMI→すぐにMONA(モルヒネ、酸素、ニトログリセリン、アスピリン)はダメ!
右室梗塞の場合、モルヒネ、ニトログリセリンを使うと、さらに静脈還流不全が悪化し、ショックを起こすこともある。II, III, aVFのST上昇を見たら、V4R, V5Rの検査も追加せよ!
「硝酸薬の薬理作用」
- 静脈拡張を介した前負荷軽減(心臓への還流血量減少)による心筋酸素需要の低下。
- 拡張期の心室サイズが減少、拡張終期圧は低下。拡張期の冠動脈へのプレッシャーが少なくなる→局所灌流の改善。
- 一時的にでも冠動脈が拡張し、ことにスパズムがあれば軽快する。
ISDN以外の硝酸薬は低用量で静脈も動脈もそれなりに開く→血圧が下がる。
低用量のISDN(アイトロール)は静脈のみ開く(濃くなれば少しだけ動脈も開く)
呼吸不全、人工呼吸器
人工呼吸器設定
- ARDSガイドラインではTV=6~8mL/kg 理想体重
- 理想体重の計算式
男性(kg):50.0+0.91×(身長-152.4)
女性(kg):45.5+0.91×(身長-152.4)
人工呼吸器設定
NPPV
NPPVの適応
NPPVの適応評価3つ(→スライド①②③)
気道分泌物が多い場合はNPPV適応難しい



NPPV中の抑制
ベンゾジアゼピン系、デクスメデトミジン、麻薬(ボーラスのみが推奨)など
NPPV初期設定

トリロジーEVO(フィリップス)
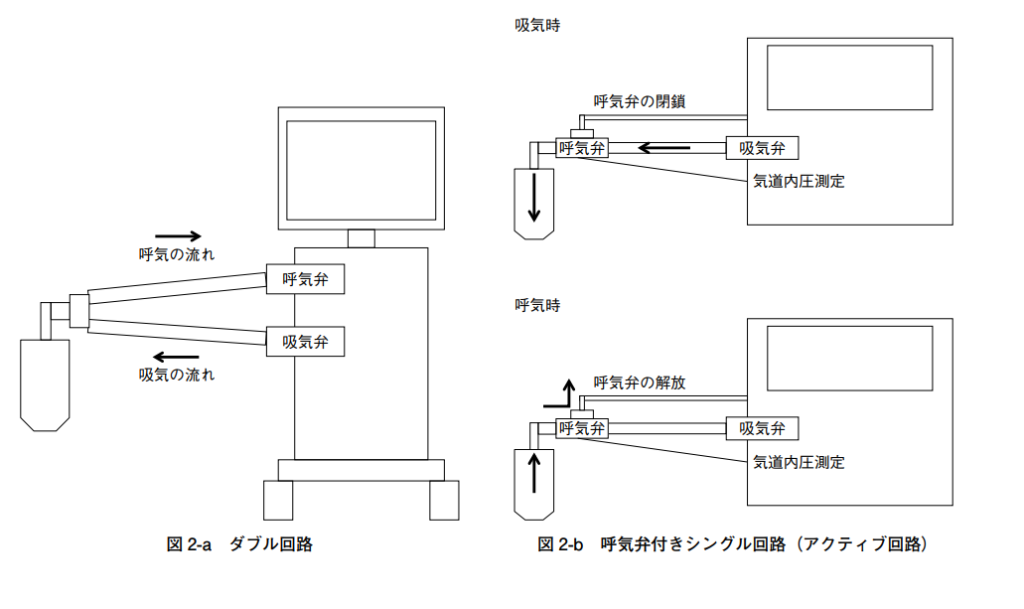
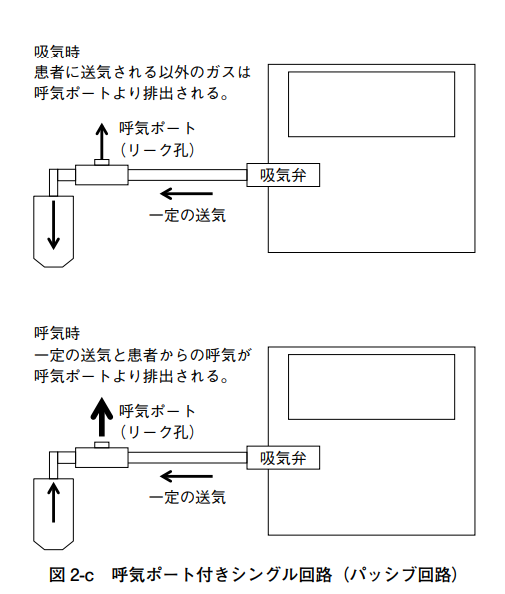
トリロジーの呼吸回路には、パッシブ回路、アクティブPAP回路、アクティブフロー回路の3種類があります。
パッシブ回路は装置からの供給量で換気量を測定
アクティブPAP回路も同様に換気量を測定します
アクティブフロー回路は回路内のフローセンサーにより患者の呼気量で換気量を測定します
気管切開術
- 鎮静薬(ミダゾラム、フェンタニル、ロクロニウム)を使用するため人工呼吸器未使用例でも呼吸器に接続
- 超肥満の場合、皮膚切開+経皮的穿刺のハイブリッドが有効
- チューブは太めのものを選ぶ(男性8~8.5㎜)
- 吸収糸の切り糸と針付きナイロン糸を用意する
- エコーで甲状腺下縁、腕頭動脈も確認しておく。
- 皮膚は横切開でも十分可能。
- 気管切開直前にFiO2:1.0にして片肺挿管にするとバルーン損傷しない。
- 左右前傾筋群の正中に黄色い脂肪組織があるので、そこを切開していく
- 最初にでてくる前頸筋群を甲状腺と見誤りやすいので注意、前傾筋群をスプリットして初めて甲状腺が見える
- 甲状腺を頭側に圧排すると気管前壁が露出する。
- 気管壁正中に1針支持糸をかけてから逆U字切開して固定糸は皮膚切開尾側縁と縫合する。
- 下甲状腺静脈の出血が危険なのであまり尾側にいかない。
CV挿入
- 救急ではカテは抜かずにどんどん追加で入れる→止血できなかったりルート不足になる
- 両下肢挙上位をとる、体位など穿刺前の準備が重要
- ひだり内頸静脈からFTL挿入する場合、ワイヤーがIVCまで落ちていることをレントゲンで確認してからダイレーションする方が安全
- FTLのワイヤーが引っ掛かる場合、FTLキット穿刺針の外筒だけをシース代わりに挿入するとワイヤーを安全に出し入れできるようになるし外筒から採血したり輸液ラインをつければ動脈血か静脈か判別が可能
- 腋窩静脈穿刺は短軸で(長軸は要アタッチメント、ただしワーキングスペース的に困難プローベは60度に寝かせて、針は45度の角度で刺入する
救急領域 ―蘇生―
心肺蘇生 アメリカ心臓協会2020
一次救命処置(AHA-BLS):
器具や薬剤を使わない救命処置(=院外CPAでバイスタンダーが行う救命処置)
AED装着が必須!!!装着すればあとはAEDの音声ガイダンス通りにすればよい
二次救命処置(AHA-ACLS):
病院等医療機関においてメディカルスタッフが行う救命処置のことで、基本のCPR(胸骨圧迫、気道確保・ 人工呼吸)と共に、気管挿管などの確実な気道確保と高濃度酸素投与、電気的除細動、静脈路確保と薬物投与を主体とした手技
心停止=4つの波形(VF、pulselessVT、asystole、PEA)
VF、pulselessVTの場合はショックが優先!とにかくショック!2サイクル目のショックのときにアドレナリン初回投与する!
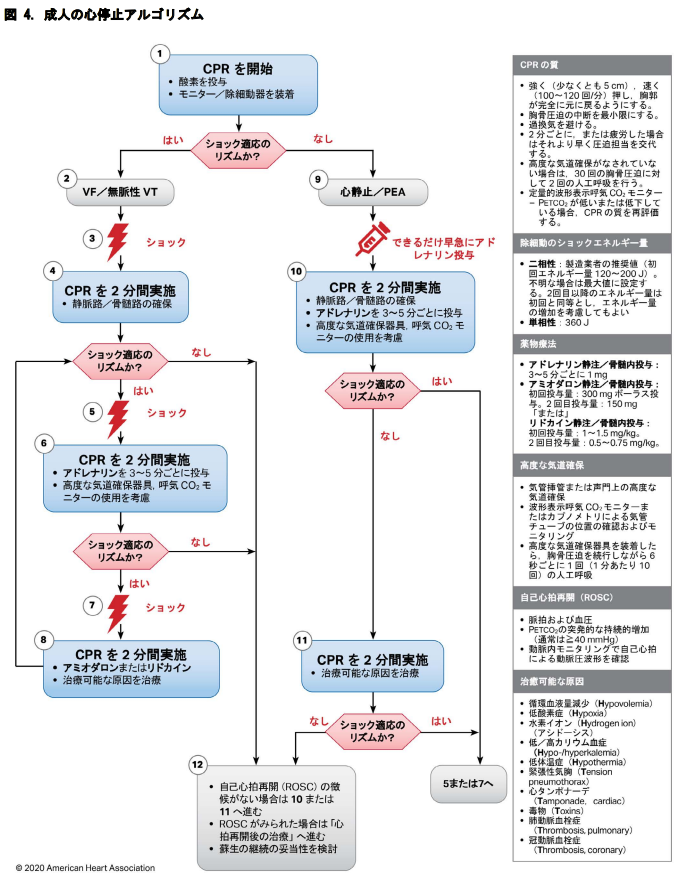
- まず、CPAであることを確認、意識、脈、呼吸→心マ開始
- 点滴、採血、タイムキーパー(できれば2分と4分でタイマー2個用意)、記録員
- AED(院内なら除細動器)、エコーを準備し解除できる異常があるか確認(心タンポ、出血、気胸←院外CPAなど機転が不明の場合はFAST)
- 蘇生と同時に原因検索→ショックの鑑別と同様(RUSH=タンク、ポンプ、パイプ)
- 2分毎にリズムチェック→PEAならパルスチェックも同時に行う
心停止時に行う鑑別6H6T(水戸済生会総合病院)
Hypovolemia(循環血液量減少)
Hypoxia(低酸素)
Hydrogen ion(アシドーシス)
Hypo/Hyperkalemia(カリウム異常)
Hypoglycemia(低血糖)
Hypothermia(低体温)
Tamponade(心タンポナーデ)
Toxins(毒)
Tension pneumothorax(緊張性気胸)
Thrombosis coronary(冠動脈疾患)
Thrombosis pulmonary(肺動脈血栓)
Trauma(外傷)
PEAの診断とマネジメントのアルゴリズム
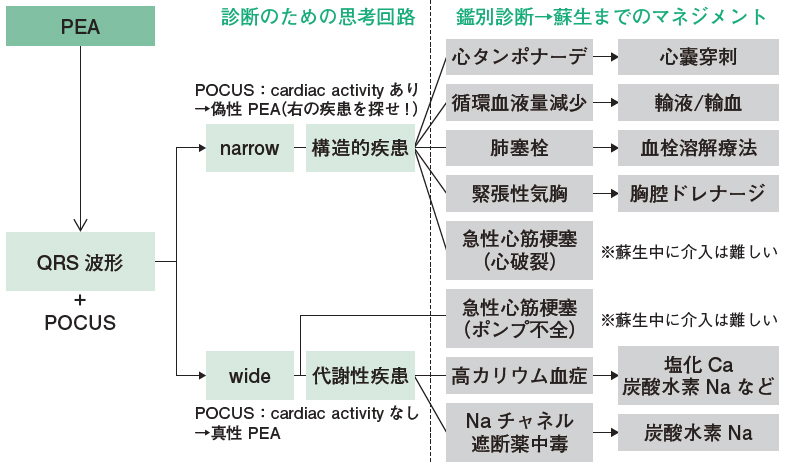
PEAの心電図波形を見て,QRS波形がnarrowかwideかである程度の鑑別が可能。原則的には,narrow QRSであれば構造的に問題がある疾患,wide QRSであれば代謝性疾患と関連がある。加えて,POCUSでcardiac activityが観察される場合は偽性PEAで構造的に問題がある疾患,観察されない場合は真性PEAで代謝性疾患と関連があると考え,鑑別を行う。
アナフィラキシーの治療に対する第一選択薬はアドレナリンであるがβ遮断薬内服下ではアドレナリンの効果が減弱し,推奨投与量の 2 ~5 倍量が必要であると報告されている。
また、β 遮断薬はヒスタミン分泌を促進するとされアナフィラキシーがより誘発されやすい状態になる→β遮断薬はアナフィラキシーのリスク因子となる。
日本のアナフィラキシーガイドライン2022(日本アレルギー学会)
グルカゴンについて「β 遮断薬服用中の場合必要となる場合がある」と記載があるのみで,推奨度等は記載されていない
アナフィラキシーショック
アドレナリンを0.01mg/㎏(体重100㎏に対して1mg、50㎏なら0.5mg=0.5A)筋肉注射(皮下注では絶対ダメ)
10~15分で再投与可能
!!!アドレナリン静注は心停止に至った場合のみ!(静注による催不整脈リスク)
Volume resuscitation(細胞外液を1-2L)も重要、適宜カテコラミン持続静注を併用
アドレナリン以外に使用できるのはグルカゴンのみ(緩徐静注)
グルカゴンGノボ1A=1㎎を緩徐静注、半減期が短い(静脈内注射の場合15〜20分)ので反復投与可能
ステロイドや抗ヒスタミン薬はショックを増長させる恐れがあるためショック時は使用できない
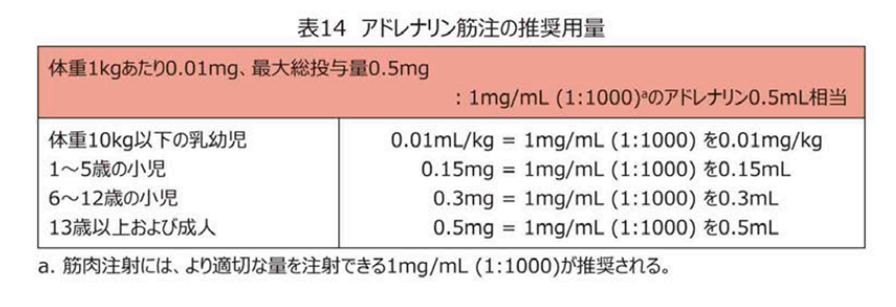





- アナフィラキシー発症から心停止までの平均時間は、薬剤投与などの医原性の場合は5分、ハチなどの毒の場合は15分、食べ物の場合は30分→皮下注では到底間に合わないので筋注が必要!
→アドレナリンの血中濃度が最高値に達するのは、皮下注射だと34分後、筋肉注射だと8分後
骨格筋は血流も豊富ですし、生理学的にもアドレナリンによって皮下の血管は収縮しますが、逆に骨格筋の血管は拡張し吸収が早くなります。先ほどのアナフィラキシーから心臓が止まるまでの時間ということからみても、筋肉注射の方が早く血中濃度の上昇が得られるのでより適している - 薬剤としては、造影剤、血液製剤の頻度が高い、ついで抗癌剤(白金製剤、タキサン系)、抗生物質
- 死亡率が高いのは造影剤と抗生物質で20%以上の死亡率がある(→血管内投与のためか)
- 蜂刺傷によるアナフィラキシーは多い順にアシナガバチ→スズメバチ→ミツバチ
ショックの鑑別
ショックは4種類に分類
①循環血液量減少性ショック(hypovolemic shock):出血,脱水,腹膜炎,熱傷など
②血液分布異常性ショック(distributive shock): アナフィラキシー,脊髄損傷,敗血症など
③心原性ショック(cardiogenic shock):心筋梗塞,弁膜症,重症不整脈,心筋炎など
④閉塞性ショック(obstructive shock):肺塞栓,心タンポナーデ,緊張性気胸など


RUSHの流れ ポンプ→タンク→パイプの順
①心臓(長軸)→②心臓(短軸)→③心臓(心窩部)→④心臓(心尖部)→⑤IVC(縦)→⑥右腎臓→⑦右胸腔→⑧左腎臓→⑨左胸腔→⑩骨盤腔,骨盤腔(縦)→⑪胸腔→⑫胸骨切痕→⑬胸部大動脈→⑭腹部大動脈→⑮大腿静脈→⑯膝窩静脈
挿管のためには昇圧が必要
→NAD5㎎+生食45mLシリンジを0.8γ(20mL/hr)くらいで急速投与してよい(BW50㎏で0.1γ=3mL)
挿管のためには事前の酸素化が必要
→Awakeのままでジャクソンリース+マスクで用手的に陽圧換気を行う
血圧維持のためにはAwakeでの挿管も辞さない
→フェンタニル1A静注+ミダゾラム0.5A静注で挿管していた
緊急時の使用薬剤
ロクロニウム(先発品エスラックス)
非脱分極型筋弛緩薬の中で作用時間が最速かつ持続時間が最短&拮抗薬(スガマデックス)がある
- 25㎎/2.5mL規格と50㎎/5.0mL規格がある
- 挿管目的には0.6㎎/㎏を静注する→25㎎規格(=42㎏程度)を1A静注しておけばOK
- ブリディオン(スガマデックス)でリバースが可能
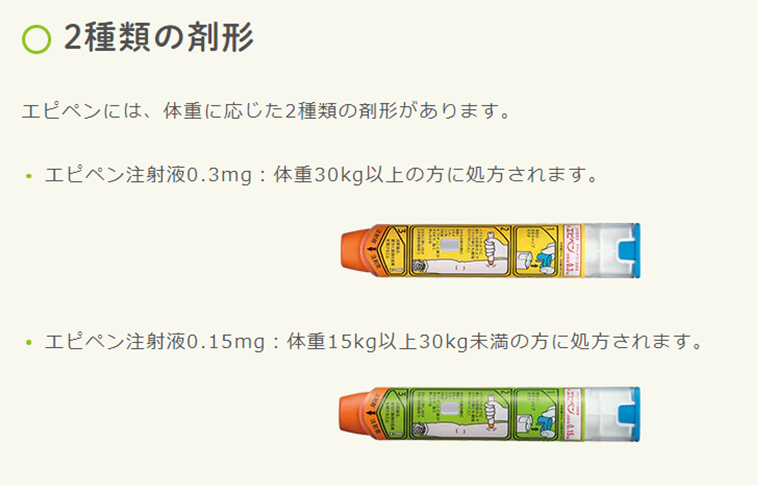
エピペン
ケースから出して、服の上から大腿中央の前外側に押しあてるだけで投与完了、0.3mgと0.15mgの2規格
有効率は70%、20%では重症のまま
硫酸マグネシウム
アンカロン(アミオダロン)
グルカゴン
救急領域 ―各論―
SAH
1万人に2人/年の発症率→そうそう出くわすものではない
予後不良→社会復帰、重い後遺症、死亡の割合がそれぞれほぼ同率の1/3
- 麻痺のない意識障害
- 光刺激を避ける(消灯+タオルで目を覆う)
- ソセゴンIV、ニカルジピンで疼痛+血圧コントロール
- 造影CT→治療方針決定
- 原因:脳動脈瘤破裂が殆ど(80から90パーセント)
- 頻度:1年で人口10万人あたり約20人(日本)、好発年令は50から60才台、女性が2倍多く、危険因子として高血圧・喫煙・最近の多量の飲酒、家族性など
DKA・HHS
典型症状は口渇・多飲・多尿+呼吸数増加(苦しそう!)+嘔吐+ぐったり
腹痛、悪心・嘔吐では必ずDKAの鑑別(急性腹症と間違えることもある)
感染(UTI)+DKAはよくある組み合わせ!!!
→尿糖+だからUTI起こしやすい→UTIが感染をさらに増悪させる→糖尿病悪化→→→
★★★重要★★★
DKAを引き起こした誘因を検索し再発予防を!
特に1型糖尿病以外の患者がDKAを発症した場合はその誘因を調べ、再発を防ぐことが重要
主な誘因:DKAの誘因「5つのI」
・Insuin:インスリン欠乏、インスリンの中断
・Infection or Inflammation:感染症や炎症
・Ischemia or Infarction:虚血や梗塞
・Intra-abdominal disease:膵炎、胆嚢炎
・Iatrogenic:医原性(IVH[中心静脈栄養]、ステロイド、薬剤性)
疫学:
DKAを発症する患者の多くが1型糖尿病患者→抗GAD抗体などはスクリーニング必要
SGLT2阻害薬使用中の患者は血糖<200mg/dLでもDKA発症例あり→SGLT2阻害薬は脱水助長する
高齢者や合併症が存在する場合には5%以上の致死率
症状:
口渇、多飲、多尿(多尿があっても脱水!!!)、倦怠感が出現→脱水増悪+代謝性アシドーシス→クスマウル呼吸+呼気アセトン臭、口腔粘膜皮膚乾燥→意識障害
病態:
脱水+インスリン不足+高血糖+代謝性ケトアシドーシス
検査:
ケトン体(尿でもOK)、血糖(尿糖でもOK)、pH、Lac、BE、HCO3-、Na、K、UN、Creなどを測定する
エコーでIVC評価
診断基準:
血糖値250mg/dL以上、重炭酸塩の低下(15mEq/L以下)、血中・尿中ケトン体の上昇を伴うアシドーシス(PH7.3以下)を認めればDKAと診断
重症度判定基準→血液pHとHCO3-と意識レベル(血糖値やケトン体ではない!)
治療:
とにかく脱水補正(4~5Lほど必要とされる)+インスリン静注+持続皮下注→入院が必要
Na補正(DKAでは低Na血症になりやすい)
K補正(インスリン療法で低下しやすいため途中から補充)
①脱水(+Na)補正:
生理食塩水の点滴を1000mL/時間(14~20mL/kg/時間)の速度で開始(高齢者は点滴速度は7~10mL/kg/時間と半分程度に減量)
②インスリン:
血糖値が50~70mg/dL/時で低下するよう、0.1単位/kg/時間の少量からシリンジポンプで持続静注(→浸透圧変化による脳浮腫予防のため)
③アシドーシス補正:
重炭酸塩での補正はpH<7.0の高度なアシドーシスの場合のみ行う(急激なpH補正は危険な場合があるので重症時のみ行う)
参考:
血清浸透圧(pOSM)=2(Na)+血糖/18+尿素窒素/2.8(Osm/L、正常値280~290)
DKAは高血糖+脱水+インスリン枯渇+ケトアシドーシス、HHSは高血糖+脱水+脱水+脱水→腎不全に注意!

ケトン体にはアセト酢酸、ヒドロキシ酪酸、アセトンの3種類がある。
病初期の重症度を反映するのはヒドロキシ酪酸
アセトンはすぐに蒸発し、呼気に排出される→アセトンだけでは病的とは言えない。
アセト酢酸はクリニック等でも定性的に測定可能だが、DKAの診断にはあまり有用ではない。
病態に関係するのは3-ヒドロキシ酪酸であり、これをPOCTで定量するのが最も有用。

アルコール依存症と各種代謝性疾患
アル中の救急要請=ビタミンB1を100㎎(アリナミンF50なら2A、F25なら4A)点滴静注する!(Wernickeなら500㎎は必要)
- アルコール多飲→ビタミンB1の大量消費+低栄養(K、P、Mgなど)に起因する多臓器不全をきたす
- B1投与前には採血でB1測定する→遮光が必要なため追加はできない
- ブドウ糖投与前に必ずビタミンB1投与する
- ビタミンB1欠乏の4大症状
- ①Wernicke脳症
- ②乳酸アシドーシス
- ③脚気心(wet beriberi)
- ④末梢神経障害(dry beriberi)
- ウェルニッケ・コルサコフ症候群(WKS):
- Wernicke脳症の古典的3徴として,①意識障害,②眼球運動障害,③歩行失調
- 脳の奥のほうの部位(脳幹部)に微小な出血が起こり、細かい眼の振るえ(眼振)が目の動きに制限が出る(眼球運動障害)、意識障害などの精神状態の変化、ふらつき(失調性歩行)といった様々な症状が急激に出現
→眼球運動障害、筋肉の動きの随意協調運動障害(運動失調)および錯乱が三徴
- MRI画像を撮影したとしても,鑑別にWernicke脳症が挙がっていなければ,視床内側や中脳水道の高信号といった特徴的な所見に気づかないこともある
- 永続的な記憶障害へと進展する
- 発症直後にチアミンを大量に点滴すれば回復することができるが、実際には見逃されることが多く、死亡率も10~17%と推計される
- 死亡例以外でも56~84%が記銘力障害や失見当識、作話を特徴とするコルサコフ症候群へ移行する
- 乳酸アシドーシス
- 救急外来で乳酸アシドーシスをみたら,ショックに代表される循環不全,腸管虚血,痙攣,薬剤などの関与を考えるが,ビタミンB1欠乏も忘れてはならない.これは解糖系がうまく回らないことを考えれば理解できる
- ビタミンB1に関しては,枯渇しやすい患者であれば躊躇する必要はなく,また敗血症では需要が増えるため,投与する選択で問題ない.
- 脚気心(beriberi heart):スリランカ語のberi=weaknessを意味する
- 脚気には末梢神経炎を主徴とするdry beriberiと高拍出量性心不全を主徴とするwet beriberiがある
- 近年、糖質摂取量の増加によるB1欠乏症が増加傾向にある
- 脚気心で高拍出量性心不全となる機序:
→末梢血管の拡張,末梢血管抵抗の減少と静脈還流の増大によるもので,末 梢血管の拡張は血管運動神経の鈍麻によるものと推測されている - 症状:
- 脚気心では浮腫、全身倦怠感、易疲労性、発汗、皮膚温上昇などがみられる
- Dry beriberiでは知覚,運動障害、腱反射(アキレス腱、膝蓋腱)消失がみられる
- アルコール性ケトアシドーシス(AKA):
- 血糖値の低いケトアシドーシスで病態はDKAに似る
- 発症の背景には,アルコール依存に伴う長期的な食事摂取不足による飢餓状態と,飲酒に伴う嘔吐・下痢や水分摂取不足,アルコール摂取に伴う抗利尿ホルモンの分泌抑制による脱水状態が存在する。
- 大量飲酒後の消化器症状により飲酒もできなくなると,アニオンギャップ開大性の代謝性アシドーシスを生じてAKAを発症する。
ビタミンB1(thiamine)は糖代謝に必須な補酵素(ちなみにB6はアミノ酸代謝に必要な補酵素)。
2020年版食事摂取基準では、ビタミンB1の一日の推奨量は、女性では18~74歳で1.1mg、75歳以上で0.9mg、男性では18~49歳で1.4mg、50~74歳で1.3mg、75歳以上で1.2mg
対して、ビタミンB1欠乏症時のビタミンB1投与量は100㎎と超高用量を用いる。
B1の含有量は製剤によりまったく異なるので、添付文書を確認する
たとえば総合ビタミンB製剤のビタメジン注(B1/6/12)にはチアミン100㎎も含まれている。
チアミン欠乏がある場合、他の水溶性ビタミンも不足していることが多いため、総合ビタミン剤での治療がより好ましい。
薬剤性のビタミンB1欠乏も報告されている
→フロセミド大量投与(水溶性ビタミンの尿中喪失)
脚気と日本人の歴史
精米技術が発達した江戸時代から第二次世界大戦前後に多発した
日本では1923年には26,797例の死亡が報告されている
陸軍軍医の石黒と森鴎外は脚気を細菌感染症と考えたが、海軍は食事が原因と考えていた
東大農学部の鈴木梅太郎教授が米糠(ぬか)から脚気予防に有効な成分としてオリザニンを抽出した→のちにチアミンであることが判明した
低カリウム性周期性四肢麻痺(HOKPP)
- 病型は麻痺型とミオパチー型に分類される
- 麻痺型:
低カリウム血症を伴う可逆性の弛緩性麻痺発作を特徴とし、多くの場合は対麻痺もしくは四肢麻痺にまで達するが呼吸筋や心筋は侵されない。急性の麻痺発作は通常、少なくとも数時間から時には数日間続く。生涯で一回しか発作を経験しない罹患者もいるが、たいていは毎日、毎週、毎月あるいはより稀な頻度で繰り返すことがほとんどである。主たる誘発因子は、高炭水化物食摂取や運動後の休息であり、珍しい例としては寒冷刺激で誘発された低カリウム性周期性四肢麻痺の報告もある。発作の間の期間は一定しておらず、カリウムやアセタゾラミドといった予防薬で発作間隔が延びることもある。発作の初発年齢は1歳から20歳と幅があり、最も発作の回数が多いのは15歳から35歳の間で、その後は年齢とともに発作回数は減少していく。 - ミオパチー型(25%):
進行性不可逆性の筋力低下が主に下肢に出現し、その結果下肢の運動耐性が低下する。その発症時期は一定していない。ミオパチー型は麻痺発作との相関はなく、それ自体が低カリウム性周期性四肢麻痺の唯一の症状であることもある。低カリウム性周期性四肢麻痺の罹患者は麻酔による周術期の筋力低下のリスクが高く、また、常染色体優性遺伝悪性高熱患者(MHS)ほどではないにしても、悪性高熱のリスクも有する。
鼻出血
鼻出血:TXA 500 mgをガーゼに染み込ませて使用
鼻出血と言えばアドレナリンガーゼ!と思っていた若かりし頃,とても衝撃的な論文を目にしたことを今でも覚えています。TXA含有ガーゼはアドレナリンに比較して10分以内の止血率を向上させ,ERからの離脱までの時間を短縮するという報告です。その後も,抗血小板薬常用者に対しても効果的であるという報告がされ,注目を浴びました。しかし,局所アドレナリンで止血できなかった鼻出血を対象にTXAの効果を検討したNoPAC試験では,前方パッキング必要率/再出血率/入院率などに有意差なしという結果に終わりました。ツッコミどころの多い研究なんですけどね。なお,NoPAC試験を含む8試験1299人を評価したメタ解析では,TXAにより早期止血達成率が3.5倍に高まり,24~72時間以内の再出血率が低下すると報告されました。TXAを鼻腔内に噴霧して鼻翼を圧迫するだけでも良いとされており,個人的には鼻出血にTXAはアリかなと思っています(→2023.06.12 週刊医学界新聞(レジデント号):第3521号より)
抗生剤投与量
eGFRとCcrの関係性
- eGFRは筋肉量が減少している患者(長期臥床など)で高めに推算される
- Crは尿細管で分泌されるため、CCrは若年者ではGFRより30%程高めに推算されるため若年者ではCG式によるeCCr×0.789で個別化eGFRに換算する
MEPM
- 50<CCR 1g 8q
- 10~50 0.5~1g 12q
- 10> 0.5g 24q
- 透析 0.5g 24q+透析後に0.5g
- CRRT 1~2g 12q
PIPC/TAZ ゾシン
- 50<CCR 4.5g 6q
- 10~50 2.25g 6q
- 10< 2.25g 8q
- 透析 2.25g 8q+透析後に0.75g
- CRRT 2.25g 6q
ABPC/SBT ユナシンS
- 50<CCR 1.5~3g 6q
- 10~50 1.5g 8q
- 10< 1.5g 12q
- 透析 1.5g 12q +透析後にABPC2g
- CRRT 3g 12q
MNZ
- 要禁酒(アンタブス効果がある)
- ワーファリンと併用注意
- bioavailability100%のため経口=静注投与
- 嫌気性菌に対する優れた活性あり
- 耐性化が起こりにくい
- 通常,成人にはメトロニダゾールとして 1 回 500mgを1日3回 又は 4 回経口投与する
- 肝代謝
- 末梢/中枢神経障害、髄膜炎に注意
CTRX
- 嫌気性菌への活性は弱い
- 低Alb血症では増量が必要
- 緑膿菌、ESBLには無効
腸球菌
- ABPCが第一選択
- セフェム系無効
- カルバペネム系無効
マルトフィリア感染症
- ST剤が第一選択(保険適応なし)内服=点滴だが点滴は水分が多くなる
- 第2選択はLVFXだが耐性化しやすい(LVFXは嫌気性カバーできないのでCLDMやMNZ併用)
ACLS
- 挿管するまでは30:2を5サイクル、挿管後は2分間のCPRでリズムチェックを繰り返す
- 薬剤投与は2回目のリズムチェック時(4分おき)に行う
- タイマーを2個用意すると便利(1個は2分サイクルのリズムチェック用、1個は4分サイクルの薬剤投与用)
- 心エコー、レントゲン、採血、血ガスで原因評価と治療
- 電解質やアシドーシス、低血糖などがないか
- 心嚢液→大動脈解離による心タンポナーデを疑う
- 肺塞栓→Dshape、頸静脈怒張、IVC怒張
肺塞栓
- 造影CT前にエコーで右心負荷所見を探す
短軸、四腔像で右室拡張、左室Dshape
IVC怒張
頸静脈怒張
- 右心負荷所見→頸静脈怒張
- 下肢浮腫
※心エコー基本断面(呼気の方が肺がしぼんで見やすい)
https://www.youtube.com/watch?v=bJdoU0oxQxg&t=5s
①左室長軸像→胸骨左縁、第2肋間を上から下げてくるといい位置が出てくる
②短軸(大動脈弁レベル→乳頭筋→心尖部)
③四腔像
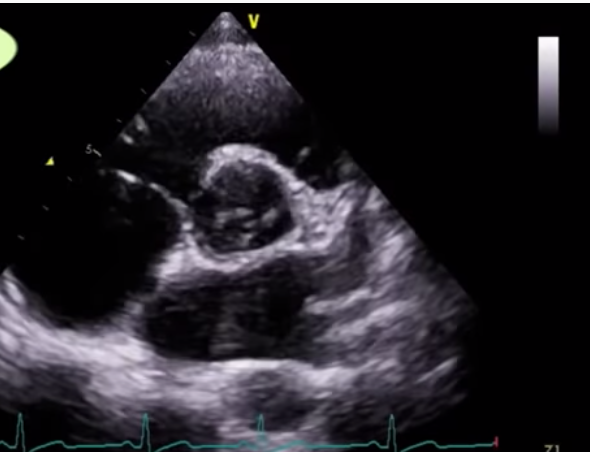
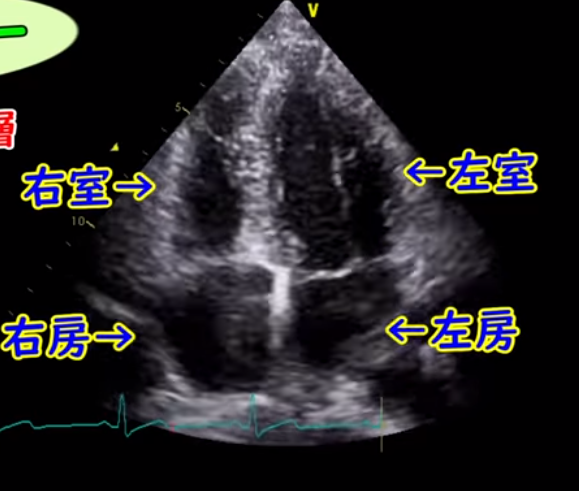
ACS
- モニタ心電図は不整脈はわかるが虚血はわからない
- II/III/F→左室下壁梗塞、RCA領域、徐脈性不整脈出てくる
- 1/2/3/4→前壁梗塞、LDA領域
- I/L/5/6→左室側壁、LCX領域
- resiprocal changeがあればより確信が得られる
気道熱傷
- 火災でJCSIII-300なら挿管+気管支鏡で精査
- 閉鎖空間での火災はCO中毒疑う→高濃度酸素投与(リザーバーマスクで搬送)
- COHb>60%は低血圧、昏睡、呼吸不全→死に至る(喫煙者は4-5%程度)
- CO濃度には静脈血サンプルを用いてもよい(SPO2があてにならないため動脈がベター)
- パルスオキシメーターは正常ヘモグロビンと一酸化炭素ヘモグロビンを区別できない
- COの消失半減期は室内気の吸入では約4.5時間、100%酸素では1.5時間
肺エコー
- 肺炎と無気肺はエコーで鑑別できない(肺炎や無気肺は肺の中の含気が少なくなるため実質臓器のような画像にみえる(tissue-like sign)。肺炎の 場合,含気のなくなった肺の中に呼吸に合わせて高輝 度な気体成分が気管支内を移動するdynamic bronchogramが確認できることがある
- 肺炎は痰に細菌が確認された状態
- 無気肺は気管支が閉塞し含気が減少した状態
- 肺炎と無気肺は併存しうる
低K血症
- KCL20mL+生食20mLを4~6mL/hrでCVから持続静注可能
高K血症
- ラシックス
- GI療法
- 10%塩化カルシウム:K>7mEq/LのときVFの危険性を減らすため、10mLを2~5分で静注
- 血液透析
雑多なtips
- 造影剤の除去効率はHD>>CRRT
- MRSA腸炎は存在しない(→CD腸炎の誤認)
- 腸球菌→セフェム自然耐性、カルバペネムも×、ブロードならPIPC/TAZ
- ETCO2値≧10mmHgはROSCと関連 (CPR20分後ETCO2 <10 mmHgのROSC率は0.5%)
PADIS
- ICU患者の長期予後改善を目的とした介入項目
- Pain:痛み
- Agitaion/sedation:不穏/鎮静
- Delirium:せん妄
- Immobility:不動化
- Sleep disruption:睡眠障害