循環器内科
心臓・血管系に関するガイドラインだけで50個もある(日本循環器学会HPより)!
日本人における死因の第2位は心疾患( 14.8%)
日本における心不全患者は2020 年には 120 万人に達する
心筋梗塞
Trop-T定性迅速テスト(検出感度>0.1ng/mL)
ラインが薄くても陽性判定(TropT陽性化までACS発症から3~5時間必要)
定性検査陽性の場合、心筋トロポニンTの濃度が0.1 ng/mL以上であり心筋傷害の存在を示す
陰性の場合、心筋トロポニンTの濃度が 0.1 ng/mL 未満であり、心筋傷害が起きていないと考えるが、心筋卜ロポニンTの遊出動態により、梗塞発症の初期では陰性を示すことがあり、心筋梗塞の疑いがあるときには、時間をおいて再検査することを検討
高感度Trop-T定量検査(検出感度0.014ng/mL=定性の約1/10まで検出可能) 112点
急性心筋梗塞におけるカットオフ値は、0.100ng/mL以下(定性検査と同様)
急性心筋梗塞、心筋炎、狭心症で陽性を示す
Trop-Tは正常化するまでに1~2週間かかる
数値の絶対値がけっこう重要で、軽度上昇ならACSではないと専門医が判断していた(少なくとも緊急PCI適応はないと判断したのだろう)
Trop-Tは腎機能の影響を受けるが、CKDでもTrop-T陰性の場合はACS陰性と判断してよい(逆は言えない)
→在宅医療現場では心電図とTropT迅速キットは導入したいところ
平滑筋には存在せず,しかも構造が心筋と骨格筋とで異なるため,両者を明確に識別することが可能となり,現在最も特異的な心筋障害のマーカーと考えられている
心筋炎, 心筋梗塞, 腎不全で高値となる

- STBT(症状から治療までの時間)<90分が予後良好
- ST上昇がないACSもある(NSTE-ACS):LCXやLMT、多枝病変の場合など→TTEやTropTなども
- 胸痛や背部痛、心電図異常の原因として大動脈解離や肺塞栓が鑑別にあがる→造影CTで鑑別

動脈硬化病変“プラーク”は、中心に脂質コアを含み、表面は線維性被膜で覆われている。心筋梗塞、不安定狭心症と虚血性心臓突然死の多くは、プラークの破綻を契機として、冠動脈内腔に血栓が形成され、内腔が閉塞ないし亜閉塞をきたすと考えられ、総称して急性冠症候群(acute coronary syndrome: ACS)と呼ばれている。プラーク破綻は、線維性被膜が破れ、脂質成分が血液と直接触れることで血栓が形成される“プラーク破裂”と、線維性プラークの表層がびらん性変化に伴って血栓が形成される“プラークびらん”に大別される。急性冠症候群(ACS)の70-80%は、プラーク破裂に伴うもので、20-30%はプラークびらんに伴うことが報告されている。
右室梗塞
右冠動脈の近位部が閉塞することで、左室の下壁領域が壊死に至るだけでなく、右室の壁運動が障害された結果、右室から肺動脈への拍出が出来なくなり、左室への潅流が減って血圧低下に至る
下壁や後壁梗塞の25%~50%に合併する
→肺うっ血は目立たないが、頸静脈などの体循環のうっ血が目立つ
肺うっ血はないためSPO2は良好なのが右室梗塞の特徴
右室梗塞の初期対応は?とうぜん緊急PCIだが・・・
右室梗塞では前負荷軽減させる治療(利尿薬や硝酸薬、モルヒネ)を使用するのはショックを増悪させるリスクがあり、逆にVolume負荷を行う必要がある
さらに右室から肺動脈への拍出を増加させる目的でカテコラミン(ドパミン、ドブタミン)を使用する
- 右室梗塞の診断手順:
- 頸静脈怒張あり
- 心電図で下壁梗塞パターン(Ⅱ、Ⅲ、aVF)でのST上昇
- 次にV1のST上昇がないかを確認→V1のST上昇は右冠動脈近位部の閉塞を示す
- V3~V6の電極を、胸骨を挟んで反対側に付け替えて心電図を記録し、ST上昇があれば確実

ACS=すぐに全例にMONA(モルヒネ、酸素、ニトログリセリン、アスピリン)はダメ!
右冠動脈閉塞のため、下壁梗塞だけでなく、右室梗塞を合併している危険性あり(25-40%)
右室梗塞では静脈還流不全がおきるため、モルヒネ、ニトログリセリンを使うと、さらに静脈還流不全が悪化し、ショックを起こすこともある
大動脈解離
- 【偽腔開存型】
- エントリーから流入した血液がリエントリーから流出しているタイプで、偽腔の中に血流がある状態
- 【ULP型】
- エントリーから偽腔に突出する血流(ULP)は確認できるが、流入した血液はリエントリーから流出せず、ほとんどが血栓(血の塊)となっているタイプ
- 【偽腔血栓閉塞型】
- 偽腔が血栓で完全に塞がっていて、血流がないタイプ
VTE(肺塞栓/DVT)
- Wellsのスコアリングシステム
- ガイドライン→問診でVTE疑い→DDでスクリーニング→陽性なら造影CTというフローチャート
- ERでは心エコーで右心負荷所見をさがす(右室拡大→D-shape)
心不全総論
心不全(とくにHFrEF)には非ジヒドロピリジン系CCB(ワソラン、ヘルベッサー)は望ましくない
心不全とはポンプ失調、うっ血に伴う症状が主体、がん同様、進行性の病気で元には戻らない
急性心不全の初期対応→CSに基づく治療
慢性心不全→心不全ステージの進行を抑える=ステージCの維持
ステージCのうち、エビデンスが豊富なのはHFrEFのみ(HFmrEF、HFpEFは研究が不十分)
ステージD(終末期心不全と言える)→症状軽減を目的とした緩和治療
- 急性・慢性心不全診療ガイドライン(2017年改訂版)
- フォーカスアップデート版急性・慢性心不全診療(2021年)→ARNi、SGLT2阻害薬、イバブラジンについて追加
- 病態:心ポンプ機能が低下し,主要臓器への灌流不全やうっ血に基づく症状や徴候が急性に出現した状態
- 症状:うっ血に伴う症状が主体
- 右心不全、左心不全のいずれかで発症するが、最終的には両心不全に至る
- 推計患者数は約200万人で, 一度心不全の診断を受けると5年生存率は50%
- 血行動態バランス調整には自律神経系と体液性因子が関与している(神経体液性因子)
- レニン-アンジオテンシン-アルドステロン系(RAA系)の過剰活性が心不全進行にきわめて重要
- RAA系は循環不全に対する代償機構の1つとして活性化されるが, 不全心の慢性化に伴い過剰活性が遷延し, 逆に心不全の進行を誘発する
- 心不全には必ず原因がある
→虚血性心疾患、心筋症、心膜炎、弁膜症、大動脈疾患(ASなど)、高血圧、肺疾患、内分泌疾患 - 急性増悪→身体機能低下を招くので、急性増悪や入院させないような管理が求められる
- 心不全はがんと同様、進行性の病態であり、必ず緩和ケアが必要(がん同様、早期からの緩和ケア介入が必要)
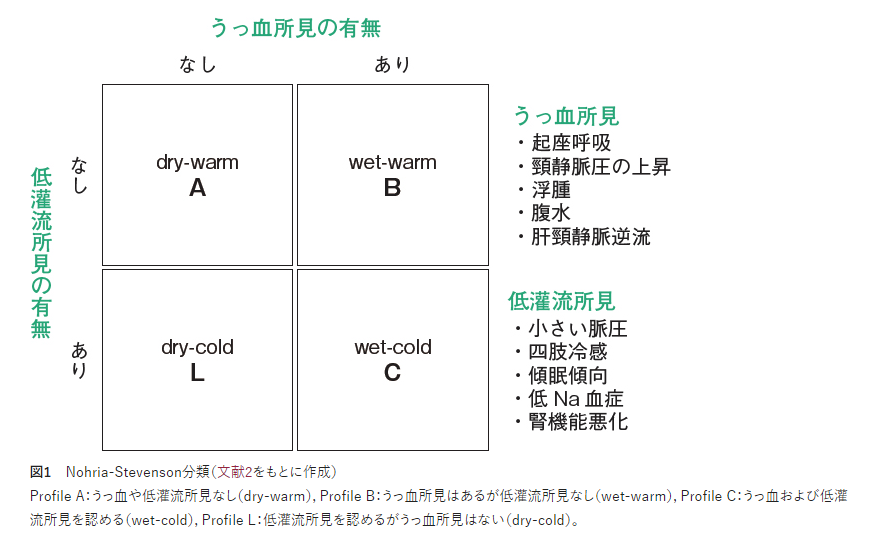
急性増悪時の診断(Nohria-Steveson分類)
肺の胸膜付近の末端部は血管陰影が見えないのが正常
→末梢まで血管陰影が見えるのがうっ血所見=カーリーBライン
カーリーBラインのみならまだ軽症→末梢血管拡張→間質への水分逸脱→気道狭窄+低酸素血症→肺胞内に水分滲出→さらなる低酸素血症の進行と泡沫様痰→陽圧換気の適応


ProfileCが最重症
急性心不全の初期対応→CSに基づく治療
CS1の心不全治療
まずは酸素とフロセミド(wetでない心不全は少ない)
以前高血圧持続(>140mmHg)なら硝酸薬を追加
それでもだめならNPPV
- CSの基づく初期対応ではサクッと血圧で分類する→SBP>140mmHgならCS1という感じ
- 急性心不全においては救急搬送から60分未満にフロセミドが投与された早期治療症例は他の交絡因子に独立して院内死亡率が低値であった
- 1回静注投与で満足な利尿効果が得られない場合には,むしろ持続静注のほうが有効な場合もある
- 急性心不全に対するトルバプタンは短期的には自覚症状や体重を改善したが投与後の生命予後を改善するには至らなかった
- 硝酸薬はけっこう血圧下がる→第二選択で使用する方が安全



HRはある一線を越えると,心臓の拡張も収縮も悪くする
その一線は,心機能低下例であればあるほど,限界が早く来る
必要以上のHRは心収縮と心拡張の悪化を起こすだけでなく,心筋虚血の原因にもなる
→たとえ洞性頻脈であっても,一線を越えたHRは,循環にとっては害悪でしかない
AFtachycardiaを伴う心不全のレートコントロールにはβブロッカーやジギタリス製剤を投与する
βブロッカーの安全域はβ1選択性の違いからカルベジロール>ビソプロロ-ル
心拍数>130bpmはレートコントロールの治療適応、目標値は安静時<80bpm、労作時<110bpm
長期リズムコントロールを行う場合は、アミオダロンが第一選択、だめなら除細動かアブレーション(Naチャネル遮断薬は禁忌)
心不全合併の心房細動では、抗凝固療法は禁忌のない限り必須!!
呼吸補助療法→ASV:Adaptive servoventilation
- 呼吸補助療法は、慢性心不全に併存する睡眠呼吸障害を治療対象として用いられる
- 治療抵抗性心不全の呼吸困難などの症状が持続する重症心不全愚者においてASVを使用した呼吸補助療法が、症状の改善をもたらす
- ASVは、心臓の機能が低下している慢性心不全の患者さんが、在宅で使用する人工呼吸器
- ASVもCPAPも、睡眠時の無呼吸を防ぐために有効な装置
- CPAPがいつも一定のリズムで酸素を送り込むのに対して、ASVは使用者の呼吸に合わせて適正な量の酸素を送り込む(呼吸と同調する)機能を持つ
- ASVは、専用のマスクを装着すれば自動的に作動する仕組みになっている
→後負荷軽減+前負荷軽減作用があるが、予後改善効果は証明されておらずルーチンでは投与しない
塩酸モルヒネは中枢性に働き,交感神経緊張の著しい亢進を鎮静することによって細動脈や体静脈を拡張し,心拍数の減少により心筋の酸素需要は減少する
細動脈の拡張により後負荷は軽減し,また静脈系の拡張により静脈還流量は減少し,肺うっ血は軽減する
血管の拡張が過度になると血圧は低下するため,低血圧,徐脈,高度房室ブロックを合併する患者では注意を要する→右心不全ではショックを増長するので禁忌
呼吸器系に対しては,呼吸回数の減少や呼吸仕事量の抑制により酸素需要を減少させるが,炭酸ガスに対する呼吸中枢の反応性低下により呼吸抑制が起こりやすく,脳内出血例,意識低下例,気管支喘息例,COPD例には原則として投与しない
予後に対する効果については,後ろ向き研究ではあるが,かわらない,もしくは悪化させると報告されておりルーチンでの投与は推奨されない
心不全の症状
心不全ステージ分類(厚労省および日本心不全学会)

慢性心不全の治療総論
HFrEF→収縮不全が主体→標準的心不全治療の適応 EF<40%
HEpEF→拡張不全が主体→標準治療が確立されていない EF>50%

慢性心不全の治療各論
治療の目的を考える→予後改善なのか、緩和治療なのか
心不全の予後改善を目指す治療は?
急性・慢性心不全診療ガイドライン 2021
β遮断薬・MRA・ARNI・SGLT2阻害薬の4つの薬剤は、これからの心不全治療の中心を担う4剤であり、「fantastic four」と総称されている
症状緩和を目的とした治療は?
酸素、利尿薬、血管拡張薬、モルヒネ、抗不安薬、経口強心薬(4種類)、ジギタリス、非薬物量療法
- 現時点でもっともエビデンスがあるのはARNi+βB+MRA、費用対効果が高いのはACEI+βB(±MRA)
- HFrEFに対するエビデンスはARNi ≧ ACE阻害薬 ≧ ARB
- ARNI(アーニー)はエンレスト1種類のみ→調節性に乏しい(全症例400mg/日を目指す)、ARNIのみ利尿作用がある→https://note.com/doctorpooh/n/n3b6ba9b3ec7dに詳しい
- MRAの上乗せ効果はHFrEFのみでしかエビデンスなし(HFpEFでは投与必要なし)
- SGLT2阻害薬(ジャディアンス、フォシーガ、効果は同等)もDM並存の有無に関わらず心不全予後改善効果あり、特にDM合併の心不全にはDPP4阻害薬よりもSGLT2阻害薬の方が予後良い(SGLT2阻害薬の心臓に対する良好な作用機序に関しては、心筋のエネルギー効率を改善して、収縮力を改善する、炎症を抑えて、心筋の線維化を抑制する、微小循環を改善するなどさまざまな機序が提唱されているが、主要な役割を果たす効果についての一致した見解はまだない)
初回治療の場合は、少量から導入して最大用量まで漸増していく→目安は3か月程度
循環器DrはADHFに対してACEI+SGLT2阻害薬+ループ利尿薬(アゾセミド60㎎)+MRA(スピロノラクトン半錠)から導入していた
経口強心薬・ジギタリス製剤、アミオダロン、血管拡張薬、トルバプタンなど
経口強心薬:
重症心不全による血圧低下や末梢循環不全を伴う患者に対して一時的に使うべき薬剤という位置づけ
→複数の大規模臨床研究にて心不全患者の予後を悪化させる結果が示されているため
心不全ガイドラインでは
「NYHAⅡ度以上で、他の薬剤で症状の改善が得られない場合、QOLの改善のため不整脈の増悪に注意を払いながらピモベンダンを追加してもよい」
硝酸薬:
未治療の虚血領域があるなら継続も可、OMIで有意狭窄ないなら終了でよい
QOL改善を目的とした短期投与が望ましい
長期投与の場合には不整脈の出現に注意する
- 経口強心薬:
経口強心薬の使用は短期間にとどめできるだけ早期に漸減、中止する
慢性心不全治療ガイドライン(2010年改訂版)においても無症状の患者に対して経口強心薬を長期投与することはクラスⅢ(禁忌)
強心剤の点滴からの離脱(クラスⅡa)やβ遮断薬導入時の補助(クラスⅡb)のために一時的に使用する
通常β遮断薬導入時にはβ刺激作用を有する薬剤ではなくPDE阻害薬(=ピモベンダン)を使う- カテコラミン類似薬→心不全ガイドラインでの記載なし
- ドカルパミン(商品名タナドーパ)
- デノパミン(商品名カルグート)
- PDE阻害薬
- ◎ピモベンダン(商品名アカルディ)
- ピモベンダンにはPDE阻害作用に加えCa感受性増強作用がある
- PICO trialではピモベンダン(2.5mg/日と5mg/日)投与により運動耐容能は改善したものの死亡率も増加する傾向がみられた
- 処方例:
1.25mg/日(分1)を開始し、効果が不十分な場合に限り2.5mg/日(分2)へ増量
そして目的を達成できたら速やかに漸減、中止する
5mg/日以上の投与は個々の症例でリスクとベネフィットを熟慮して判断する
- ベスナリノン(商品名アーキンZ)
- ◎ピモベンダン(商品名アカルディ)
- カテコラミン類似薬→心不全ガイドラインでの記載なし
- ジギタリス製剤:
- 心房細動などにおける心拍数コントロールを目的に,0.125~0.25 mgを緩徐に静注し,中毒に注意しながら適宜使用する方法が一般的であり,急速静注飽和療法は現在では用いられることが少ない
- ジギタリス投与の禁忌例として,徐脈,第2~3度房室ブロック,洞不全症候群,WPW症候群,閉塞性肥大型心筋症,低カリウム血症,高カルシウム血症、心アミロイドーシスがあげられる
- ジギタリス製剤は半減期の長い腎排泄の薬剤で,かつ血中濃度の治療域がきわめて狭い
- ジギタリス製剤は P-糖蛋白質を基質とするため,アミオダロン,ベラパミル,利尿薬(スピロノラクトン,トルバプタン)などの薬剤においては血中濃度上昇の恐れがあるため併用に注意を要する
- 心不全合併の心房細動のレートコントロールにはワソラン、ヘルベッサーはガイドライン上、禁忌
→ジギタリスまたはβブロッカー(カルベジロールがよりマイルドに作用し安全域高い、がっつり下げるならビソプロロ-ルの方がβ1選択性が高く効果的)、アミオダロンを使用する
- トルバプタン(サムスカ):
- 長期投与について明確なエビデンスはなく、継続の可否に迷うようなら専門医に相談すべき
- 血管拡張薬:
- 硝酸薬→投与の是非はPCIで未治療の心筋虚血があるかどうか?がすべて
- 体血管は静脈>動脈に拡張する、冠動脈拡張作用も有する
- 一般的には急性心不全に対する治療薬と考える、最も良い適応はACSによる急性心不全
- 急性左心不全による重症肺水腫では有効性は硝酸薬>>利尿薬
- 収縮期血圧90mmHg未満の心原性ショック患者に対する血管拡張薬の使用は控えるべき
- 血圧高値,心筋虚血を合併する患者,僧帽弁逆流症がある患者などは血管拡張薬が望ましい場合がある
- 慢性心不全の急性増悪のように体液貯留によるうっ血が著明の場合には利尿薬主体の治療を行う
- ニトログリセリンや硝酸イソソルビドの舌下やスプレーおよび静注投与が,急性心不全や慢性心不全急性増悪時の肺うっ血の軽減に有効である
- 作用機序:
低用量では静脈系容量血管を,高用量では動脈系抵抗血管も拡張し,前負荷軽減効果(肺毛細管圧低下)および後負荷軽減効果(末梢血管抵抗低下に伴う心拍出量の軽度上昇)を発現する - 副作用:
硝酸薬の副作用として,血圧低下と肺内シャント増加に由来する動脈血酸素飽和度の低下があげられる
また,静注投与に伴って早期から耐性が発現する
- ニコランジル(シグマート):
- 硝酸薬にくらべて薬剤耐性を生じにくい
- さらに,過度な降圧をきたしにくい
- 心筋梗塞急性期におけるニコランジル投与によって,梗塞サイズならびに心臓死および心不全入院についてプラセボ群と有意差を認めなかった
- カルペリチド(ハンプ):
- 血管拡張作用,ナトリウム利尿効果,レニンやアルドステロン合成抑制作用などにより減負荷効果を発現し,肺うっ血患者への適応とともに,難治性心不全に対してカテコラミンなどの強心薬と併用される
- 急性心不全におけるカルペリチド投与については,他の血管拡張薬と同様,予後改善効果は確立されておらず,今後有効な患者の選択が重要である
- 投与初期に血圧の低下を生じることがあるので,投与開始の際には低用量(0.025~0.05 μg/kg/分[場合により0.0125 μg/kg/分])から持続静脈内投与する
- 重篤な低血圧,心原性ショック,急性右室梗塞患者,脱水症では禁忌である
- 硝酸薬→投与の是非はPCIで未治療の心筋虚血があるかどうか?がすべて


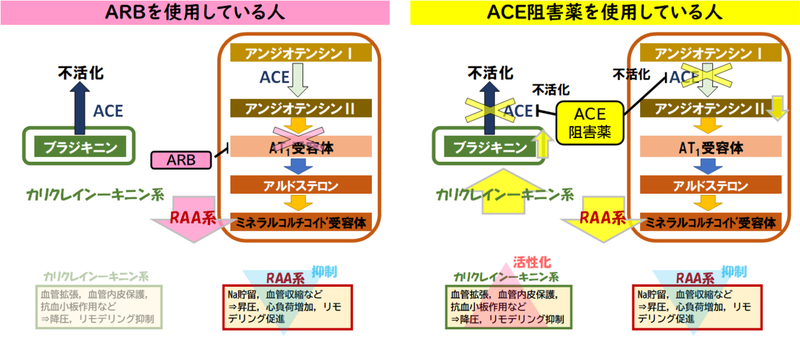
- 降圧効果:日本高血圧学会のガイドラインではいずれを優先して推奨するような記載はなく対等
→降圧効果は同等、薬価はARB>>ACEI、ACEIの問題は空咳がでることくらい
ACEIの保険用量は少ないためACEIは降圧効果が出ないと思われがち(→イミダプリル(タナトリル)やペリンドプリル(コバシル)が推奨) - 心不全:日本循環器学会のガイドラインでは,「ACE阻害薬が忍容性の点で使用できない場合にARBを用いるべき」→両薬剤のエビデンスの違いがある
- 心不全を合併していない心血管疾患高リスク症例のメタ解析(J Am Coll Cardiol. 2013 Jan 15;61(2):131-42.)
ACE阻害薬→心筋梗塞,脳卒中,全死亡,心不全新規発症,糖尿病新規発症を有意に抑制
ARB→脳卒中,糖尿病新規発症のみしか抑制しなかった - BPLTTC試験(J Hypertens. 2007 May;25(5):951-8. )
ACE阻害薬はARBより9%有意に冠動脈イベントを抑制 - 心疾患治療においては,ARBはACE阻害薬にエビデンスで劣る
- 出典:循環器Drぷーさんのブログ https://note.com/doctorpooh/n/nc1991c2fdd8d
MRAに分類される薬剤は①ミネラルコルチコイド受容体(MR)への選択性、 ②薬剤構造 (ステロイドor非ステロイド骨格)の2点から第1~第3世代に分類される。
第一世代に分類されるアルダクトン®AはMRへの選択性が低く、 アンドロゲン、 グルココルチコイド、 プロゲステロン、 エストロゲンなどの各受容体も阻害する。
MRAの利尿効果はごくわずか(Na再吸収の1~3%しか担っていない)→K保持性利尿薬と呼ぶには不適。
MRAの心不全予後改善効果は利尿作用によるものではなく、ACEI/ARB開始後に生じるアルドステロンブレイクスルーである→唯一の対策はACE阻害薬/ARBにMRAを併用すること
MRAのうち、心不全に適応があるのはアルダクトンとセララ
セララはアルダクトンに比べて利尿効果が少なく、血圧降下が強く、女性か乳房が少ない
心不全に対するMRAの使い分けもガイドラインには明記されていない

アルドステロン系は生物が海から陸へ上陸した際に、陸上生活に適応するために進化した。アルドステロンの過剰発現は心臓や腎臓の肥大や線維化、リモデリングの促進、あるいは酸化ストレス発生やアポトーシス誘導をもたらし、また血管平滑筋の収縮増速作用、線維化促進や内皮機能の低下、炎症反応の惹起作用をきたす。
心不全ガイドラインでは
COPD+HFrEFにおいてはHFrEFに対する標準治療(βブロッカー含む)+COPDに対するLABA+LAMAの吸入療法を併用することが推奨されている
COPD+HFpEFにおいてはCOPD治療を優先する
気管支喘息+HFrEFに対するβ1選択性の高いβB(=ビソプロロ-ル)の投与はIIaで推奨される
気管支喘息発作時のSABA使用においては、心不全の増悪に注意する
呼吸困難時におけるCOPDと心不全の鑑別にはNT-proBNPが有用
→https://www.medsi.co.jp/Download_files/CardiovascularDrugFile2Ep236-241.pdfに詳しい
喘息と心不全のどちらがより重症かにもよるが、β1選択性が高いII類薬は気管支喘息、冠攣縮性狭心症の患者でも使用可能(慎重投与)
心不全治療に対し保険適応下で使用できるβ遮断薬は現在2種類(その他のβBは使用できない)
カルベジロール(アーチスト)→αβブロッカー(=β1非選択性)のため、喘息禁忌!
ビソプロロール(メインテート、ビソノテープ)→β1選択性のため、喘息でも使用可能
カルベジロールは肝代謝、ビソプロロールは一部腎代謝→カルカン・ビジンで覚える

内因性交感神経刺激(intrinsic sympathetic activity: ISA):
→交感神経興奮時にはβ遮断作用を呈し、非興奮時にはβ刺激作用をもつことを意味し徐脈を起こしにくい
ISA-の方が好ましいとされている
膜安定化作用(membrane stabilizing activity: MSA):
→膜を安定化し、高用量で活動電位の立ち上がりを抑制することらしいが、実診療ではどうでもいいらしい
Q.では心不全患者にβ刺激薬の吸入薬を使用するのは安全か?
A.吸入β刺激薬は主要心血管イベントリスクを上昇させる
喘息患者において
β2刺激薬はMACEリスク(=心血管イベント)と関連していなかった
COPD患者において
LABA(ハザード比2.38、95%CI 1.04-5.47)、SABA(ハザード比2.02、95%CI 1.13-3.59)、ICS/LABA(ハザード比2.08、95%CI 1.04-4.16)使用者はSAMA使用者と比較してMACEリスクが増加
- ホクナリンテープ(ツロブテロールテープ):
- 添付文書上、心疾患に禁忌ではない
- β2選択制が最も高いので、心疾患にも使用しやすい

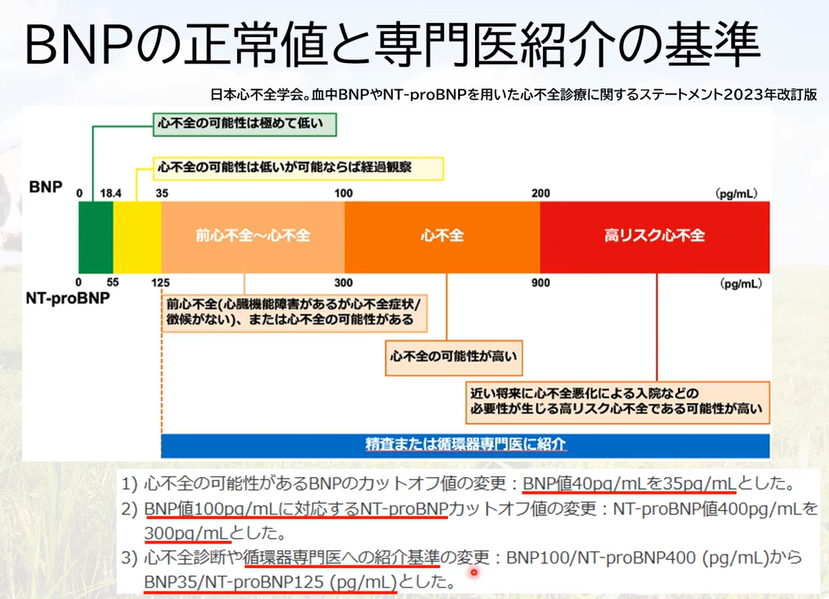
- NT-proBNPが上昇する因子:加齢、腎機能障害、貧血、全身炎症
- NT-proBNPが低下する因子:肥満
- 心不全の重症度を鋭敏に反映(ANP < BNP < NT-proBNP)
- ANPとBNPはそれぞれ心房性優位、心室性優位に分泌される
- BNPやNT-proBNPは、主として心室にて、壁応力(伸展ストレス)に応じて遺伝子発現が亢進し、速やかに生成・分泌される。両ペプチドとも心室のみならず心房からも10%ほど分泌されるため、心房細動などでも軽度上昇する
- ともに心臓から分泌されるホルモンで、利尿作用、血管拡張など、心臓に対する負荷を軽減する
- ANPやBNPの健常人の血中濃度は極めて低値だが、急性および慢性心不全患者では重症度に比例して増加し、特にBNPは、病態に応じて鋭敏に反応するため、心不全の診断または病態把握に広く用いられる。
- 症状のない早期心不全でも血中濃度が上昇していることから、最近は心不全のスクリーニング検査としても注目され、人間ドックや検診にも用いられている。
- NT-proBNPは、BNPと同じくBNP前駆体から分解されて生じるホルモンで、心不全患者で著明に上昇し、診断精度も同等で血清検体で測定でき、採血後の検体での保存安定性も良好なことから、他の生化学項目と同一採血管での測定や追加検査も可能
- BNP、NT-proBNPともに腎機能の低下に合わせて血中濃度が上昇する
- BNPとNT-proBNPは1:1で分泌される
慢性心不全ステージDに対する緩和治療
緩和治療およびACPはステージCから病状と患者の抱える苦痛に合わせて提供されていくものであり,ステージDを迎えてから開始するものではない
人生の最終段階で苦痛を抱えながら生を終えることは,患者及び家族のQOL及びQOD(qualityof death)を高度に低下させるものであり,心不全薬物療法の確立は喫緊の課題
- https://www.jstage.jst.go.jp/article/naika/109/2/109_240/_pdf#:~:text=%EF%BC%8A%EF%BC%8A%E5%BF%83%E4%B8%8D%E5%85%A8%E3%81%A7%E3%81%AF%E4%BF%9D%E9%99%BA,%E3%81%A7%E3%81%AE%E4%BD%BF%E7%94%A8%E3%82%92%E8%A6%81%E3%81%99%E3%82%8B%EF%BC%8E
- https://www.jstage.jst.go.jp/article/yakushi/140/7/140_19-00237-4/_pdf
- 2021年改訂版 循環器疾患における緩和ケアについての提言(日本循環器学会、日本心不全学会合同)
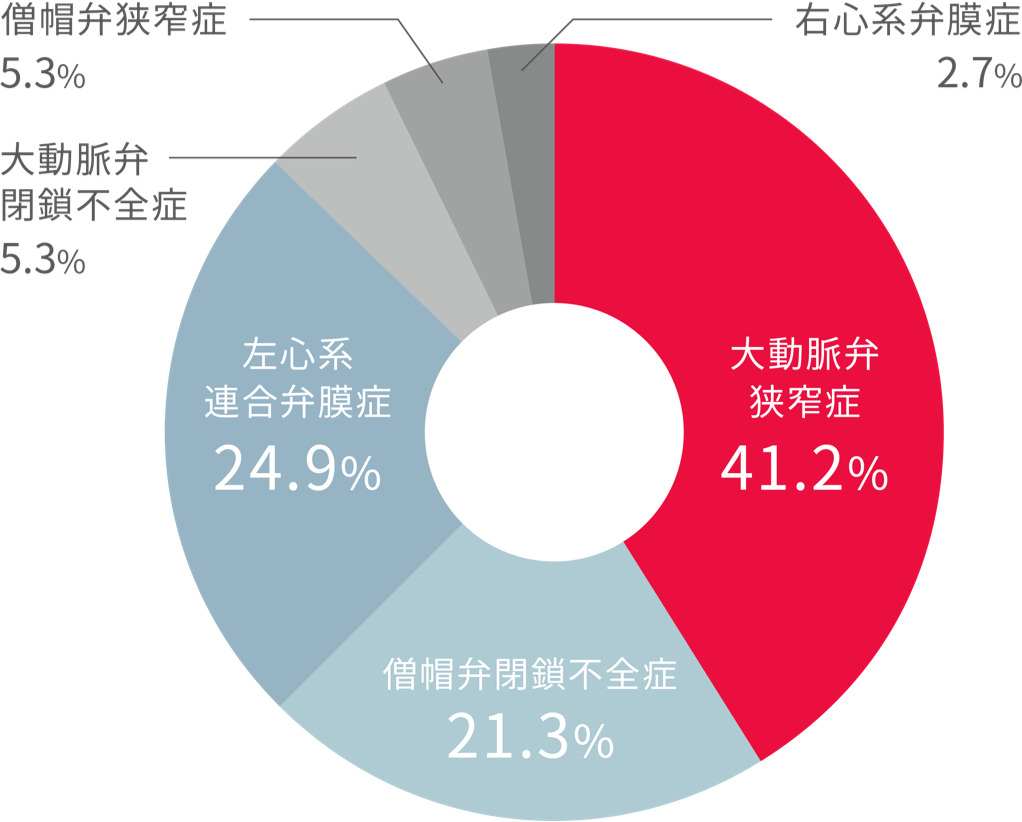
心臓弁膜症
頻度順にAS>MR>AR>MS
AS
有病率は後期高齢者の13%で日本では284万人(重症は約56万)
高齢者ASでもっとも多い原因はA弁の石灰化
有症状ASの予後は悪性腫瘍とほぼ同じ

※低流量低圧較差AS(low flow,low gradient AS)→重症化し心不全をきたすとPGはむしろ減少することがある

SVI; Stroke volume index. (1 回心拍出量係数) 1 回心拍出量を体表面積で補正した値
- 疫学:
- 有病率は後期高齢者の13%で日本では284万人以上いるが、治療を受けているのは2万人/年
- 症状:
- 息切れ
- 胸の痛み、重苦しさ(狭心症)
- 疲労
- めまい、失神
- 活動範囲の減少
- その他(頻拍または不整脈、動悸)
- 身体所見・検査:
- 収縮期駆出性雑音
- Ⅱ音が小さいか、または聴こえない
- 他に頸動脈の立ち上がりが遅い等の身体所見
- 左室機能障害が進行すると収縮期雑音が小さくなるため、収縮期雑音の強弱のみの判断では、病態の重症度を見誤る可能性がある
- 心エコーによる重症度分類
- BNP→無症候性重症ASにおける症状出現や心血管イベントを予測しうるためフォローアップに適している
- 予後:
- 狭心症状が出ると平均5年、失神だと平均3年、心不全だと平均2年の余命→重症化前の早期治療が重要
- 悪性腫瘍と同程度の5生率
- ASは心臓の出口の障害が引き金となり、その手前すべてが障害されていくために予後不良となる
- 治療成績:
- 弁膜症ガイドラインにも薬物治療の記載なし→治療法は手術のみ
- 年間に1万人がTAVI(=TAVR)、1万人がSAVRを受けている
- TAVIは導入から10年を過ぎ、現在はSVARと同程度行われている
- 弁膜症治療のガイドラインでは治療法選択における年齢のおおまかな目安として、80歳以上はTAVI、75歳未満はSAVR

心臓が一瞬とまる収縮末期または拡張中期と言われる時期のボリュームデータを集めて画像を構築する手法
リウマチ熱とは、A群溶血性レンサ球菌(溶連菌)に対する免疫反応によって生じる炎症性の合併症の1つ
溶連菌感染症は治療せずに自然治癒することもあるが、治療を行わなかった場合に、治癒してから通常2~3週間後に関節や心臓、皮膚、神経系に炎症が起こることがある
この溶連菌に対する抗体による自己免疫性合併症がリウマチ熱で、さまざまな部位に炎症が生じる結果、発熱に加えて関節痛や胸痛、発疹、不随意運動など、炎症部位に応じた症状がみられるようになるが、最も問題になるのが心臓弁膜症でリウマチ熱患者の50〜60%に発症する
ペニシリンによる抗菌薬の導入により、1980年代では、200〜400分の1の発生数に激減しているが、発展途上国ではいまだにリウマチ熱の発生頻度は高い
現在、日本におけるリウマチ熱の年間報告数は数例と非常にまれな合併症である
発症者は子どもに多く、特に5~15歳くらいによくみられる
心房細動
80歳以上の高齢者にはリクシアナ15mg(エドキサバン)の有効性、安全性が高い
ELDERCARE-AF試験
エドキサバンの非弁膜症性心房細動を有する出血リスクの高い高齢者を対象とした国内第3相臨床試験
The New England Journal of Medicineにオンライン掲載された
本試験は、既存の経口抗凝固剤の承認用法及び用量での投与が困難と判断された出血リスクの高い80歳以上の非弁膜症性心房細動患者984例を対象として、エドキサバン15 mg 1日1回経口投与時の有効性(脳卒中および全身性塞栓症の発症抑制)の検証および安全性(出血性イベント等)を検討するプラセボ対照二重盲検比較試験です。
脳卒中および全身性塞栓症の年間発現率は、エドキサバン群2.3%に対し、プラセボ群6.7%で、エドキサバン群の優越性が示され、所期の目的を達成しました。
安全性評価項目の一つである重大な出血の年間発現率は、エドキサバン群3.3%に対し、プラセボ群1.8%で、エドキサバン群において高い傾向にありましたが、特に臨床的に問題と考えられる致死的な出血や頭蓋内出血は、両群間で差はありませんでした。
本試験は、既存の経口抗凝固剤の承認用法及び用量での投与が困難と判断された出血リスクの高い80歳以上の非弁膜症性心房細動患者984例を対象として、エドキサバン15 mg 1日1回経口投与時の有効性(脳卒中および全身性塞栓症の発症抑制)の検証および安全性(出血性イベント等)を検討するプラセボ対照二重盲検比較試験です。
本試験における主要評価項目である脳卒中および全身性塞栓症の年間発現率は、エドキサバン群2.3%に対し、プラセボ群6.7%で、エドキサバン群の優越性が示され、所期の目的を達成しました。
安全性評価項目の一つである重大な出血の年間発現率は、エドキサバン群3.3%に対し、プラセボ群1.8%で、エドキサバン群において高い傾向にありましたが、特に臨床的に問題と考えられる致死的な出血や頭蓋内出血は、両群間で差はありませんでした。

2020 年改訂版 不整脈薬物治療ガイドライン(日本循環器学会)
大規模臨床試験からわかったこと
①心房細動治療において最も大事なことは、脳塞栓症の合併をいかに減らすかということ
②心房細動治療で抗不整脈薬による洞調律維持は心拍数調節に勝るものではない
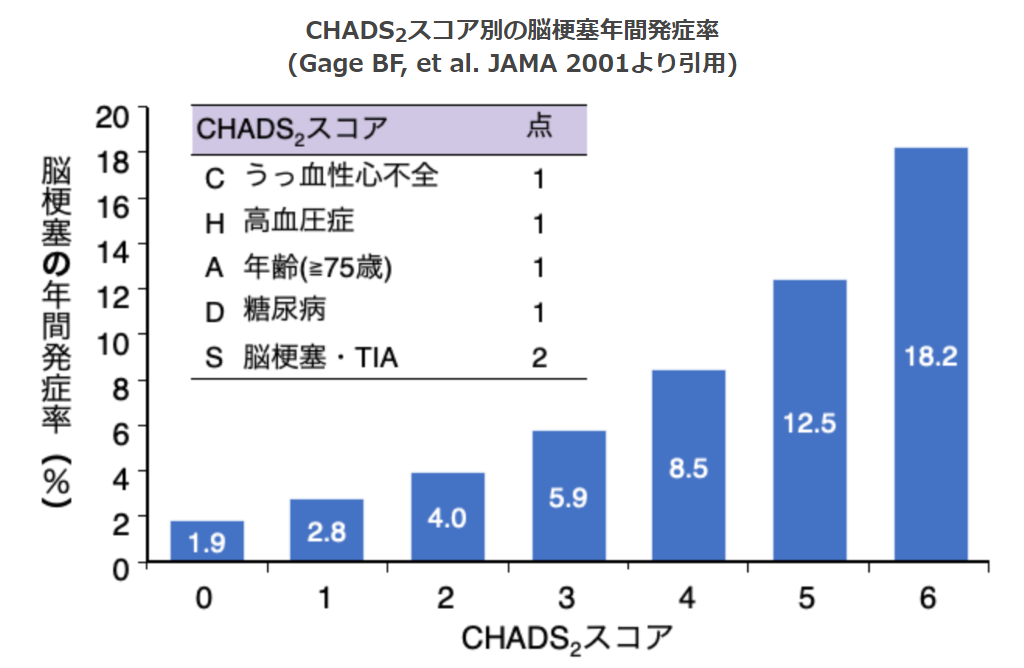
- 脳梗塞リスク評価に応じて(→CHADS2スコア)抗凝固療法を開始する(発作性、持続性問わず)
- 弁膜症性=僧帽弁狭窄もしくは人工弁(機械弁+生体弁)
- 甲状腺機能評価を行う(甲状腺の治療で70%が自然停止)
- 心雑音があれば弁膜症性を疑う
- WPW症候群+Afは除細動の適応(Vfへの進展リスクあり)
- ダビガトラン、リバーロキサバンの消化管出血はワーファリンよりも高頻度
- DOAC処方時はCockcroft-Gault推定式に従う
- 発作性心房細動の人でも、持続性心房細動の人でも、その危険性は同じで、年間の脳梗塞と全身性塞栓症の発症率は約3%
- 非弁膜症性心房細動の患者では、正常洞調律の人と比べて、脳卒中の危険性が5倍高くなり、約1/3の患者が脳卒中を発症します。


- 心房細動の血栓による脳塞栓症は,アテローム性などのその他のタイプの脳梗塞と比較し,中枢側で血栓閉塞するため重症度が高いことが知られており,半数以上が死亡,あるいは重篤な後遺症を残すと報告されている
- 心房細動が原因の脳塞栓症は, 脳梗塞全体の約30%と報告されている
- 日本循環器学会ガイドラインにおいては, CHADS2スコア1点以上は抗凝固療法を推奨

睡眠呼吸障害(Sleep Disordered Breathing, SDB)
SDBとは、睡眠中に一過性の呼吸異常または障害が断続的に出現する病態
近年、高血圧から虚血性心疾患、不整脈、肺高血圧症、心不全まで、様々な循環器疾患に高率にSDBが合併すること、ひいてはその発症と進展に大きく関与する可能性が指摘されている
SASのように日中の過剰な眠気やいびきのような典型的な症状を伴わない場合にも、呼吸不安定とそれに伴う低酸素血症は心・肺・血管に悪影響を与えることが証明され、その適切な診断と管理が、すなわち適切な集学的循環器診療の一部であることから、SDBという診断名を用いるようになった
- 「AHA/ ACCによる睡眠時無呼吸と心血管病変に関するガイドライン」2008年
- 「循環器領域におけるSDBの診断・治療に関するガイドライン」 日本循環器学会、2010年
プライマリケアのための心電図:総論
- 心電図が最も威力を発揮する場面は「不整脈」の診断
- STEMIにおいては発症から再灌流までの時間をいかに短くするかがとても重要で、最初の医療者のコンタクトから再灌流までは120分以内、病院のドアから再灌流までの時間(door to balloon time)は90分以内が推奨
- NSTEMIは冠動脈の不完全閉塞や一過性の閉塞が自然に再灌流した場合、完全閉塞でも良好な側副血行路からの残存血流が存在する場合など、心臓の壁の一部に心筋虚血が生じている状態
- 虚血はNSTEACSがあるため、心電図では診断できないACSが存在する
→ACSの診断は「胸部症状」「バイオマーカーの上昇」「心電図虚血所見」の組み合わせで診断 - 虚血は常に内膜側から生じる→内膜側のみならST低下、貫壁性ならST上昇
- 弁膜症や心筋症など心臓の構造的な異常は心電図ではわかりにくい→心エコーが勝る
- 心筋梗塞→LAD狭窄が最も多い
→急性前壁梗塞ではLADの閉塞部位が近位部か遠位部かを診断することが重症度評価に重要!!! - 電気軸
- 移行帯
- 狭心症
- VT
- 変更伝導
- 脚ブロック
- 房室ブロック
- 急な右室負荷(肺塞栓など)で右軸偏位を起こす
心電図の取り方と誘導

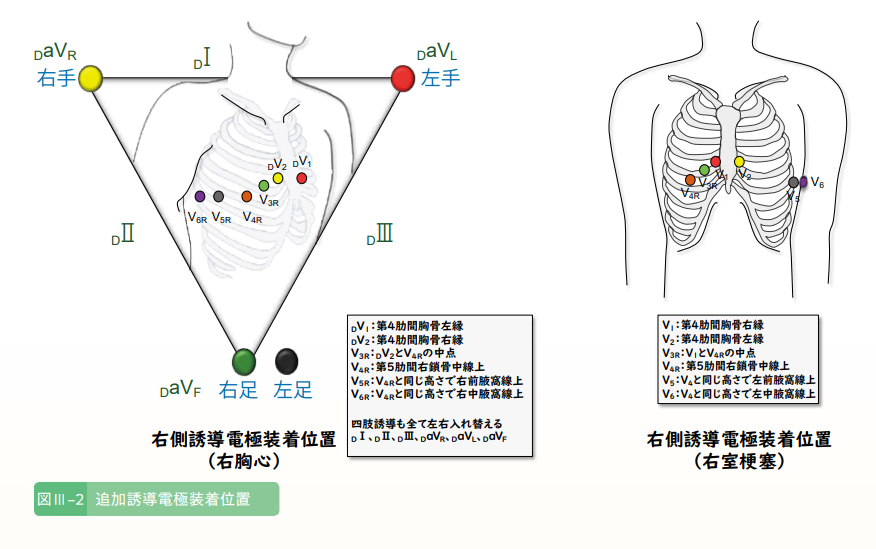
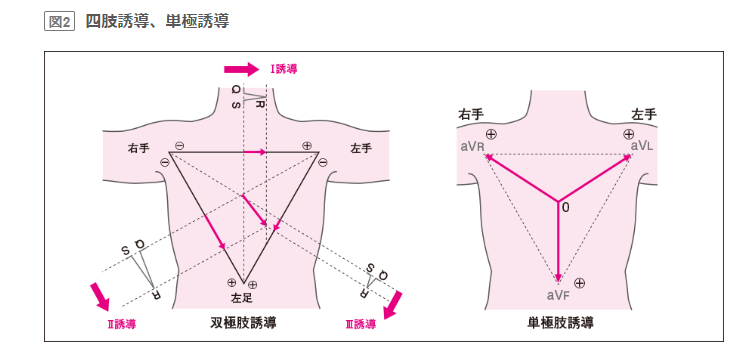
言葉の定義
- PQ時間:電気が洞結節から房室結節まで流れる時間(正常0.12-0.2s)
- R波:
QRS波形は左壁の興奮電動だけ考えればよい(右室の興奮は波形に関与しない)
肥大によりRは増高する。肥大した心筋は虚血を伴い典型的な左室肥大は①R波増高に、②虚血性ST-T変化を伴うようになる - T波:
収縮した心臓がもとに戻るときに(弛緩)できる波
心肥大や強い心筋障害があると、スムーズに弛緩できないためにR波だけでなくT波にも異常が出る
このときにR波が重なるとRonT→致死的不整脈が誘発される - ST上昇:
- ST低下:
右上がりのST低下は頻脈などで生じる正常心電図
水平または右下がりのST低下は虚血性変化 - wideQRS:QRS波の幅が大きく変化するのは、心室の中の電気の流れが悪くなり、時間が長くかかるとき
①脚ブロック②心筋虚血(心室内伝導障害)③WPW症候群の3つを考える。左脚ブロックとも右脚ブロックともいえないような、特徴的な心電図を心室内伝導障害と呼び、心筋梗塞に近い高度の心筋虚血を示している。 - QT時間:
心臓の電気的収縮時間 - QT延長:
QT延長は、再分極(T波)が遅れて心臓の興奮が延長していることを示す
QTが延長すると心室細動という重篤な不整脈が起こりやすく、突然死の原因になる
QT時間の評価は、正確には心拍数で補正されたQTc時間で行う
学童検診ではQTc時間が450msecを超えると異常
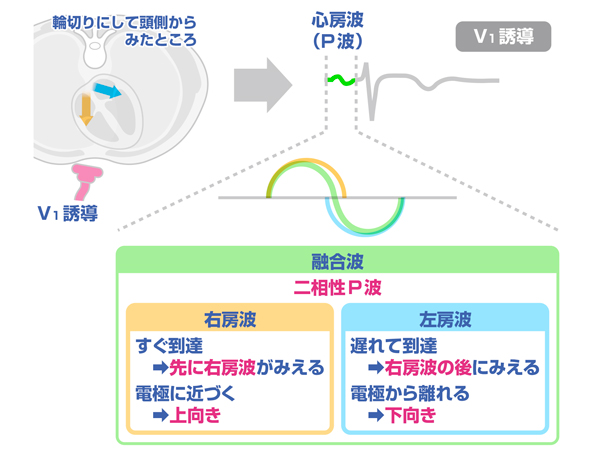
P波の異常
- 正常P波は,心房の興奮過程を示しまず右房が興奮した後に左房が興奮するため、P波の開始点は右房の興奮の始まりを示し,P波の前3分の2が右房の興奮を,後ろ3分の2が左房の興奮を示し,両者が融合したものがP波として示される
- P波の幅の正常値は 0.06 <P≦ 0.10 秒,高さは< 0.25 mV
- 「Ⅱ誘導」→常に上向き、と「V1誘導」→左房負荷では2相性、で評価する
- P波は心房にある心臓のスイッチ
P波がなくてR波が出ていれば、心房内のスイッチが入らなくて房室結節や心室から収縮の刺激が始まったことが分かり、洞結節に異常があることがわかる - P波の形が変化している場合、スイッチは正しく入っていても、心房の中でスイッチの場所が移動していたり、弁膜症などで心房が大きくなっていることが推測される

PQ時間の異常
- PQ時間は電気が洞結節から房室結節まで流れる時間(0.12~0.20s)
- PQ時間が短縮:バイパス経路がある(→WPW症候群)
- 房室結節は本来,1本の通り道であるがなかには通路の途中が分岐し二重伝導路(fast pathwayとslow pathway)となっていることがある(健常者の4人に1認といわれている)

左室肥大
- 典型的な左室肥大では、肥大した心筋は血流不足になるため(心筋虚血)、ST降下やT波陰性化を伴う
- 著明な左室肥大を起こす肥大型心筋症では、ST降下と巨大陰性T波が特徴
- 強い左室肥大では、心筋虚血と同じようにST降下やT波の変化が起こるため、まとめてST-T変化という

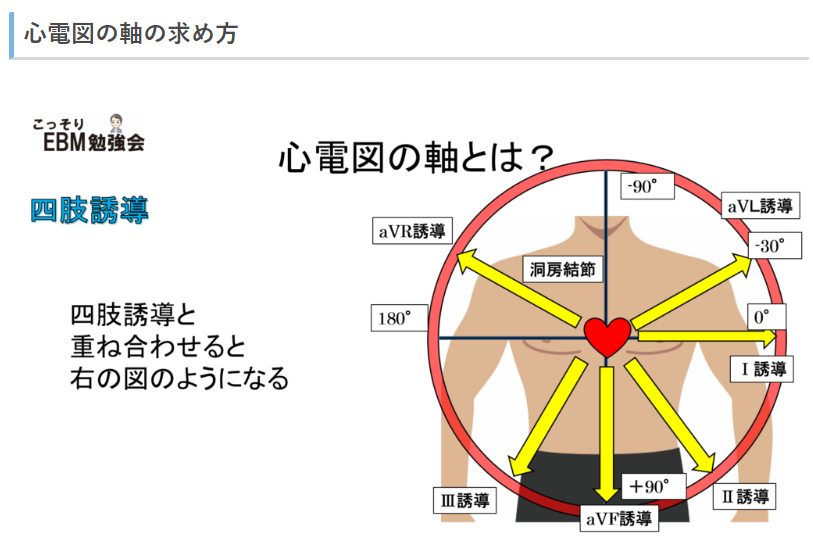
電気軸
早期再分極(early repolarization syndrome;ERS)
早期再分極に見られる心電図所見の特徴
J点の上昇あるいはJ波の存在
- J点とは
→QRS波とST部分の境界点 - J波とは
→QRS終末部に見られるノッチもしくはスラーの総称

「J点上昇」と「J波」は出現誘導や頻度,さらに男女の比率も異なっている
両者は異なる機序で生じている可能性があり,早期再分極所見として同一視するのは問題という考えもある
- 頻度:
- 早期再分極所見あるいは J波は,報告者によりまちまちであるが,一般人口の 5~ 24%
- 好発誘導:
- J波の出現が最も多い誘導は,男女ともに下壁誘導(Ⅱ,Ⅲ,aVF)、次いで左側胸部誘導(V4-6)
- 特発性心室細動症例に関連した J波(J波症候群)
- Brugada型波形を示さない特発性心室細動例の31%にERSを伴うとする報告がある
- 日内変動や日差変動を呈することが知られている
- J波は特に自律神経や心拍数の影響を受け,その振幅は心拍数の上昇により減高し,心拍数の低下によって増高する
心電図各論
心房細動
塞栓リスクと同時に出血リスクも評価する

- HAS-BLEDスコア
出血リスクの層別化には、2010年の欧州心臓病学会ガイドラインに採用されたHAS-BLEDスコアが、日本人でも利用できるがCHADS2スコアとHAS-BLEDスコアの両方に高血圧、高齢、脳卒中の3つの因子が存在し、塞栓症を予防したい患者は出血のリスクも高いというジレンマがある- 同スコア0点を低リスク(年間の重大な出血発症リスクが1%)
- 1~2点を中等度リスク(同2~4%)
- 3点以上を高リスク(同4~6%)と評価する
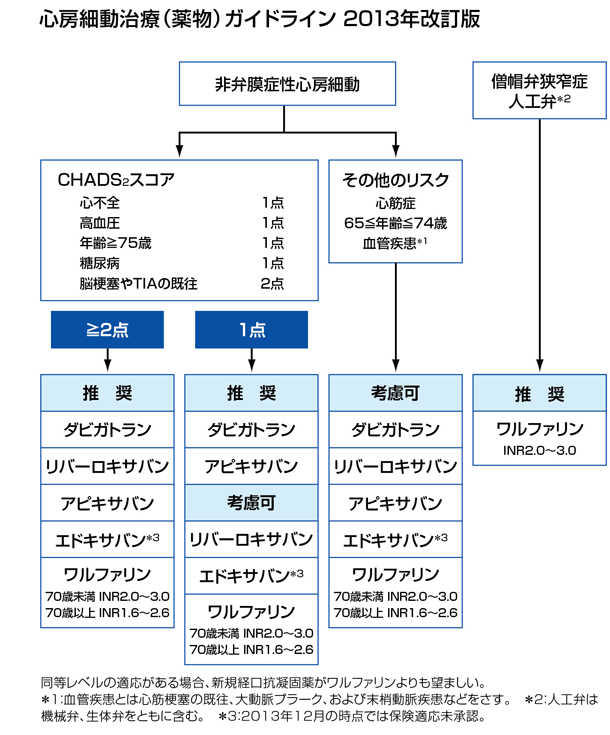
弁膜症性心房細動の定義は、リウマチ性の僧帽弁狭窄症あるいは人工弁置換術を行った心房細動→ワーファリン
それ以外はすべて非弁膜症性心房細動→脳梗塞発症リスクの評価方法CHADS2スコア→DOACが第一選択
大動脈弁疾患、あるいは僧帽弁閉鎖不全であれば、非弁膜症性の定義に当てはまる
- CHADS2スコア
簡便であるが非弁膜症性心房細動の大半はCHADS2スコア1点以下の患者さんであり、リスクとしては低いものの絶対数が多いため脳梗塞をきたす患者数としてはかなりの割合を占めている。
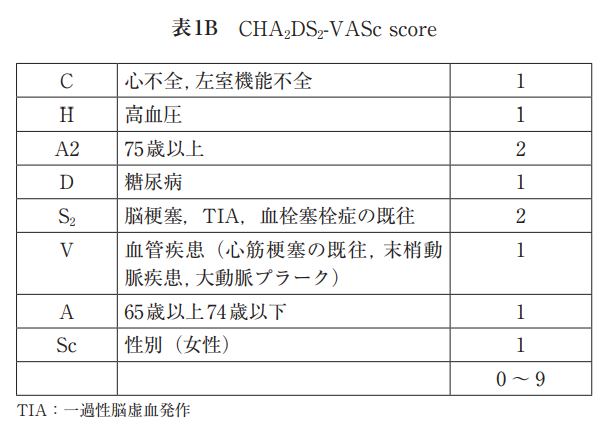
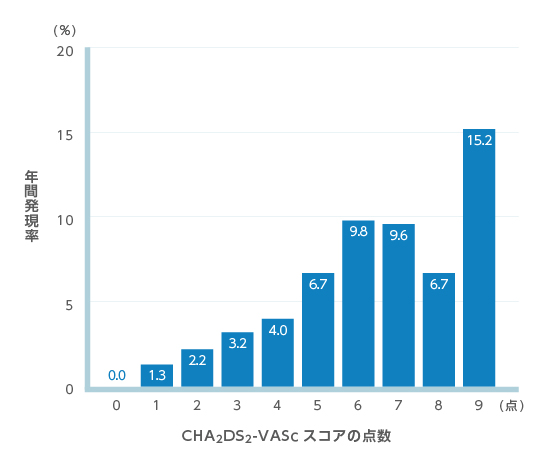
CHADS2スコアで用いられる危険因子以外にも、心筋症、年齢(65-74歳)、心筋梗塞の既往、大動脈プラーク、血管疾患、性別(女性)等が報告されていることから、CHADS2スコアだけでは脳梗塞のリスクを評価できない年齢(65-74歳)、心筋梗塞の既往などの血管疾患合併例、女性(器質的心疾患を有さない65歳未満の女性は計算されない)をそれぞれ1点とし、75歳以上の年齢ではリスクがさらに高まることを考慮して2点として計算されるCHA2DS2-VAScスコアが提唱されたが、わが国の2020年改訂版「不整脈薬物治療ガイドライン」では依然としてCHADS2スコアが用いられている。 - CHADS2スコアが1点以上の場合、脳梗塞を発症するリスクが高い
- 低リスク:0点(年間脳梗塞発症率1.9%)
- 中等度リスク:1点(同2.8%)
- 高リスク:2点以上(同4.0%以上)
- 「不整脈薬物治療ガイドライン」では、出血リスクをHAS-BLEDスコアで評価することがクラスIで推奨された

洞不全症候群
- 洞結節細胞群は自動的に電気的興奮を発生することのできる能力(自動能)を有しており、洞結節および洞結節周辺部組織の機能的もしくは器質的障害により、洞自動能や房室伝導能の低下が生じて、原因不明の持続性洞性徐脈、洞停止又は洞房ブロック、徐脈頻脈症候群の3つのタイプの徐脈性不整脈を呈す
- 通常の心拍数は1分間に60回~100回程度ですが、洞不全症候群では運動時や発熱時などの心拍数が上昇する状態においても十分な心拍数の上昇が認められない
- 洞性徐脈:
心房興奮を反映するP波が規則正しい間隔で現れる数が少ないもの - 洞停止(洞房ブロック):
P波が突然現れなくなる場合 - 徐脈頻脈症候群:
心房細動や心房粗動、発作性上室性頻拍などの様々な頻脈性上室性不整脈を合併し、その頻脈が停止した後に洞停止を生じる。徐脈頻脈症候群は洞性徐脈性不整脈単独例に比べ、頻脈停止後に高度の心停止をきたして失神の原因となることが多く、重症な洞不全症候群として位置づけられる。
ペースメーカーの適応
失神、痙攣、眼前暗黒感、めまい、息切れ、易疲労感などの症状あるいは心不全がある徐脈性不整脈(洞不全症候群、Ⅱ度~Ⅲ度の房室ブロック、徐脈性心房細動)が、ペースメーカーの適応となります。Ⅱ度~Ⅲ度の房室ブロックでは、無症状でも適応になることがある
- 最近ではMRI対応ペースメーカーもある
- 無症候性の徐脈性心房細動の場合、一応5秒以上(大きなマスで25マス、3秒=15マスという意見もあるが、対象症例が多すぎるという意見も)というのが一つの目安
- 徐脈性の疾患の場合、ペースメーカーを入れてそのような症状が完全になくなれば、専門医の許可のもと運転ができるようになる
徐脈性不整脈に対する薬物療法
- シロスタゾール、イソプレナリン、テオフィリンは有害事象として頻脈があり、徐脈に使用できる
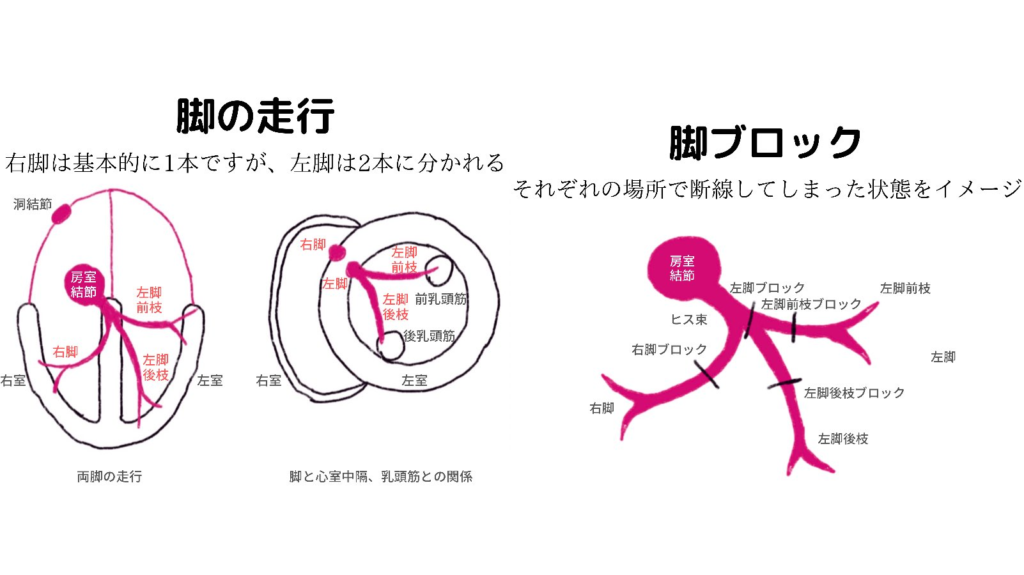
右脚ブロック
- 右脚ブロックだけでは右軸偏位とはならない(軸はあくまで左室壁の電気の流れを反映する!)
- 実臨床ではCRBBB+心肥大でST変化を伴うwideQRSに見えることがあるが、心エコーを行えば心肥大もasynergyも一発で評価ができ、その場でACSを否定できる。
左脚ブロック
- 左脚後枝は太く、通常単独では障害されない
- 左脚前枝ブロック→高度左軸偏位(図で青)
- 左脚後枝ブロック→高度右軸変異(図で紫)
- V6にseptalqがない
- 左脚ブロックでは、電気は左軸偏位になる
- https://www.youtube.com/watch?v=RDJgDZWzdmw

2枝・3枝ブロック
- 束枝ブロックは他の伝導障害と併存することがあり,RBBBは左脚前枝または後枝ブロックと併存することがあり(2枝ブロック),左脚前枝または後枝ブロックはRBBBおよび第1度房室ブロックと併存することがある(不正確に3枝ブロックと呼ばれているが,第1度ブロックは通常,房室結節起源である)。
- 3枝ブロックとは,右脚ブロックと左脚前枝および左脚後枝の交代性ブロックの併存,または左脚および右脚の交代性ブロックを指す。心筋梗塞後の2枝または3枝ブロックの存在は,広範囲の心筋損傷を示唆する。2枝ブロックは,間欠性の第2度または第3度房室ブロックが存在しない限り,直接の治療を必要としない。真の3枝ブロックには,緊急のペーシングとその後の恒久的ペーシングが必要である。
- QRS幅が延長するが(120msecを超える),QRSパターンがLBBBまたはRBBBに典型的なものでない場合は,非特異的心室内伝導障害と診断する。プルキンエ線維より末梢側で伝導遅延が生じる可能性もあり,これは心筋細胞間の遅い伝導に起因する
WPW症候群
- 通常は心房心室間は房室結節以外は電気的に絶縁されているが発生の段階でアポトーシスがうまく進行せずに
伝導路が複数形成されてしまう状態 - 非発作時の心電図では容易に診断可能(デルタ波と)
- 潜在性WPW症候群
頻脈性不整脈
頻脈性不整脈を見たら,stableかunstableか即座に判断を判断
→unstableなら即座に電気的除細動(自己脈があるため全例カルディオバージョンを選択)
→stableなら原因精査(電解質異常やACS合併など)と心電図の診断
頻脈性不整脈の分類は2×2表に大分類
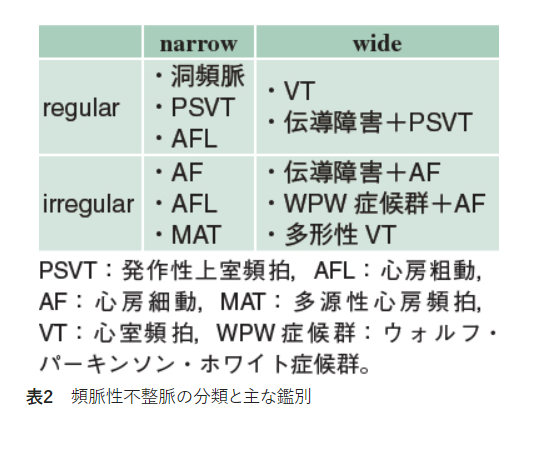

SVT/PSVT
まずはmodified Valsalva法とreverse Valsalva法を試す
→無効の場合は薬物的除細動
→無効の場合は電気的除細動(カルディオバージョン)
- AT、AVNRT、AVRT(ORT:orthodromic re-entry tachycardia)の3種類を鑑別する
- ATP製剤使用する前に心エコーで低心機能を除外しておく→心停止する
- PSVTであれば致命的になることはほとんどないため,停止後は多くは安全に帰宅可能
- 帰宅させる前に,特に急性冠症候群(ACS)でないかどうか,洞調律復帰後の心電図波形の評価は忘れない!!!
- 帰宅時には発作時の心電図を本人に渡す→別の医療機関受診時の診療の指標となり得る
- AVNRT
- 自然停止する
- 治療法:
- modified Valsalva法:
- 従来のValsalva法である息こらえはあまり効果がなく,洞調律復帰率は5~20%程度
- modified Valsalva法は50%程度の洞調律復帰率が期待できる
- modified Valsalva法:

- reverse Valsalva法:
- 50%程度の洞調律復帰率

- 薬物的除細動:
- ATPの急速静注:第一選択
- ATPは気管支攣縮作用があるので,気管支喘息は禁忌
- マイナーな副作用:顔面紅潮や呼吸困難,頭痛,嘔気嘔吐,不安や恐怖心の出現など
- 投与方法:
- ATPは5~10 mgを急速静注し,効果がなければ最大20 mgまで使用可能
- 急速投与が重要→点滴刺入部はなるべく中枢寄りに、三方活栓を操作してATPを生食で急速に後押しする(フラッシュ用生食20mLをあらかじめ接続しておく)
- Ca拮抗薬:第二選択
- ATPでも止まらない頑固なPSVTには,Ca拮抗薬を使用
- 房室伝導を抑制する目的で,ベラパミルやジルチアゼムを投与する
- PSVT停止率はATPとおおむね同等
- 実際の投与方法:
- ワソラン(ベラパミル)1A=5㎎/5mL
- ベラパミル1A(=5mg)を5分かけて点滴
- ◎ヘルベッサー(ジルチアゼム)1管=10㎎
- 1管(=10 mg)を3分かけて投与する
- 陰性変力作用の弱いジルチアゼムを選択する方がよりベター
- ベラパミルは1 mg/分,ジルチアゼムは2.5 mg/分の速度で投与することで,効果はそのままで低血圧発生率を1%未満に抑えられる
- ワソラン(ベラパミル)1A=5㎎/5mL
- ATPの急速静注:第一選択
- カルディオバージョン/電気的除細動を行うと,リエントリーに起因する頻拍性不整脈を極めて効果的に停止させることができる
- RonTは催VF作用があり危険なため、心電図同期でR波の直後に放電するようになっている
- エネルギー量:
- 除細動:2相性150Jで固定されている
- カルディオバージョン:疾患ごとに推奨されるエネルギー量が異なる
- カルディオバージョンの合併症:
- 通常軽微であり,具体的には心房および心室性期外収縮や筋肉痛などがある
- 頻度はより低いが,左室機能が正常下限の場合や複数回のショックが用いられた場合には,カルディオバージョンは心筋細胞障害や電気収縮解離の発生頻度を高める可能性がより高くなる
- 実際のやり方
- 鎮静に伴う誤嚥予防の観点から絶食時に行うことが望ましい
- パッドを貼り除細動器で心電図をモニタリングする
- 同期ONにすると除細動器のモニタ上のR波に認識したサインが表示され始める
- エネルギー量を設定する→疾患ごとに異なる
- 同期短時間の全身麻酔か鎮痛薬および鎮静薬の静注
- ラボナール2〜4mL(2.5%溶液で50〜100mg):喘息には禁忌
- フェンタニル1μg/kgに続いてミダゾラム1~2mg,2分毎,最大5mg

- 300㎎(溶解液12mL)と500㎎製剤(溶解液20mL)があるが、300㎎で十分
- 添付溶解液で2.5%水溶液(25 mg/mL)に調整して使用する→調整後の濃度は300でも500でも同じ
- 投与量:
- 最初に2~3 mL(2.5%水溶液で50~75 mg)を10~15秒位の速度で注入後30秒間麻酔の程度,患者の全身状態を観察する.
- さらに必要ならば2~3 mLを同速度で注入して適度な鎮静を得る
- 2~3mLの追加投与でで10~15分の鎮静追加を得る
- 最初に2~4 mL(2.5%溶液で50~100 mg)を注入(Slow静注で可)して患者の全身状態,抑制状態などを観察し,その感受性から追加量を決定
- カルディオバージョンの麻酔として使用する場合は50㎎程度~投与開始して適宜追加する(内視鏡のミダゾラム鎮静と同様)
- ラボナール(チオペンタール):
- カルディオバージョンの場合は5㎎とごく少量
(麻酔前投薬として使用する場合は50㎎程度、精神科領域(電気痙攣療法)では300㎎も使用)
- カルディオバージョンの場合は5㎎とごく少量
心房粗動・心房頻拍
内膜下虚血、完璧性虚血
見逃してはいけない心電図
LMT主幹部閉塞
- LMT主幹部閉塞
- aVRでのST上昇(+下壁誘導ST低下=reciprocal change)
- LV基部完璧性梗塞
- LV全体の内膜下虚血によるST低下のミラーイメージ(=reciprocal change)
前胸部誘導のST偏位によりLAD閉塞部位を判別することは難しいとされている。近位部閉塞例では,左室心基部寄りに貫壁性虚血を生じるため傷害電流ベクトルは右上方へと向かい,このため左室心基部に面するaVR誘導のSTは上昇し,これに対する対側性変化として下壁誘導のSTは低下する。一方,遠位部閉塞例では,傷害電流ベクトルは前方に向かうため下壁誘導に対側性変化によるST低下は生じない。急性前壁梗塞では肢誘導のST偏位が重要である。
- aVRでのST上昇(+下壁誘導ST低下=reciprocal change)
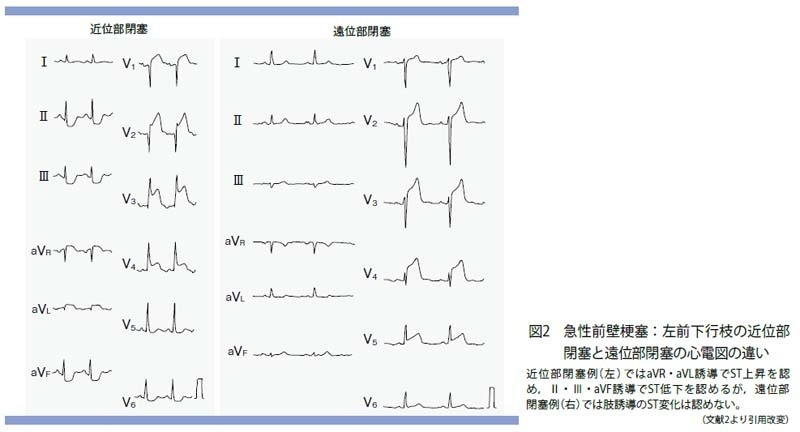
- 心筋梗塞でショックになるのはLMT病変、LAD近位部病変→ただちに3次医療機関への搬送が必要
LM閉塞例では灌流域が非常に大きいにもかかわらず前胸部誘導のST上昇はむしろ軽度な例やST低下を認める例もあり注意を要する。これは左室前壁(LAD領域)と左室後壁(左回旋枝領域)のST上昇が同時に存在し互いに相殺し合うためで,左室後壁のST上昇が高度である場合にはむしろ前胸部誘導のSTは低下し,より重症例である。また,広範で高度な心筋虚血に起因する心室内伝導障害を反映しQRS幅が増大するのが特徴である(ネット記事より)。

側壁梗塞
- 側壁梗塞では、Ⅰ、aVLおよび側胸部誘導でST上昇
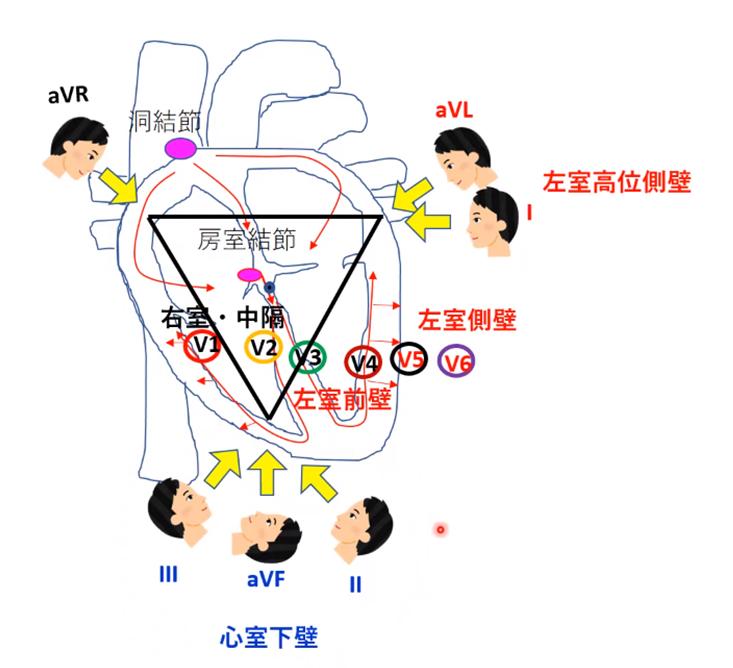
- V1は右室、V2は中隔、V3-4が左室前壁、V5-6が左室側壁を投影する
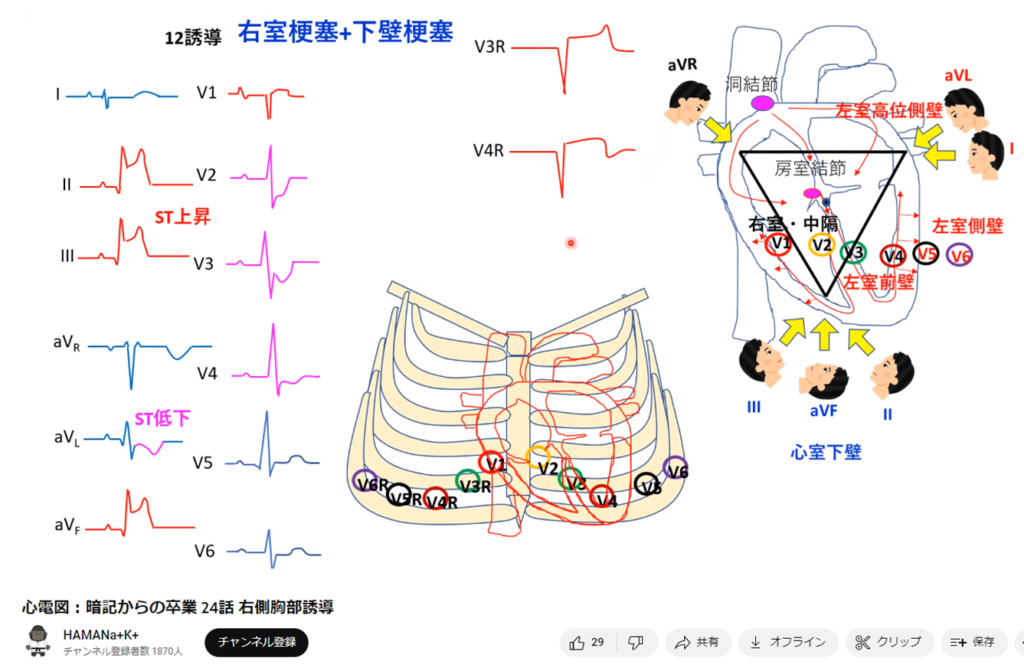
右室梗塞
- 右室梗塞は単独では起こりづらく通常、下壁梗塞を伴う
- 右室梗塞(+下壁梗塞)ではⅡ、Ⅲ、aVf(+V1も)に変化が出やすい
- 下壁梗塞を見た場合、右室梗塞の合併にも注意が必要→下壁梗塞では右側胸部誘導を追加する
- 嘔気、嘔吐、下痢といった腹部症状はAMIとくに下壁梗塞でしばしば見られ、右冠動脈領域の疾患においてBezold-Jarisch反射として知られている副交感神経緊張に由来する。
下壁梗塞
- 下壁梗塞は責任病変が右冠動脈、回旋枝いずれの場合もある
- 下壁梗塞では、右室虚血を合併した場合、対側性変化としての前胸部誘導のST降下は減弱する。これは、右室虚血が右側胸部誘導だけでなく、V1誘導を中心とした前胸部誘導のST部分を上昇させる方向に働くため。
- 下壁梗塞による対側性変化はaVLに最もよく反映される。左回旋枝による下壁梗塞の場合は、aVL誘導のST降下が側壁の虚血によるST上昇に相殺されますが、その場合は前胸部誘導に対側性変化が現れるため、診断は難しくない。
後壁梗塞
- 背部誘導(V7・V8・V9)を追加する
ブルガダ症候群
- 右室流出路付近に原因がある
- 若い男性に多い
- 第3肋間でV1B、V2Bを追加するとより鮮明化する

Wide QRS tachycardia
Wide QRS tachycardiaでは「否定されるまで心室頻拍VTを疑え」が原則
- もともと脚ブロックやWPWを有する患者が、洞性頻脈や発作性上室性頻拍症、頻脈性心房粗・細動を生じた場合(220/minを超える頻拍では1:1伝導の心房粗動の存在を疑います)
- 変行伝導を伴う上室性頻拍の場合
- https://miyake-naika.com/01sindan/wide-qrs.html#gsc.tab=0
正常時に伝導障害はなくても、上室性頻拍の際に機能的不応期による右脚ブロックを合併する場合があります。
心拍数がある一定数より速くなると一過性に右脚ブロック、右軸偏位(下方軸)を来しやすくなりますが、これは右脚の不応期が左脚より長いために起こる機能的ブロックで病的意義はありません。
VT
- 定義:連続で3拍以上にわたり心拍数が120/分以上となる状態
- QRS幅の広い頻拍(QRS ≥ 0.12秒)は,VTでないことが証明されるまでは,全てVTとみなすべき
- 房室解離があればVT
- ほとんどのVT患者は有意な心疾患(特に 心筋梗塞の既往または 心筋症)を有する
- 心室頻拍は単形性と多形性に,また非持続性と持続性に分類される
- 単形性VT:単一の異常興奮起源またはリエントリー伝導路に起因し,同じ形態のQRS波が規則的に生じる
- 多形性VT:いくつかの興奮起源または伝導路に起因し,そのためQRS波は不規則で,形態が変化する
- 非持続性VT(NSVT):持続時間30秒未満
- 持続性VT(sustained VT):30秒以上継続するか,血行動態の破綻により30秒未満で停止する
- 予後:
- 基礎心疾患のみられない正常心機能症例 の非持続性心室頻拍は生命予後に関与しない→治療対象外
- 基礎心疾患があり(日本では30%が心筋梗塞、70%が心筋梗塞以外の心疾患)心機能が中等度以上(EF40%~35%以下)に低下している症例の非持続性心室頻拍は予後不良
肥大型心筋症(指定難病58)
- 肥大型心筋症の診療に関するガイドライン(日本循環器学会)
- 高血圧や弁膜症などの心肥大を起こす明らかなほかの原因がないのに、左室に異常な肥大を起こす疾患
- 心筋の不均一な肥大と拡張不全を特徴とする心筋症で、左室内圧格差の有無(HOCM→HCMの25%程度、それ以外か)が重要だが、左室内圧較差は固定された値ではなく病状の変化によりその値を大きく変化させることが特徴
- 肥大型心筋症患者の20%以上に心筋虚血を合併している
- 頻度:心エコースクリーニングでは、一般人口の1/500〜1/1000人において認められる
- 家族歴:HCM患者の約半数は常染色体優性遺伝形式に従う明らかな家族歴を認める、突然死の家族歴も聴取する
- 症状:不整脈や心原性塞栓、突然死の原因となる。自覚症状がほとんどない症例も多く存在するが胸痛,胸部絞扼感という狭心症との鑑別が必要な症例,また,めまいや失神などの脳症状を強く訴える症例も多い
- 心音:巨大IV音(心尖部で触知可能)を聴取し,また多くの患者でIII音を聴取
- 心電図:①R波の高電位と陰性T波の存在は典型的な左室肥大所見の反映、その他の所見として②QT 時間の延長、②胸部誘導でR/T比の減少(T波増高)、③II,III,aVF における q ~ Q 波など
- 心エコー:HCMに必須の検査
- 心室中隔厚/左 室 後 壁 厚 比 > 1.3とASH (asymmetric septal hypertrophy)
- 予後:心不全発症後の予後はHCM(38か月)<<<DCM(225か月)でHCMで圧倒的に予後不良
- 治療:
- βB:左室拡張障害の改善効果は乏しいこと,また心肥大退縮効果がなく,心筋障害進展の抑制効果(いわゆる拡張相への移行の抑制)は極めて乏しいことから長期の生命予後の改善効果は乏しい
- Ca拮抗薬:ベラパミル、ジルチアゼムが用いられる。細胞内Ca2+濃度の上昇がHCM患者の左室拡張障害に強く関与していること,また細胞内Ca2+濃度の上昇そのものが心肥大の程度とも密接に関連している。
虚血性心疾患・冠動脈疾患
INOCA:
狭心症状を有し非侵襲的検査で心筋虚血所見が認められるにもかかわらず、冠動脈造影検査で心外膜冠動脈に狭窄病変を認めない疾患。INOCAには主に冠攣縮と微小血管障害の2つの病態が関与している。
MINOCA:
心筋虚血に伴う心筋逸脱酵素上昇などから心筋梗塞と診断されるにもかかわらず、冠動脈に閉塞性病変が認められない疾患。女性に多くNSTEMI(non-ST elevation myocardial infarction)の発症形式をとる特徴がある。MINOCAの原因は多岐にわたり(プラーク破綻・冠攣縮・冠動脈解離など)、個々の症例における最適な治療戦略を構築するためにその原因を明らかにすることが必要である。
冠攣縮性狭心症
治療の基本は「危険因子の是正」と「薬物治療」である。
冠攣縮の発作時には,ニトログリセリンの舌下錠もしくはスプレーの口腔内噴霧が有効である。
- 危険因子:
- 喫煙は明らかな危険因子であり,禁煙は必須である
- 飲酒については,大量飲酒後数時間経過してから発作が起こることが多いため,節酒する必要がある
- 有酸素運動が,血管内皮機能,酸化ストレスや炎症の改善作用を介して発作を抑制することが報告されている。しかし,早朝の運動は冠攣縮誘発の恐れがあるため,午後に行うなどの指導が必要である。
- 薬物治療:
- Ca拮抗薬:薬物治療の第一選択薬
血管平滑筋細胞へのCa2+の流入を抑制することで冠攣縮を抑制する。
夜間~早朝にかけて冠攣縮発作を認める場合が多いため,夕食後あるいは就寝前投与が推奨されるが,症例により生活リズムが異なるため,発作時間帯に合わせた処方設計を心がける。
治療に用いられるCa拮抗薬にはベンゾジアゼピン系やジヒドロピリジン系があり,単剤で著効しない場合には複数を組み合わせて用いる。 - ニコランジル:
選択的な冠動脈拡張作用と抗冠攣縮作用を持つ薬剤で,Ca拮抗薬と異なる薬理作用であるため,Ca拮抗薬抵抗性の症例に併用する。 - スタチン:
脂質改善効果のほか,内皮機能改善作用,抗炎症作用,Rhoキナーゼ抑制作用を有し,冠攣縮を抑制する効果が示されている。
- Ca拮抗薬:薬物治療の第一選択薬
【治療上の一般的注意&禁忌】
β遮断薬は心筋の酸素需要を低下させるため,器質的狭窄合併例にはよい適応となるが,β遮断薬の単独投与は,相対的なα受容体刺激により血管収縮を促し冠攣縮を惹起する可能性があるため,長時間作用型Ca拮抗薬を併用する。
また,硝酸薬の血中濃度が一定であると耐性が生じやすいので,耐性を避けるためには休薬時間を置くことが重要である。発作の出現状況を詳細に聴取し,冠攣縮の活動性が最も高い時間帯に硝酸薬の十分な血中濃度が維持できるように,投与時刻や投与量を決定する。