5類以降後の対応とエビデンスまとめ
「5類」に移行したあとは、発症の翌日から5日間は外出を控えるほか、症状が軽くなってから24時間程度は外出を控えることが推奨されるとしています

- 最新の手引きは2023年8月更新 新型コロナウイルス感染症(COVID-19)診療の手引き 第10.0版
- 2023年5月4日にWHOは,国際的に懸念される緊急事態 PHEICの終了を宣言した
- オミクロン株の症状:
- 咽頭痛で発症することがしばしば、嗅覚味覚障害の頻度は減少した
- 重症化すると下気道にまで炎症が広がる(中等症~重症)が、症例数は激減している
- 血栓塞栓症(肺塞栓や脳卒中など)はオミクロン株で頻度が減ったとされているが心血管系の合併症には引き続き注意が必要(不整脈、ショック、心筋炎など)
- 再感染は最後の感染から3か月間は起きにくいとされる
- 15歳未満の小児における無症候性感染の割合はオミクロン株で10%程度(従来は30~40%)まで減少したが、けいれん(7~13%)や悪心嘔吐(12~22%)の頻度はむしろ増加しているが、小児は軽症例(95%以上)が多い
- 現在の感染管理:
- 発症日は0日目、発症翌日からカウントして丸5日間(=120時間)が経過した6日目から通常生活可能
- 症状の改善が5日目以降だった場合は、症状改善後24時間以上経過してから
- ワクチン接種の推奨について
- 現在のワクチンはオミクロン対応2価mRNAワクチン(インフル4価、肺炎球菌23価、HPV9価)
- オミクロン株の変異に合わせてワクチンも製造承認を繰り返している(BA.1→BA.4-5対応ワクチンへ移行)
- 日本小児科学会では、生後6か月から17歳のすべての小児にワクチン接種(初回接種および追加接種)を推奨
- 日本産婦人科学会では、すべての妊婦に週数を問わずワクチン接種を推奨
- RCTの効果から治療効果が証明されず、使用されなくなった薬が多々ある
- ファビピラビル(アビガン)
- イベルメクチン:捏造論文まで出る始末
- 治療:
- エビデンスはオミクロン株流行前、流行後いずれのデータもある
- 一律に投与するのではなく、適応をしぼって使用する→診療の手引き(厚労省作成)に準じて治療適応を評価
- 中等症以上は入院を推奨→薬物療法+酸素療法
- 中等症II以上に対する抗ウイルス薬はレムデシビル(ベクルリー)1択
- パキロビット、ベクルリーは腎機能による用量調節が必要
- 中等症II:SpO2が93%以下(=呼吸不全あり、酸素投与開始)
- 酸素投与が必要となるため総合病院へ入院
- レムデシビル+酸素療法に加えて、ステロイド療法を考慮する
- 細菌性肺炎の合併を考慮し抗生剤治療を併用する
- 中等症I:SpO2が94~95%→厳密には非常に少ないか
- SpO2モニタリングを要するため(1日2回以上)入院を考慮する
- フローチャートに沿って薬物療法を行う(パキロビットパック→ベクルリー→ラゲブリオ)
- 軽症例:SpO2が96%以上
- 対症療法を行う(NSAIDS使用を禁止するほどの強いエビデンスはない)
- ゾコーバ:重症化リスクのない軽症例で、特に臨床症状が強く日常生活に支障をきたしている者(高熱や全身の筋肉痛、咽頭痛、食思不振など)に限定処方
- レムデシビル(ベクルリー):ギリアド・サイエンシズ株式会社 1瓶100㎎=61,997 円 ダントツ高額治療
- エビデンス:
- 重症化リスクを有する発症7日以内の自宅療養者(軽症/中等症I)に対するベクルリー3日間投与は、プラセボ群に比し入院/死亡を87%減少させた
- 重症化症例に対しては効果が期待できないが、そこまでに至らない症例には症状の早期改善が期待できる
- 投与期間は原則5日間(5日と10日で有効性と有害事象に差なし)
- 用法用量:
- 成人及び体重40kg以上の小児にはレムデシビルとして、投与初日に200mgを、投与2日目以降は100mgを1日1回点滴静注
- SARS-CoV-2による感染症の症状が発現してから速やかに投与を開始し、3日目まで投与する。
- SARS-CoV-2による肺炎を有する患者では、目安として、5日目まで投与し、症状の改善が認められない場合には10日目まで投与する。
- 慎重投与:
- 腎不全(eGFR<30では推奨できない)だが、透析患者にも使用経験あり
- エビデンス:
- ニルマトレルビル/リトナビル(パキロビットパック):ファイザー、1回19,805.5円で最安値!!!
- エビデンス:
- 重症化リスクを有する非重症患者に対する投与で入院/死亡リスクが89%減少
- 中等症II以上の治療や重症化予防にはエビデンスがなく使用できない
- エビデンス:
- モルヌピラビル(ラゲブリオ):MSD、200㎎錠2357.8円 1回で約5万円
- エビデンス:弱い
- 重症化リスクを有する非重症患者に対する投与で重症化を30%減少(プラセボ群9.7%vsラゲブリオ群6.8%)
- 中等症II以上の治療や重症化予防にはエビデンスがなく使用できない
- 用法用量:
- 発症5日以内に投与を開始すること
- 18歳以上には1 回 800mg を1日2回、5日間経口投与(200㎎錠2357.8円、1日薬価9428円、1回5万円)
- 禁忌:
- 妊産婦
- エビデンス:弱い
- エンシトレルビル(ゾコーバ):塩野義製薬、7407.4円/錠→費用対効果が悪い!!! 1回で約5万円
- エビデンス
- 国内製造薬のため海外使用歴もなく、国内緊急承認されたため、エビデンスに乏しい→今後消える?
- 臨床試験では、臨床症状を1日程度短縮させた
- 重症化予防効果は証明されていない
- 用法用量:
- 12歳以上の小児及び成人にはエンシトレルビルとして1日目は375mgを、2日目から5日目は125mgを1日1回経口投与
- エビデンス











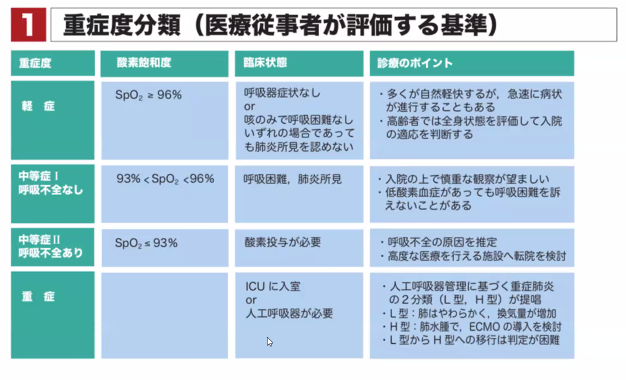
- かつては感染、発症から重症化までタイムラグがあった
- 感染早期(軽症期)に抗ウイルス薬や抗体薬を使用すべき
- 重症化した場合は抗炎症薬(ステロイド薬)を使用することが優先
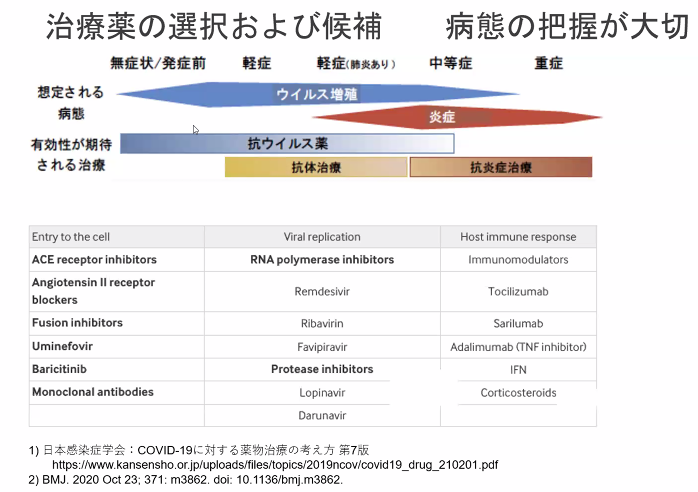



→プライマリケアでは治療薬は4択
- 抗体薬は変異のたびに効果がなくなる→現在の株には効果がなく、現状で推奨されている抗体薬はない

- もっとも有効性が高いのはパキロビットだった



- ゾコーバは不要な薬、自然に治るグループなので処方不要 重症化防ぐデータが示されなかった

- やはり重要なのはワクチン接種→ワクチンなければもっと大勢が死んでいた
- 現在の死亡例はウイルスではなく、細菌感染の合併で死亡することが多い(とくにワクチン接種例)→抗生剤の併用が重要

- 米国のガイドラインには使用の推奨順が示されている→日本でもようやく明記された

診療ガイドライン
- COVID-19診療の手引き(厚労省)→2022年10月でVer8.0まで更新されている
- COVID-19に対する薬物治療の考え方(日本感染症学会)
後遺症
嗅覚障害・味覚障害
- ネットでは当帰芍薬散がいいのでは?とうわさされている
- 和漢の先生的には、証に合ったくすりがよいのでは?とのこと
- 当帰芍薬散→冷え性のタイプならこれで良い
- 暑がりタイプなら同系統の桂枝茯苓丸
- 感冒後の様々な症状によく出すのは柴胡桂枝湯
- 漢方はすべての症状がいっぺんに解決することはなくとも、徐々によくなっているならそのまま継続するとよい
臨床(オミクロン株)
- 現行の流行株
- 2022年9月現在、世界で検出されるウイルスのほぼすべてがオミクロン株(主にBA.5)と考えられている
- 過去のSARS/MERSとの違いは、発症前から感染性があること(大流行の最大要因)
- 2022年9月までの世界の感染者6億人、死者650万人、超過死亡約1500万人
- 潜伏期・臨床経過
- 潜伏期2~3日、大部分が7日以内(中央値2.9日)、99%が暴露後10日以内に発症する
- 無症候性感染者の割合は20~40%
- 感染可能期間は発症2日前から発症後7~10日程度、血液、尿、便からの感染はまれと考えてよい
- 症状
- オミクロン株では、鼻汁・鼻閉、咽頭痛などの感冒症状が強まった(味覚・嗅覚障害の頻度は減少した)
- 急性喉頭炎や喉頭蓋炎、小児ではクループ症候群に至る可能性もある
- 多くの患者では、上気道炎にとどまるが下気道にまで広がると重症化する
- 症状からインフルエンザとの鑑別は困難
- 重症化・死亡率
- オミクロン株に移行し、死亡例は大多数が80歳以上の高齢者となった
- デルタ株と比較し、重症化率が減少し、致死率は 67%低下した(英国のデータ)
- 病態
- 肺炎はII型肺胞上皮細胞へのウイルス感染が本態で、重症例ではARDSに準じた病態(びまん性肺胞傷害)となる
- 基礎疾患・重症化リスク因子:下記表参照、もっとも重要な重症化因子は高齢


- 重症化予測因子:すでにいくつかのスコアリングがあるが、ワクチン普及前のデータだったりデルタ株やアルファ株、オミクロン株での普遍性についての議論の余地がある

- 呼吸器以外の合併症
- 呼吸器以外の病変部でもSARS-COV-2が検出されるかどうかはコンセンサスが得られていない
- 心血管系
- 急性期の不整脈、急性心障害、ショック、心停止のほか、症状回復後の心筋炎など
- 発症から1か月以上経過しても脳血管障害、不整脈、虚血性心疾患、心膜炎、心筋炎、心不全などのリスクがある
- 2回目のワクチン接種後にも心筋炎・心膜炎を疑う報告をまれに認めるが有益性がリスクを上回ると判断されている
- 血栓塞栓症
- 肺塞栓症、急性脳卒中などの血栓塞栓症が報告されている
- COVID-19中等症以上では、予防的な抗凝固療法が広く施行されるようになり、国内入院患者における血栓塞栓症発症者は約1.9%(脳梗塞や肺塞栓/DVTが最多)と報告されている
- 炎症性合併症
- 重症例においてはサイトカイン放出症候群、ギランバレー症候群、川崎病類似の小児多系統炎症性症候群(MIS-C)などを合併することがある
- 罹患後症状(post-COVID-19 condition)
- WHOの定義:罹患後2か月以上続く急性期症状や新たな症状の出現や再燃

- 病原体診断
- 核酸検出検査
SARS-COV-2に特異的なRNA遺伝子配列を増幅・検出する検査法
感染後のPCR陽性の継続期間は平均44.9日間(最長82日後、韓国)であった- リアルタイムPCR:ウイルスのコピー数の比較や推移が推定できることなどから信頼性が高い
- LAMP法、TMA法:設備が簡便で、35~50分程度で完了するが若干感度が低い
- 抗原検査
抗原定性検査は有症状者(発症から9日以内)の確定診断に用いる検査法
抗原定量検査は特異度も高く、無症状者のスクリーニングとしても利用できる - 血清診断(抗体検査)
実験室で用いる試薬は存在するが、日本国内で承認された製品はまだ存在しない
- 核酸検出検査

小児例の特徴
- オミクロン流行期では、小児入院症例の低年齢化(中央値6.0歳)と基礎疾患有病率の上昇(有病率12.6%)が認められた
- オミクロン株では、発熱、咽頭痛、痙攣が増加し、嗅覚・味覚障害は減少した
- デルタ株流行期にはICU入室症例の増加を認め、オミクロン株でもほぼ同等
- 成人に比し少ないが、3.5%に罹患後症状(頭痛、倦怠感、発熱、咳嗽、嗅覚・味覚障害、腹痛、下痢など)を認める
- 重症化は基礎疾患ありで5.1%、なしでは0.2%
- 入院例の年齢層は未就学児49.3%、小学生29.6%でほぼ8割を占める
- 2022年の国内小児死亡例は41人/8か月であった(5人/月程度)
- 小児へのオミクロン株感染経路は家庭内47%、学校・幼稚園23%、不明25%
行政・届出
- 全数把握は継続するが、医療機関の患者発生届け出は重症化リスク例に限定
- 医師による最寄り保健所への届出義務・・・4種類
- 65歳以上の者
- 入院を要する者
- 重症化リスクがあり、かつ、新型コロナ治療薬の投与が必要な者 または
重症化リスクがあり、かつ、新型コロナ罹患により新たに酸素投与が必要な者 - 妊婦
- COVID-19で死亡した症例も保健所に届け出る必要がある(上記基準と関係なし)
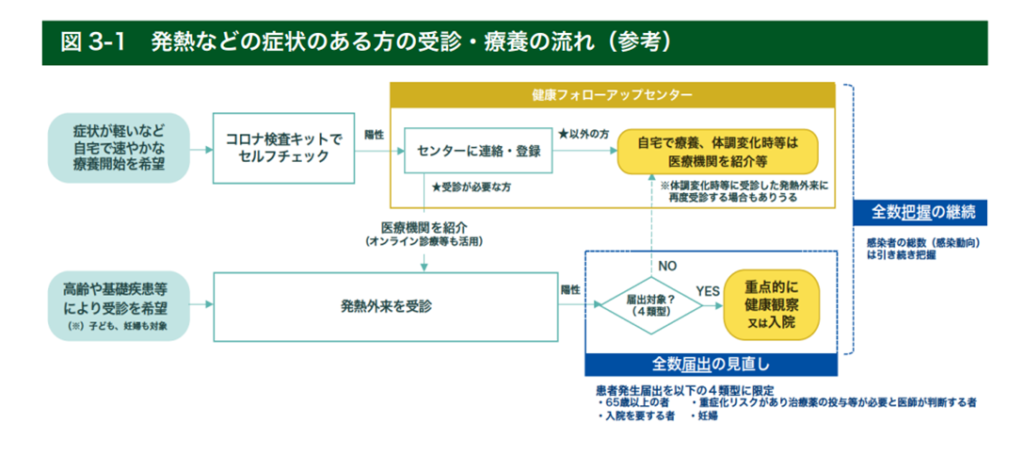
重症度診断

- 軽症
-
「パルスオキシメーター」で測る血液中の酸素の値が96%以上あり、咳は出ても息苦しさはなく、肺炎にはなっていない状態です。自然に回復することが多いものの、病状が急速に進行することもあり、慢性の腎臓病や肥満など、重症化のリスクが高い患者は、入院の対象となるとしています。
- 中等症I
-
血中の酸素の値が、93%から96%の間で、息苦しさや肺炎が認められる状態です。中には酸素の値が低下しても、患者が息苦しさを訴えないケースもあるため、入院をした上で、慎重に観察することが求められるとしています。
- 中等症II
-
血中の酸素の値がさらに下がって93%以下で自力での呼吸が難しく、酸素投与が必要な状態で、高度な医療を行える施設への転院を検討するとしています。
- 重症
-
肺炎が進行して、自力での呼吸ができず、全身に炎症が出たりする状態で集中治療室での治療や人工呼吸器を使った治療が必要。さらに容体が悪化すると、人工心肺装置=「ECMO」を使う場合もあるとしています。
- SpO2 の誤差が3%程度予測されるので、酸素投与の基準を93%と設定した
ワクチン
ワクチンの効果
- 発症予防効果
- オミクロン株に対する発症予防効果(2回接種後6か月の発症予防効果約50%)
- 重症化予防効果
- オミクロン株に対する死亡リスク減少(未接種0.3%→2回接種後0.08%、追加接種者0.07%)
- とくに80~90歳代の重症化リスクは大きく低下させる(未接種者8-9%→3回接種者1-2%)

ワクチンの接種期間
- 原則:令和2年10月1日から、異なるワクチンの接種間隔について、注射生ワクチンどうしを接種する場合は27日以上あける制限は維持しつつ、その他のワクチンの組み合わせについては、一律の日数制限は設けないこととなった
- 「注射生ワクチン」の接種後27日以上の間隔をおかなければ、「注射生ワクチン」の接種を受けることはできない
- それ以外のワクチンの組み合わせでは、前のワクチン接種からの間隔にかかわらず、次のワクチンの接種を受けることができる
- コロナワクチンとインフルエンザワクチンは同時接種可能
- コロナとその他のワクチンは自治体によっては14日程度(2週間後の同曜日から接種可)の間隔をあけているところもあるが、創傷時の破傷風トキソイド等、緊急性を要するものに関しては、例外として2週間をあけずに接種することが可能としている

ワクチンの種類について
注射生ワクチン:麻しん風しん混合ワクチン・水痘ワクチン・BCGワクチン・おたふくかぜワクチン など
経口生ワクチン:ロタウイルスワクチン など
不活化ワクチン:ヒブワクチン・小児用肺炎球菌ワクチン・B型肝炎ワクチン・4種混合ワクチン・
日本脳炎ワクチン・季節性インフルエンザワクチン など
治療薬
- 抗ウイルス薬と中和抗体薬の併用はエビデンスがなく推奨されない

- レムデシビル:商品名ベクルリー点滴静注液(ギリアド・サイエンシズ)、2020年5月承認
- モルヌピラビル:商品名ラゲブリオ(メルク)、2021年12月に特例承認、初めての経口抗ウイルス薬
- ニルマトレルビル/リトナビル:商品名パキロビッドパック(ファイザー)、2022年2月に特例承認
- エンシトレンビルフマル酸:商品名ゾコーバ(塩野義)、2022年11月に緊急承認
重症化リスク因子を1つ以上有する症例を対象とした臨床試験一覧
(重症化リスク因子は試験ごとに異なる)

抗ウイルス薬
オミクロン以後のエビデンス
90歳以上の患者でも、オミクロン株では、5%未満の致死率→そもそも治療適応?
△ラゲブリオ
オミクロン株流行前→重症化を予防する効果(入院や死亡を減らす効果)は約30%と報告
オミクロン株流行後→ラゲブリオは重症化を予防する効果を認めなかった
→変異を繰り返した新型コロナウイルス感染症に対しては、ラゲブリオは有効とは言い切れない状況
◎パキロビットパック
オミクロン株流行前→重症化を予防する効果は約89%と報告
オミクロン株流行後→40~64歳の方では重症化を予防する効果は認めず、65歳以上の方は重症化予防効果を認めた(下図)
パキロビットパックは令和5年3月から一般流通となっている
1回10万円

N Engl J Med 2022;387:790-798
- パキロビッドパックは、安定的な供給が難しいことから、一般流通は行わず、当面の間、厚生労働省が所有した上で、対象となる患者が発生又は発生が見込まれる医療機関(病院、有床診療所及び無床診療所)及び薬局からの依頼に基づき、無償で譲渡される
- 令和4年9月16日から、ラゲブリオカプセルの一般流通が開始された
- パキロビッドパックとラゲブリオの対象者は重症化リスクを有する者に限定、発病してから5日以内に使うことが原則
- パキロビッドパックは効果はあるが、併用薬の禁忌項目が多く、認められた薬局や医療機関にしか配られていない
- ラゲブリオは一般流通が開始され入手可能だが、治療効果は4割~6割程度でパキロビッドパックに劣る
- ゾコーバは重症化リスクを有さない若い人でも処方可能だが、実際には不要な薬である
- 以上から、経口薬の重要度はパキロビッドパック>ラゲブリオ>>ゾコーバとなる

ラゲブリオ/モルヌピラビル
- 重症化リスクを要する軽症者・中等症Iに投与可能
- 入手が容易で一般診療で使用可能
ゾコーバ錠/エンシトレンビル フマル酸
- 薬価:1錠7407.4円、1治療で5万1851.8円
- 元気な若者にも投与可能な唯一の薬だが、使用価値があるかは疑問
- 塩野義製薬が日本で創薬した薬(海外にはまだない)、適正使用ガイド
- 国内で使用可能(緊急承認、2022年11月22日~)
- 「適格性情報チェックリスト」、「患者同意説明文書」(→ゾコーバ登録センターに掲載)を記入する
特例承認よりもさらに迅速に承認するための新制度。特例承認は、すでに海外で流通している医薬品が対象だが、緊急承認はまだ海外で流通していない医薬品も対象となる。緊急承認は治療薬だけでなく、ワクチンなども対象となり、主にMade in JAPANの薬剤の国内早期承認を目指すための制度。
パキロビッドパック/ニルマトレルビル錠・リトナビル錠
- ファイザー製薬、適正使用ガイド
- 作用機序:ニルマトレルビルはSARS-CoV-2のメインプロテアーゼ(Mpro:3CLプロテアーゼ又はnsp5とも呼ばれる)を阻害し(IC50=19.2nmol/L)、ポリタンパク質の切断を阻止することで、ウイルス複製を抑制します。リトナビルはニルマトレルビルのCYP3Aによる代謝を阻害し、血漿中濃度を増加させます。
- 適応疾患:SARS-CoV-2による感染症(重症化の予防という位置づけ、重傷者の治療ではない)
- SARS-CoV-2による感染症の重症化リスク因子を有する等、本剤の投与が必要と考えられる患者に投与すること
- 重症度の高いSARS-CoV-2による感染症患者に対する有効性は確立していない
- 臨床成績(国際共同第Ⅱ/Ⅲ相試験[C4671005(EPIC-HR)試験)
- 無作為化されたすべての被験者2,246例(日本人6例)における補足的な解析での主要評価項目(mITT集団)の
- 結果は、ニルマトレルビル及びリトナビル併用群で入院5/697例(0.7%)、死亡0/697例(0%)であり、プラセボ群で入院44/682例(6.5%)、死亡9/682例(1.3%)でした。
- 用法用量:成人および12歳以上かつ体重40 kg以上の小児に、ニルマトレルビル1回2錠、リトナビル1回1錠を同時に1日2回、5日間経口投与
- 症状発現から速やかに投与を開始すること(症状発現から5日まで)
- 中等度の腎機能障害患者(eGFR[推算糸球体ろ過量]30mL/min以上60mL/min未満)には、ニルマトレルビルとして1回150mg及びリトナビルとして1回100mgを同時に1日2回、5日間経口投与すること。重度の腎機能障害患者(eGFR 30mL/min未満)への投与は推奨しない。
- 併用禁忌薬が非常に多い、肝障害や腎障害者も要注意
- 国内で使用可能(特例承認、2022年2月~)
- 特例承認→承認時において有効性、安全性、品質に係る情報は限られており、引き続き情報を収集中で、データが収集された後に有効性や安全性が改めて評価される予定
- 特例承認とは、外国で本剤が既に対象となる疾患の治療に用いられていることを条件に、国民の生命および健康に重大な影響を与えるおそれのある病気のまん延等を防止するための緊急の使用が必要な医薬品について、厚生労働大臣が、専門家の意見を聞いた上で通常の承認の要件を満たさない場合でも承認が可能となる制度


ベクルリー点滴静注/レムデシベル
- 入院を要する患者の第一選択薬(特に中等症IIでは必須、中等症Iでも使用可)
- 中等症・重症COVID-19を対象とした5つのRCTでは、重症例には効果が期待できないが、中等症には有効
- 日本では、中等症Iでも投与可能
- 原則として5日間投与する
- 重症化リスクを有する軽症例にも使用可能となった(入院または死亡を87%減少させた、PINETREE試験)
- 重度の腎機能障害への投与は推奨されないが、禁忌ではない(透析でも使用可)
新型コロナウイルスの治療薬として承認申請が行われている「アビガン」について、富士フイルムは治験の結果、重症化を抑える効果が確認できなかったとして、コロナの治療薬としての開発を中止し、承認申請を取り下げた。会社側は、重症化リスクがある20歳以上の軽症のコロナ患者を対象に、新たな枠組みで治験を進めたが、集まった84人のデータを解析した結果、重症化を抑えるとする有意な結果は得られなかった。富士フイルムによれば「感染拡大の当初は新型コロナの治療薬の候補がなく、既存の薬を転用する形で開発が進んだが、病態の解明も進み役割を終えたと考えている」。
中和抗体薬
ゼビュディ点滴静注/ソトロビマブ
- オミクロン株に対して効果減弱、その他の治療法が優先される
- 2021年9月、特例承認
ロナプリーブ / カシリビマブ/イマデビマブ
- オミクロン株に対して効果減弱、その他の治療法が優先される
- 2021年7月、特例承認
エバシェルド筋注セット/チキサケビマブ及びシルガビマブ
- オミクロン株に対して効果減弱、その他の治療法が優先される
- 2022年8月、特例承認
退院基準・療養解除基準
- 症状のある方は発症から丸10日間 、症状のない方は発症から丸7日間が経過するまでは感染リスクが残る



感染対策
マスク
- 一般的な粒子の大きさはスギ花粉が約30㎛、動物の体細胞が約10㎛、会話やくしゃみでの飛沫が5㎛以上、飛沫核が5㎛未満、PM2.5が2.5㎛、細菌約1㎛、ウイルス0.02~0.3㎛。一般的なマスクではPM2.5は防げない。
- マスクの性能はN95マスク>サージカルマスク>=一般的な不織布マスク
- 一般的な不織布のマスク
-
不織布とは繊維を織らずに絡み合わせたシート状の布で、繊維を絡み合わせたもので通気性があるため当然、繊維と繊維の隙間がある。ウイルス自体はこの隙間を十分に通れるくらい小さいが、ウイルスは飛沫として飛んでいるため、不織布マスクで十分にキャッチすることができ一般的なマスクでも十分に感染対策に貢献することがわかっている。Lancetに2020年6月27日に掲載された論文(16か国で行われた172の観察研究のメタアナリシス)では、1m以上の距離を取っているのと、1m以下よりの距離しかない場合より、明らかにウイルスの伝播が少ないこと、フェイスマスクを使用しているとしていないのと比較して感染の可能性が明らかに低下すること、目の保護が感染の現象に関連することが示された。特にマスクに関しては、2647人を調査してオッズ比が0.15と高い予防効果が示されてた。また、理化学研究所が複数の大学と共同で行った研究では、マスクをしたときの飛沫の飛び方をスーパーコンピューター「富岳」を用いてシミュレーションした結果、不織布マスクを使用すれば、マスクをしていない状態と比較して吐き出し飛沫量を80%、吸い込み飛沫量を70%減らすことが示された。
- サージカルマスク(医療用マスク)
-
サージカルマスクは医療従事者が医療業務に従事する際に、自身や周囲の人を感染から守るために着床するマスクで、不織布でできているマスクがほとんどだが、家庭用のものよりフィルターの目が細かいものが使われている。ただ海外では一定の規格があるが、日本ではサージカルマスクの定義を細かく定めた規格は存在せず米国の医療用マスクの規格に沿ったものが基本的にはサージカルマスクとみなされることが多い。
- N95マスク(防塵マスク)
-
よりフィルターが細かく、細かい粒子をキャッチできるマスク。N95とは塩化ナトリウム(空力学的質量径0.3μm)の捕集効率試験で95%以上捕集することを意味している(通常のマスクだと5μmの粒子をキャッチする)。家庭用の不織布マスクも十分な性能があるため、家庭用マスクを着用することで十分な予防効果が得られると考えられる。
米国ではASTM(米国試験材料協会)で医療用マスクの性能条件(ASTM F2100-19)を定めており、「レベル1」「レベル2」「レベル3」に分類されている。日本の基準としてはJIS T9001(医療用及び一般用マスクの性能要件及び試験方法)があるが、基準はASTM基準をそのまま踏襲している。


- PFE(Particle Filtration Efficiency)
-
「微粒子ろ過効率」のことで、約0.1㎛(マイクロメートル)サイズの粒子をどれくらいろ過(捕集)できたのかを表す。インフルエンザウイルス、ウイルス単体(飛沫核)、結核菌ウイルスなどが対象。「PFE95%」という表記であれば、約0.1㎛サイズの粒子を95%ろ過(捕集)するということ。
- BFE(Bacterial Filtration Efficiency)
-
「バクテリア(細菌)ろ過効率」のことで約3㎛の細菌を含む粒子がどれくらいろ過(捕集)できたのかを表す。花粉や咳・くしゃみに伴う水分を含んだウイルスの飛沫などが対象。「BFE95%」という表記であれば、約3μmの細菌を含む粒子を95%ろ過するということ。
- VFE(Viral Filtration Efficiency)
-
「ウイルスろ過効率」のことで約0.1㎛~5.0㎛のウイルスが含まれた粒子がどれくらいろ過(捕集)できたのかを表す。インフルエンザウイルス、咳・くしゃみを伴う水分を含んだウイルスの飛沫などが対象。「VFE99%」という表記であれば、約0.1μm~5.0μmのウイルスが含まれた粒子を99%ろ過するということ。
日本産業規格(JIS=Japanese Industrial Standardsの略)。日本の産業製品に関する規格や測定法などが定められた日本の国家規格のこと。自動車や電化製品などの産業製品生産に関するものから、文字コードやプログラムコードといった情報処理、サービスに関する規格などもある。